SCI论文(www.lunwensci.com)
摘要:目的 探讨人类表皮生长因子受体 -2 ( Her-2 ) 阳性乳腺癌患者经曲妥珠单抗与帕妥珠单抗联合化疗后,对患者肿瘤标志物与 免疫功能指标的影响。 方法 按照随机数字表法将 2018 年 1 月至 2021 年 11 月期间宜兴市肿瘤医院收治的 60 例 Her-2 阳性乳腺癌患者分 为参照组(曲妥珠单抗、多西他赛联合治疗) 与研究组(曲妥珠单抗、多西他赛、帕妥珠单抗联合治疗) ,每组 30 例, 3 周为 1 个疗程, 均治疗 4 个疗程。对比两组患者治疗后疾病控制率,治疗前后糖类抗原 125 ( CA125 ) 、癌胚抗原( CEA ) 、糖类抗原 153 ( CA153 )水 平及 T 细胞亚群指标水平, 以及治疗期间不良反应发生情况。 结果 研究组与参照组患者的疾病控制率分别为 96.67% 、73.33% ,研究组 较参照组显著升高;较治疗前, 治疗后两组患者血清 CEA 、CA125 、CA153 水平及 CD3+ 百分比、 CD4+/CD8+ 比值、 CD4+ 百分比均显著 降低, CD8+ 百分比均显著升高, 但研究组 CEA 、CA125 、CA153 水平及 CD8+ 百分比均较参照组显著降低, CD3+ 百分比、 CD4+/CD8+ 比 值、 CD4+ 百分比均较参照组显著升高(均 P<0.05 ) ;参照组与研究组患者不良反应总发生率分别为 16.67% 、23.33% ,组间比较,差异 无统计学意义(P>0.05 )。 结论 Her-2 阳性乳腺癌患者经曲妥珠单抗与帕妥珠单抗联合化疗后, 可对血清肿瘤标志物水平进行抑制, 疗 效显著,同时对患者机体细胞免疫功能的影响较小,且不增加不良反应。
关键词:人类表皮生长因子受体 -2.乳腺癌,帕妥珠单抗,曲妥珠单抗,多西他赛,癌胚抗原,糖类抗原125.糖类抗原153
乳腺癌为女性最常见的恶性肿瘤之一,具有较高的发 病率,随着病情的不断进展,可引起恶病质综合征、全身 转移等 [1] 。人类表皮生长因子受体 -2 ( Her-2)基因扩增 或过度表达是乳腺癌患者特殊的临床特点,且报道显示, 高达 30% 的乳腺癌患者会出现上述情况,由于患者早期 症状并无特异性,就诊时已处于晚期,多需进行化疗治 疗 [2] 。多西他赛主要通过干扰细胞有丝分裂、分裂间期细 胞功能所必需的微管网络,而起到抗肿瘤作用;曲妥珠单 抗属于一种靶向治疗药物,可有效作用于 Her-2.从而杀 伤肿瘤细胞,但仍有部分 Her-2 过表达患者在治疗过程中 产生耐药性,难以有效控制病情发展 [3] 。帕妥珠单抗为一 种 Her-2 受体拮抗剂,多以 Her-2 为靶点进行治疗,主要 通过抑制配体 - 启动细胞内信号的两条主要信号通路,使 肿瘤细胞生长停止并促进其凋亡,抑制肿瘤细胞增殖,被 广泛应用于 Her-2 阳性转移性乳腺癌的一线治疗与 Her-2 阳性乳腺癌的辅助治疗 [4] 。本研究旨在探讨 Her-2 阳性乳 腺癌患者经曲妥珠单抗与帕妥珠单抗联合化疗后,对其临 床疗效的影响,现报道如下。
1 资料与方法
1.1 一般资料 将宜兴市肿瘤医院 2018 年 1 月至 2021 年 11 月期间收治的 Her-2 阳性乳腺癌患者 60 例,按照随机数字表法分为参照组与研究组,每组 30 例,参照组患 者年龄 29~55 岁,平均(42.00±8.50 )岁;病程 2~6 个 月,平均(4.00±0.56 )个月;肿瘤 TNM 分期 [5]:Ⅱ b 期 16 例、Ⅲ a 期 14 例;肿瘤部位:左侧 17 例,右侧 13 例。研究组患者年龄 28~55 岁,平均(41.50±8.45)岁; 病程 3~5 个月,平均(4.00±0.50 )个月;肿瘤 TNM 分 期:Ⅱ b 期 17 例,Ⅲ a 期 13 例;肿瘤部位:左侧 16 例, 右侧 14 例。两组患者一般资料比较,差异无统计学意义 ( P>0.05),组间可比。纳入标准:符合《Her-2 阳性乳腺 癌临床诊疗专家共识》 [6] 中关于 Her-2 阳性乳腺癌的诊断 标准者;免疫组织化学染色确诊为 Her-2 阳性者;预计 生存期 >10个月者;肿瘤未发生远处转移者。排除标准: 具有其他恶性肿瘤疾病者;肝、肾功能障碍者;合并血液 系统、免疫系统、感染性疾病者;脑膜转移者;无法耐受 化疗方案者。院内医学伦理委员会已批准此研究,患者或 家属签署知情同意书。
1.2 治疗方法 患者接受常规对症治疗,包括予以保肝 药物、止吐,并给予营养补充疗法 [7] 。在此基础上采用多 西他赛注射液(Sanofi-Aventis Deutschland GmbH,注册证 号 J20150083.规格: 1.0 mL ∶20 mg)治疗,75 mg/m2 ,溶 于 250 mL 的 0.9% 氯化钠溶液,进行静脉滴注, 1 次 /3 周。在上述治疗基础上,参照组患者加用注射用曲妥珠单抗 ( Genentech Inc. ,注册证号 S20181016.规格: 440 mg/ 瓶) 治疗,静脉滴注,8 mg/kg 体质量为初始负荷量,静脉滴注 90 min,1 次 /3 周,此为第 1 个疗程;自第 2 个疗程起, 静脉滴注 6 mg/kg 体质量,滴注时间 1.5 h 以内,1 次 /3 周 ( 1 个疗程),共治疗 4 个疗程。在参照组的基础上研究组 患者加用帕妥珠单抗注射液( Roche Diagnostics GmbH , 注册证号 S20180029.规格: 420 mg/ 瓶)治疗,静脉滴 注,840 mg/ 次,1 次 /3 周,此为第 1 个疗程,自第 2 个疗 程起,将其剂量改为 420 mg/ 次,1 次 /3 周( 1 个疗程), 共治疗 4 个疗程。
1.3 观察指标 ①参照《Her-2 阳性乳腺癌临床诊疗专家 共识》 [6] 中的相关诊断标准评估两组患者肿瘤控制效果, 肿瘤完全消失,肿瘤标志物水平处于正常范围,且持续 1 个月以上为完全缓解;病灶最大直径相加之和缩小 30%, 肿瘤标志物水平高于正常范围,且持续 1 个月以上为部分 缓解;靶病灶病灶最大直径相加之和缩小≤30% 或增大 <20% 为疾病稳定;病灶最大直径之和增大≥20%,并出 现≥ 1 个新病灶为疾病进展。疾病控制率 = 完全缓解率+ 部分缓解率 + 疾病稳定率。②取患者空腹静脉血 3 mL, 经 3 500 r/min 转速离心 10 min 后,取血清,采用电化学 发光免疫分析仪(上海聚慕医疗器械有限公司,型号: CL50)检测糖类抗原 125 ( CA125)、癌胚抗原(CEA )、 糖类抗原 153 ( CA153 )水平。③治疗前后 CD3+、CD4+、 CD8+ 百分比,血液采集方法同②,由流式细胞仪(北京 赛泰克生物科技有限公司,型号:Aurora)检测,并计算 CD4+/CD8+ 比值。④统计患者治疗期间不良反应(胃肠道 反应、关节肌肉痛、皮疹、肝功能损害等)发生情况。 1.4 统计学方法 采用 SPSS 22.0 统计学软件分析数 据,计数资料(肿瘤控制效果与不良反应发生情况)以[ 例 (%)] 表示,采用 χ2 检验;计量资料( CEA、CA125、 CA153 水平及免疫功能指标)均经 K-S 法检验证实符合正 态分布,以 (x ±s) 表示,组内治疗前后比较采用配对 t检 验,两组间比较采用独立 t 检验。以P<0.05 表示差异有 统计学意义。
2 结果
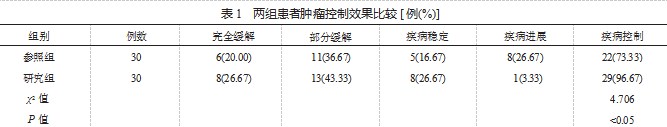
2.1 两组患者肿瘤控制效果比较 参照组、研究组患者 的疾病控制率分别为 73.33%、96.67%,研究组显著高于参 照组,差异有统计学意义(P<0.05),见表 1.
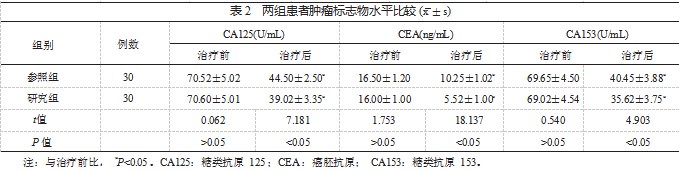
2.2 两组患者肿瘤标志物水平比较 与治疗前比,治疗 后两组患者各项肿瘤标志物水平均显著降低,研究组显著 低于参照组,差异均有统计学意义(均 P<0.05),见表 2.
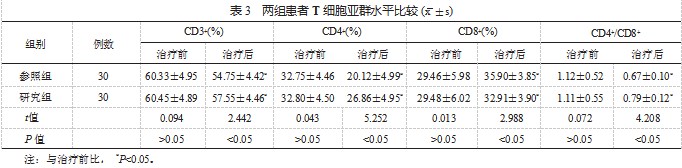
2.3 两组患者 T 细胞亚群水平比较 与治疗前比,治 疗后两组患者 CD3+、CD4+ 百分比、CD4+/CD8+ 比值均显 著降低,但研究组显著高于参照组; CD8+ 百分比显著升 高,但研究组显著低于参照组,差异均有统计学意义(均 P<0.05),见表 3.
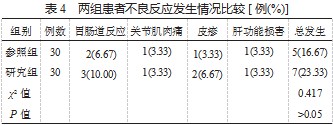
2.4 两组患者不良反应发生情况比较 参照组、研究组 患者不良反应总发生率分别为 16 .67%、23 .33%,组间比 较,差异无统计学意义(P>0.05),见表 4.
3 讨论
乳腺癌主要是发生在乳腺上皮组织的恶性肿瘤, Her-2 基因为一种原癌基因, 主要位于人体 17 号染色体长臂上, 属于人表皮生长因子受体(Her)家族, 具有酪氨酸蛋白激 酶活性,会经过多种途径,抑制肿瘤细胞凋亡,促进其增 殖,促使肿瘤细胞发生转移。随着抗 Her-2 靶向药物的出 现,乳腺癌的综合治疗方案也在不断更新。多西他赛为治疗 乳腺癌的常用药物,可与多种肿瘤细胞内微管蛋白结合, 形成稳定的微管,抑制其聚集,从而对肿瘤细胞的有丝分 裂进行拮抗,但也会对患者机体内正常细胞产生影响,影响患者免疫功能 [8];曲妥珠单抗是治疗乳腺癌的一种Her-2 靶向药物,可以选择性地作用于 Her-2 的细胞外部分,对 Her-2 介导的信号转导通路具有阻断作用,从而可使细胞膜 Her-2 蛋白浓度明显降低, 促使 Her-2 受体蛋白加速降解, 有效参与抗血管生成,抑制细胞生长,诱导细胞凋亡;但 相关研究中显示,相比于单靶向药物联合化疗治疗 Her-2 阳性乳腺癌患者,双靶向联合化疗治疗的患者临床缓解率 更高,且在常规化疗方案的基础上联合双靶药物治疗并未 增加 Her-2 阳性乳腺癌患者的不良反应 [9- 10]。
帕妥珠单抗是一种人源化的单克隆抗体,能够与Her-2 受体选择性的结合,抑制肿瘤细胞的生长与增殖,进而控 制病情发展,疗效显著;且帕妥珠单抗通过与 Her-2 二聚 化结构域结合, 抑制Her-2 与其他Her 家族受体的异源二聚 化,在扰乱 Her 家族其他复合物的形成方面较曲妥珠单抗 更为有效,因此对于 Her-2 阳性乳腺癌患者抗肿瘤效果更 为显著 [11- 12] 。CEA、CA125、CA153 作为常见的肿瘤标志 物,在乳腺癌患者体内呈升高表达,其水平越高,病情越 严重 [13]。本研究中, 参照组与研究组患者的疾病控制率分 别为 73.33%、96.67%,研究组较参照组显著升高, 且治疗 后研究组患者 CEA、CA125、CA153 水平均显著低于参照 组,提示 Her-2 阳性乳腺癌患者经曲妥珠单抗与帕妥珠单 抗联合化疗后,可有效降低机体的血清肿瘤标志物水平, 提高治疗效果。
T 淋巴细胞具有多种效应、免疫调节功能等作用,在乳 腺癌患者体内,肿瘤免疫缺陷是机体免疫功能低下导致的, 自身免疫抑制和对肿瘤细胞免疫应答的减少会降低患者机 体识别和杀伤突变细胞的能力,进而促进肿瘤转移 [14] 。 本研究中,较治疗前,治疗后两组患者 CD3+ 百分比、 CD4+/CD8+ 比值、 CD4+ 百分比均显著降低,但研究组显 著高于参照组,CD8+ 百分比均显著升高,但研究组显著低于参照组;对照组、参照组患者不良反应总发生率分别 为 16.67%、23.33%,组间比较,差异无统计学意义,提 示 Her-2 阳性乳腺癌患者经曲妥珠单抗与帕妥珠单抗联合 化疗后,对患者机体细胞免疫功能的影响更小,且安全性 良好。分析其原因可能为,常规化疗在杀灭肿瘤细胞的同 时,也会对机体正常细胞造成严重的损害,因此需结合靶向 治疗药物,减轻化疗对机体免疫力的影响,本研究中,曲 妥珠单抗特异性结合 Her-2 蛋白在细胞膜外的第 4 个功能 域, 阻断信号转导, 介导细胞免疫作用杀伤肿瘤细胞 [15]; 帕妥珠单抗主要靶向作用于 Her-2 受体的胞外受体结构域Ⅱ(二聚体区域) ,可阻断 Her-2 受体的激活,进而阻断 信号转导,特异性地杀死肿瘤细胞,曲妥珠单抗与帕妥珠 单抗双靶治疗,常常相得益彰,多靶点攻击肿瘤细胞,对 正常细胞损伤小,可减轻对患者机体免疫功能的损伤,改 善患者预后 [16- 17]。
综上,Her-2 阳性乳腺癌患者经曲妥珠单抗与帕妥珠单 抗联合化疗后,可对血清肿瘤标志物水平进行抑制,疗效 显著,同时对免疫功能的影响较小,且不增加不良反应, 临床上可推广与应用。
参考文献
[1] 曹萌 , 刘相麟 , 刘喆赢 , 等 . 汉曲优与帕妥珠单抗联合化疗新辅助治疗 HER-2 阳性乳腺癌疗效和安全评价 [J]. 中国临床研究 ,2022. 35(3): 319-324.
[2] NAGARAJ G, MA C X. Clinical challenges in the management ofhormone receptor-positive, human epidermal growth factor receptor 2-negative metastatic breast cancer: A literature review[J]. Adv Ther, 2021. 38(1): 109- 136.
[3] 惠广盈 , 郭艳绒 , 阮稳稳 . 曲妥珠单抗联合多西他赛对 HER-2 阳性中晚期乳腺癌患者血清肿瘤标志物及免疫功能的影响 [J]. 中 国肿瘤临床与康复 , 2019. 26(11): 1180- 1183.
[4] 程元甲 , 徐玲 , 叶京明 , 等 . 帕妥珠单抗与曲妥珠单抗联合化疗在早期乳腺癌新辅助治疗中的疗效评价 [J/CD]. 中华临床医师杂 志 ( 电子版 ), 2020. 14(5): 344-348.
[5] 刘爱军, 卢丽清, 张建萍. TE 方案与CEF 方案比较治疗中国女性TNM 分期ⅡA ~ Ⅲ C 乳腺癌的有效性和安全性的Meta 分析 [J]. 中国循证医学杂志 , 2017. 17(12): 1413- 1418.
[6] 中国抗癌协会乳腺癌专业委员会 . Her-2 阳性乳腺癌临床诊疗专家共识 [J]. 中国癌症杂志 , 2012. 22(4): 314-318.
[7] 王慧 , 赵安帝 , 杨谨 . 曲妥珠单抗联合帕妥珠单抗用于 HER2 阳性早期乳腺癌研究进展 [J]. 华中科技大学学报 ( 医学版 ), 2020. 49(1): 111- 116.
[8] 刘淑珍 , 温涛 , 陈伟焱 . 曲妥珠单抗联合多西他赛对乳腺癌的疗效分析 [J]. 中国药物与临床 , 2015. 15(11): 1550- 1552.
[9] 黄世芬 . 帕妥珠单抗联合曲妥珠单抗在 HER-2 阳性乳腺癌新辅助治疗中的疗效及影响因素分析 [D]. 兰州 : 兰州大学 , 2021.
[10] 顾文静 . 通阳祛瘀中药联合曲妥珠单抗治疗乳腺癌疗效及对血清 CEA、CA153、CA724 的影响 [J]. 现代中西医结合杂志 , 2017.26(23): 2599-2601.
[11] 贾才凤 , 张森 , 徐浩 , 等 . 帕妥珠单抗联合曲妥珠单抗、多西他 赛一线治疗HER2 阳性转移性乳腺癌的成本- 效用分析 [J]. 中国 药房 , 2022. 33(4): 481-486.
[12] 李原 , 乔进余 , 刘芳 . 帕妥珠单抗联合含多柔比星脂质体治疗表 皮生长因子受体 2 阳性晚期乳腺癌的临床效果 [J]. 中国临床实 用医学 , 2018. 9(6): 37-39.
[13] 马善义 , 马俊 , 吴芳芳 , 等 . 曲妥珠单抗联合帕妥珠单抗在HER2过表达乳腺癌中的应用价值 [J]. 临床与病理杂志 , 2021. 41(7): 1573- 1578.
[14] 刘刚 , 薛孝斌 , 任冬莉 . 外周血 T 淋巴细胞亚群变化对乳腺癌新 辅助化疗疗效的预测价值 [J]. 海南医学 , 2022. 33(7): 864-868.
[15] 肖聪 , 张懿敏 , 孙圣荣 . 曲妥珠单抗联合 CAF 化疗治疗晚期乳腺癌临床效果观察 [J]. 临床军医杂志 , 2019. 47(4): 368-370. 374.
[16] 刘晨 , 杨志光 , 路云 , 等 . 帕妥珠单抗联合曲妥珠单抗治疗HER-2 阳性乳腺癌的 Meta 分析 [J]. 中国新药杂志 , 2019. 28(24): 3035-3041.
[17] 姜战胜 , 杨艳芳 , 潘战宇 . 帕妥珠单抗在 HER-2 阳性乳腺癌治 疗中的临床转化 [J]. 中国肿瘤生物治疗杂志 , 2016. 23(4): 545- 549.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/53855.html