SCI论文(www.lunwensci.com)
【摘要】目的 研究曲妥珠单抗联合新辅助化疗( NACT ) 对人类表皮生长因子受体 -2 ( HER-2 ) 阳性乳腺癌患者的预后影响因素, 为临床治疗该疾病提供参考。 方法 回顾性分析 2011 年 1 月至 2017 年 12 月北京市普仁医院接受 NACT 治疗的 223 例 HER-2 阳性浸润性 乳腺癌患者的临床资料, 根据是否联合曲妥珠单抗治疗, 将患者分为非治疗组( 83 例)和治疗组( 140 例)。统计分析两组患者的临床特 征,随访期间统计患者肿瘤复发、远处转移、死亡情况;使用 Cox 比例风险回归模型分析患者死亡的影响因素。结果 治疗组导管原位 癌残留、术后辅助化疗、 Miller-Payne ( MP )分级 1~2 级的患者占比均显著低于非治疗组;患者的随访时间为 38~62 个月, 中位随访时间 57 个月,治疗组患者复发率、远处转移率及死亡率均显著低于非治疗组(P<0.05 ); Cox 比例风险回归模型单因素和多因素分析结果显 示, T1~2 分期、放疗及 MP 分级是影响 NACT 后 HER-2 阳性乳腺癌患者死亡的独立影响因素(HR=0.716 、0.583 、1.142.均 P<0.05 )。 结 论 曲妥珠单抗联合 NACT 可降低 HER-2 阳性乳腺癌患者的复发、远处转移及死亡风险;T 分期、放疗及 MP 分级 1~2 级是影响 NACT 治疗 HER-2 阳性乳腺癌患者死亡的独立危险因素,可根据上述因素采取相应措施进行干预,提高患者生存率,改善预后。
【关键词】 乳腺癌,曲妥珠单抗,新辅助化疗,人类表皮生长因子受体 -2 ,预后
乳腺癌是导致全球女性死亡的重要原因。人表皮生 长因子受体 -2 ( HER-2)在部分浸润性乳腺癌患者中存 在 HER-2 蛋白过表达和基因扩增现象,与 HER-2 阴性乳 腺癌患者比较,HER-2 阳性乳腺癌患者预后更差,恶性程 度高,且总生存时间(OS)短,远处转移和死亡风险更 高 [1] 。针对 HER-2 的单克隆抗体曲妥珠单抗,可选择性 地对 HER-2 蛋白细胞外区域产生作用,调节 HER-2 阳性 肿瘤细胞释放的拓扑异构酶Ⅰ表达,抑制肿瘤细胞增殖; 此外,曲妥珠单抗还可以激活固有免疫细胞以杀灭肿瘤细 胞,临床上已经将其用于非小细胞肺癌、胃癌、乳腺癌等 多种 HER-2 阳性肿瘤的治疗,持续抗 HER-2 治疗可有效 抑制癌细胞的增殖 [2]。HER-2 靶向治疗显著改善了新辅助 化疗(NACT)对 HER-2 阳性乳腺癌患者的预后,近年来 已证实 NACT 后患者可实现病理完全缓解(pCR) [3]。本 研究旨在探讨曲妥珠单抗联合 NACT 治疗 HER-2 阳性乳 腺癌患者预后影响因素,现报道如下。
1 资料与方法
1.1 一般资料 回顾性分析 2011 年 1 月至 2017 年 12 月 北京市普仁医院接受 NACT 治疗的 223 例 HER-2 阳性浸润性乳腺癌患者的临床资料,根据 NACT 是否联合曲 妥珠单抗治疗,将患者分为非治疗组( 83 例)和治疗组 ( 140 例)。诊断标准:参照《中国抗癌协会乳腺癌诊治指 南与规范(2008 版)》[4] 中的相关标准。纳入标准:符合 上述诊断标准者;初次治疗者;肿瘤分期为 T1-3、N1-3、M0 者;接受 NACT 治疗者;HER-2 蛋白阳性表达者;临床相 关资料完整者等。排除标准:合并其他恶性肿瘤者;存在 远处转移者;对曲妥珠单抗过敏者等。本研究经院内医学 伦理委员会批准。
1.2 治疗方法 所有患者均接受蒽环联合紫杉类 NACT 方案治疗:注射用盐酸多柔比星 [ 辉瑞制药(无锡) 有限公司,国药准字 H20013334 ,规格: 10 mg/ 支 ] 60 mg/m 2 ,第 1 天静脉滴注;紫杉醇注射液(北京 协和药厂有限公司,国药准字 H20083786 ,规格: 10 mL ∶ 60 mg ) 175 mg/m2 ,第 1 天静脉滴注;注射用 异环磷酰胺(哈尔滨三联药业股份有限公司,国药准字 H20084196.规格: 1.0 g/ 支) 600 mg/m2 ,第 1 天静脉 滴注,21 d 为 1 个疗程,共治疗 4 个疗程。治疗组患者 在上述治疗的基础上联合注射用曲妥珠单抗 [Genentech Inc. ,注册证号 J20180073.规格: 440 mg ( 20 mL )/ 瓶 ]治疗,初次负荷量为 4 mg/kg 体质量,之后 2 mg/kg 体质量,1 次 / 周,共治疗 12 周。NACT 后经影像学检查,均达到 完全缓解,结束后 3~4 周两组患者均进行手术治疗,保 乳手术患者于术中和术后前哨淋巴结阳性需进行腋窝淋巴 结清扫;对于肿瘤直径大于 5 cm 、保乳手术、切缘阳性、 腋窝淋巴结阳性患者建议进行放疗;雌激素受体( ER )、 孕激素受体(PR)阳性者进行内分泌治疗。
1.3 观察指标 ①统计并比较两组患者年龄、T 分期、ER、 PR 阳性情况、手术方法、是否腋窝淋巴结清扫、是否放 疗、是否导管原位癌残留(采用超声检查)、是否内分泌 治疗、是否术后辅助化疗、Miller-Payne( MP)分级 [5] (根 据 NACT 后患者肿瘤细胞减少的比例分为 1~5 级,1 级 表示肿瘤细胞未减少,5 级表示未见浸润癌细胞)等临床 特征。②对两组患者进行随访,统计患者死亡和复发情 况。③使用 Cox 比例风险回归模型对经 NACT 治疗的 HER-2 阳性乳腺癌患者的生存情况进行单因素和多因素 分析。
1.4 统计学方法 采用 SPSS 22.0 统计学软件分析数 据,计数资料以 [ 例 (%)] 表示,采用 χ2 检验;患者生存 情况影响因素采用 Cox 比例风险回归模型进行分析,以 P<0.05 为差异有统计学意义。
2 结果
2.1 两组患者临床特征情况比较 治疗组导管原位癌残 留、术后辅助化疗、MP 分级 1~2 级的患者占比均显著低 于非治疗组,差异均有统计学意义(均 P<0.05 ); 两组患 者年龄、T 分期、ER、PR 阳性情况、手术方法、腋窝淋巴 结清扫、放疗、内分泌治疗等情况经比较,差异均无统计 学意义(均 P>0.05),见表 1.
2.2 两组患者随访情况比较 患者的随访时间为 38~62 个月,中位随访时间为 57 个月,末次随访时间为 2022 年6 月。随访过程中,治疗组、非治疗组中局部复发分别为3、7 例;发生远处转移分别为 2、6 例;非治疗组 1 例同时 存在局部复发和远处转移;治疗组、非治疗组死亡分别为1、6 例。治疗组患者肿瘤复发率、远处转移率、死亡率分 别为 2. 14% ( 3/140 )、1.43% ( 2/140 )、0.71% ( 1/140),非治 疗组患者肿瘤复发率、远处转移率、死亡率分别为 9.64% ( 8/83 )、8.43% ( 7/83 )、7.23% ( 6/83),治疗组复发率、远处 转移率及死亡率均显著低于非治疗组,差异均有统计学意 义(χ2=4.747、4.917、5.289.均 P<0.05 )。
2.3 影响 NACT 后 HER-2 阳性乳腺癌患者生存情况的 单因素分析 本研究中共有 7 例患者死亡,单因素分析结 果显示,T1~2 分期、放疗及 MP 分级 1~2 级是影响 NACT 治疗后 HER-2 阳性乳腺癌患者预后的相关因素,差异均有统计学意义(HR=0.846、0.531、1.127.均 P<0.05), 见 表 2.
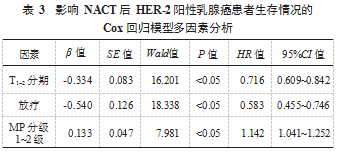
2.4 影响 NACT 后 HER-2 阳性乳腺癌患者生存情况 的多因素分析 将单因素分析中差异有统计学意义的因 素(T1~2 分期、是否接受放疗及 MP 分级)纳入 Cox 比例 风险回归模型进行多因素分析,结果显示,T1~2 分期、放疗及 MP 分级 1~2 级是影响 NACT 治疗后 HER-2 阳性 乳腺癌患者死亡的独立危险因素,差异均有统计学意义(HR=0.716、0.583、1.142.均 P<0.05),见表 3.
3 讨论
乳腺癌属于恶性肿瘤,发生于乳腺上皮细胞组织,其 治疗方法有手术、放化疗及内分泌治疗等,且化疗为主要 治疗方法。HER-2 高表达是乳腺癌患者病情进展的重要 原因,并且是判断乳腺癌预后的独立指标,曲妥珠单抗是 HER-2 阳性乳腺癌的一线靶向治疗药物,通过抑制患者 HER-2 基因的过度表达, 阻碍病情的进展。曲妥珠单抗属 于抗 HER-2 的单克隆抗体, 可附着于 HER-2 上,从而阻止 人体表皮生长因子附着在 HER-2 上,抑制癌细胞的生长, 同时其还可以刺激机体自身的免疫细胞去摧毁癌细胞,主 要应用于 HER-2 过度表达的转移性乳腺癌患者的治疗, 且 有研究显示,采用曲妥珠单抗进行辅助化疗,可有效降低 患者的复发率和死亡率 [6]。
本研究中首先对是否接受曲妥珠单抗治疗的两组患者 的临床特征进行比较, 结果显示, 治疗组导管原位癌残留、 术后辅助化疗、MP 分级 1~2 级的患者占比均显著低于非 治疗组,提示曲妥珠单抗联合 NACT 治疗 HER-2 阳性患 者可降低患者导管原位癌残留的风险,提高 MP 分级,且 可减少术后辅助化疗的应用,疗效确切。在对患者进行随 访的过程中,治疗组肿瘤复发率、远处转移率、死亡率均显著低于非治疗组,表明在进行新辅助化疗时联合曲妥珠 单抗可使乳腺癌患者的复发率和死亡率降低。孙愚等 [7] 对 HER-2 阳性乳腺癌患者的研究中也发现, 新辅助化疗联合 曲妥珠单抗后患者的无病生存期和OS 均长于单纯化疗组。 曲妥珠单抗能够作用于 HER-2 受体的胞外部分, 使 HER-2 与其他HER 家族基因形成异源二聚体的过程被阻断, 对丝 氨酸、苏氨酸激酶等酶的活性产生抑制作用,导致原癌基 因失活,从而阻止癌症的发生。
本研究中 Cox 回归模型分析发现,T1~2 分期、放疗 及 MP 分级 1~2 级是影响接受 NACT 后 HER-2 阳性乳腺 癌患者生存情况的独立因素。分析原因在于,T 分期越高 提示患者肿瘤越大、侵袭程度越高,患者预后相对更差; T 分期可以通过肿瘤大小对微小转移病灶和孤立性肿瘤结 节进行判断,以腋窝淋巴结转移数目作为分期的重要元 素,能够客观评价淋巴结转移对预后的影响 [8] 。而放疗作 为乳腺癌综合治疗的重要方式,其利用放射线能够将癌细 胞杀死,控制人体内癌细胞的 DNA 复制、分裂及增殖, 减缓肿瘤的发展速度,减轻患者的病痛;对于具有放疗适 应证患者进行放疗后可以降低其乳腺癌的复发风险,降低 患者死亡风险 [9] 。MP 分级是评估乳腺癌患者治疗前后肿 瘤细胞减少比例的重要参数,分级越高提示细胞减少越 多; MP 分级 5 级表明患者接受 NACT 治疗后原肿瘤部位 已无浸润性癌细胞,治疗效果达到了完全缓解,患者的 复发风险较其他 MP 分级更低,且远期生存率更高,预后 良好。
邵婉婷等 [10] 在对 HER-2 阳性乳腺癌患者采用曲妥珠 单抗联合新辅助化疗的治疗效果及其预后影响因素的研究 中发现,采用靶向联合化疗方案治疗的患者,其 OS 和无 病生存期均长于单纯化疗的患者;同时通过分析发现, 原发肿瘤大小、初诊与术后淋巴结情况及 MP 分级均是 HER-2 阳性乳腺癌患者 OS 和无病生存期的影响因素。
因此, MP 分级可用来预测曲妥珠单抗联合新辅助化疗后 HER-2 阳性乳腺癌患者的预后情况, 临床上应根据 HER-2 阳性乳腺癌患者的 T1~2 分期、是否进行放疗及 MP 分级对 患者进行筛选,对 T 分期较高、未接受放疗及 MP 分级 较低的患者及时采取术后辅助化疗等措施,以改善患者的 预后。
综上,曲妥珠单抗联合 NACT 治疗 HER-2 阳性乳腺 癌患者可降低患者复发风险;T1~2 分期、放疗及 MP 分级 1~2 级是NACT 治疗 HER-2 阳性乳腺癌影响患者死亡的独 立危险因素,可根据上述因素采取相应措施进行干预,提 高患者的预后效果。但本研究也存在一定局限性,首先本 研究为回顾性分析,易导致选择偏倚;其次,患者化疗方 案并未完全均衡,为了方便统计将单独使用蒽环类或紫杉 类化疗者进行了合并,这种差异可能影响最终研究结果准 确性;另外本研究受患者数量限制和随访时间的影响,未 进行亚组分析,今后值得更大样本量的前瞻性研究,进一 步明确该结论。
参 考 文 献
[1] NAGARAJ G, MA C X. Clinical challenges in the management of hormone receptor-positive, human epidermal growth factor receptor 2-negative metastatic breast cancer: a literature review[J]. Adv Ther, 2021. 38(1): 109- 136.
[2] 秦文婧 , 张双林 . 雌激素受体、孕激素受体及原癌基因 Her-2 在肺腺癌中的表达 [J]. 中国现代医生 , 2016. 54(12): 8- 10.
[3] 伍雁琦 , 罗婷 . 激素受体 / 人表皮生长因子受体 2 阳性乳腺癌治疗研究进展 [J]. 中国全科医学 , 2021. 24(8): 1028- 1032. 1036.
[4] 中国抗癌协会乳腺癌专业委员会 . 中国抗癌协会乳腺癌诊治指南与规范 (2008 版)[J]. 中国癌症杂志 , 2009. 19(6): 448-474.
[5] 李诚 , 张亚囡 , 张雅婷 , 等 . 乳腺癌新辅助化疗 Miller/Payne 分级病理疗效相关预测因子分析 [J]. 潍坊医学院学报 , 2020. 42(3): 218-221.
[6] 韩逸群 , 樊英 , 陈闪闪 , 等 . 跨线曲妥珠单抗治疗 HER2 阳性乳腺癌疗效分析 [J]. 临床药物治疗杂志 , 2019. 17(6): 71-75.
[7] 孙愚 , 李帅 , 罗婷 , 等 . 曲妥珠单抗联合新辅助化疗对 HER-2 阳性乳腺癌患者近远期疗效的影响 [J]. 实用癌症杂志 , 2016. 31(8): 1355- 1356.
[8] 姜朋丽, 付彤, 武盼盼, 等. 不同T 分期乳腺癌患者分子分型与腋窝淋巴结转移的关系及其临床意义 [J]. 吉林大学学报 ( 医学版),2016. 42(1): 144- 148.
[9] DUMA M N, BAUMANN R, BUDACH W, et al. Heart-sparing radiotherapy techniques in breast cancer patients: a recommendation of the breast cancer expert panel of the German society of radiation oncology (DEGRO)[J]. Strahlenther Onkol, 2019. 195(10): 861-871.
[10] 邵婉婷 , 付彤 , 武盼盼 , 等 . Her-2 阳性乳腺癌患者曲妥珠单抗联 合新辅助化疗的效果评价及其预后影响因素分析 [J]. 吉林大学 学报 ( 医学版), 2016. 42(2): 351-357.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/62431.html