SCI论文(www.lunwensci.com)
【摘要】 目的:对 420 例严重药品不良反应(ADR)报告进行系统分析。方法: 回顾性分析 2018 年 12 月至 2021 年 12 月鹤壁市 上报的 420 例严重 ADR 的临床资料,统计患者性别、年龄、给药途径、转归情况,ADR 报告者、关联性评价、药品种类和名称、上报例 数前 6 种药品及临床表现。结果: 420 例发生严重 ADR 患者中, 男 260 例, 占 61.90%, 女 160 例, 占 38.10%, 以男性居多, 以 60~79 岁 年龄段最多,占 42.62%;严重 ADR 给药途径以口服和静脉滴注占比最高,分别为 47.62% 和 42.62%;严重 ADR 报告者最多为药师,占 47.86%,其次为医生,占 38.10%;转归情况以痊愈和好转为主,其中痊愈 68 例,占 16.19%,好转 320 例,占 76.19%;关联性评价以可 能为主;药品种类以解热镇痛抗炎药和抗肿瘤药为主,其次是血液系统用药和抗感染药,发生严重 ADR 上报例数前 6 种的药品为阿司匹 林肠溶片、华法林片、多西他赛注射液、顺铂注射液、紫杉醇(白蛋白结合型)、硫酸氯吡格雷片,临床表现以血液系统损害和消化系统 损害为主。结论: 发生严重 ADR 的种类、原因各异,应加强解热镇痛抗炎药、抗肿瘤药、血液系统药和抗感染药的临床用药监测及患者 用药教育。
【关键词】 不良反应,监测报告,严重,药品,合理用药
Analysis of
ZHANG Yanrong1. ZHANG Feibiao2. LI Yuanyuan1. FENG Wenjuan3
[1. Hebi Hospital of Traditional Chinese Medicine, Hebi 458000 Henan, China;
2. Hebi Medical Device Adverse Drug Reaction (Event) Monitoring Center, Hebi 458000 Henan, China;
3. The First Affiliated Hospital of Henan University of Traditional Chinese Medicine, Zhengzhou 450000 Henan, China]
【Abstract】 Objective:To analyze 420 cases of serious adverse drug reactions (ADR). Methods:420 cases of serious ADR reported in Hebi City from December 2018 to December 2021 were retrospectively analyzed. The patients’ gender, age, route of administration, outcome, ADR reporter, relevance evaluation, drug type and name were statistically analyzed. The top 6 drugs and clinical manifestations were reported. Results:Among the 420 cases of severe ADR, 260 cases were male, accounting for 61.90%, and 160 cases were female, accounting for 38.10%. The patients were main those with 60-79 years old, accounting for 42.62%. Oral and intravenous infusion accounted for the highest proportion of severe ADR, which were 47.62% and 42.62%, respectively. The most serious ADR reporters were pharmacists, accounting for 47.86%, followed by doctors, accounting for 38.10%. The outcome was mainly cured and improved, of which 68 cases were cured, accounting for 16.19%, and 320 cases were improved, accounting for 76.19%. The relevance evaluation was mainly possible. The types of drugs were mainly antipyretic analgesic anti-inflammatory drugs and antitumor drugs, followed by hematological drugs and anti-infective drugs. The top 6 drugs with serious ADR were Aspirin enteric-coated tablets, Warfarin tablets, Docetaxel injection, Cisplatin injection, and Paclitaxel (albumin-bound) and Clopidogrel Sulfate tablets. The main clinical manifestations were blood system damage and digestive system damage. Conclusions:The types and causes of serious ADR are different. Therefore, the clinical medication monitoring of antipyretic analgesics, antitumor drugs, hematological drugs and anti-infective drugs and the patient medication education should be strengthened.
【Keywords】 Adverse reactions; Monitoring report; Serious; Drugs; rational administration of drugs
药品不良反应(adverse drug reaction,ADR) 是指合格药品在正常用法用量下出现与用药目的无 关的有害反应 [1] 。ADR 监测是为了进一步了解药 品的不良反应,评估药品安全性,并对药品加强管 理,预防和减少不良反应的发生 [2]。据国家 ADR 监测年度报告数据显示,近十年我国严重 ADR 发生率持续增长,上报主体主动意识显著提高。本文 对 420 例严重 ADR 进行系统分析。
1 资料与方法
1.1 一般资料 回顾性分析 2018 年 12 月至 2021 年 12 月鹤壁市上报到国家药品不良反应监测中心 的 8367 例 ADR 的临床资料。根据《药品不良反应 报告和监测管理办法》中关于严重 ADR 的判断标 准 [1] ,因使用药品引起以下损害情形之一的反应: ( 1 )导致死亡;(2 )危及生命;(3)致癌、致畸、致出生缺陷;(4)导致显著的或永久的人体 伤残或器官功能损伤;(5)导致住院或住院时间 延长;( 6)导致其他重要医学事件,如不进行治 疗可能出现上述所列情况的。挑选符合以上不良反 应发生情况,且只发生一种不良反应类型,从中筛 选出 420 例严重 ADR 报告。
1.2 方法 ( 1)参照《中华人民共和国药典临床 用药须知》对药品名和药品分类进行标准化 [3] ,并 根据《药品不良反应术语使用指南》对 ADR 名称 进行标准化 [4]。(2)对发生严重 ADR 患者的年龄、 性别、给药途径、转归、关联性评价、ADR 报告者、 药品种类和名称、上报例数前 6 种药品及临床表现 进行系统整理。
2 结果
2.1 发生严重 ADR 患者性别和年龄分布 420 例 发生严重 ADR 患者中,男 260 例, 占 61.90%,女 160 例, 占 38.10%。以男性居多,以 60~79 岁年龄 段最多,占 42.62%。见表 1.
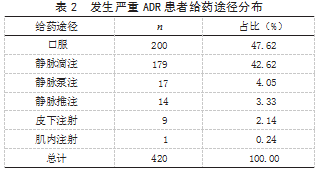
2.2 发生严重 ADR 患者给药途径分布 420 例发 生严重 ADR 患者包括 6 种给药途径,其中以口服 给药占比最高,为 47.62%,其次为静脉滴注,为 42.62%。见表 2.
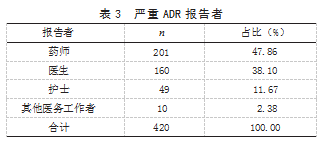
2.3 严重 ADR 报告者类型 严重 ADR 报告者最 多为药师,占 47.86%,其次为医生,占 38.10%。 见表 3.
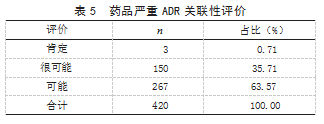
2.4 发生严重 ADR 患者转归情况 420 例发生严 重 ADR 患者的转归情况以痊愈和好转为主,其中痊愈 68 例, 占 16.19%,好转 320 例, 占 76.19%。 见表 4.2.5 药品严重 ADR 关联性评价 根据《药品不良 反应报告和监测手册》,结合时间相关性、ADR 的已知性、减量及停药后 ADR 的对应性、再激发 反应评价 ADR 与药品的关联性。见表 5.
2.6 发生严重 ADR 的药品种类及分布 发生严重 ADR 药品种类以解热镇痛抗炎药为主,其次是抗 肿瘤药、血液系统用药和抗感染药。其中,解热镇 痛抗炎药主要以水杨酸类为主,抗肿瘤药以植物来 源及其衍生物类和金属铂类为主,血液系统用药以 抗凝药为主,抗感染药以喹诺酮类为主。见表 6.
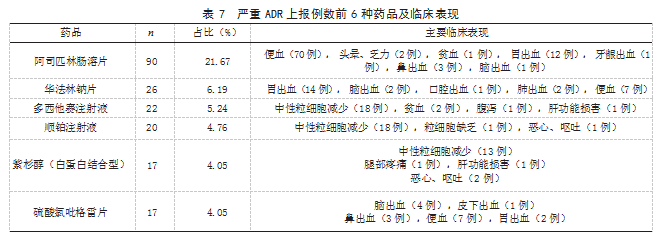
2.7 发生严重 ADR 上报例数前 6 种药品及临床表 现 发生严重 ADR 上报例数前 6 种的药品为阿司 匹林肠溶片、华法林片、多西他赛注射液、顺铂注 射液、紫杉醇(白蛋白结合型)、硫酸氯吡格雷片, 临床表现以血液系统和消化系统损害为主。见表 7.
3 讨论
3.1 严重 ADR 患者年龄、性别分析 420 例严重 ADR 男性与女性的比例为 1.625 ∶ 1.男性占比明 显高于女性,这一结果与文献报道一致 [5]。但与国 家 ADR 监测年度报告不符 [6] ,可能与本地男女人口比例有关。另外不同年龄段上报比例差异也较大, 60 岁以上上报比例较高,达 63.57%,老年人大多 数存在基础疾病,合并用药种类复杂 [7] ,且肝肾功 能减退,更易发生严重 ADR。对此建议,针对 60 岁以上老年患者,经肝肾代谢的药品应减量,采取 个体化给药方案,并进行适当的用药教育。
3.2 严重 ADR 上报者分析 严重 ADR 不良反应 上报者中,药师占比最大,为 47.86%。这与 2020 年国家 ADR 监测年度报告不符,分析原因为临床 药师可通过药师查房、药历书写、临床会诊等方式密切监测严重 ADR 发生情况,提高参与度 [8]。临 床医师应提高严重 ADR 的主动上报意识,作为直 接接触患者的一线人员,应发挥其在 ADR 监测工 作中的促进作用。
3.3 严重 ADR 给药途径分析 严重 ADR 的给药 途径主要以口服给药为主,占 47.62%,与 2020 年 国家 ADR 监测年度报告不符,主要原因可能与上 报者的认知偏差和口服药的使用率有关,老年慢性 病患者多选择口服方式,且联合用药导致的不良反应风险较高。对此,建议应根据患者的既往史、 过敏史、肝肾功能代谢率,严格制订联合用药方 案;其次,静脉滴注严重 ADR 发生率也偏高, 占 42.62%,主要与临床用药多以静脉滴注为主,药物 酸碱度、溶媒、滴速、药物配伍及操作不当都可能 引起严重 ADR[9]。对此建议,临床用药应根据联合 用药和患者机体代谢情况选择适宜的给药方式,但 仍应坚持“能口服不静滴”的原则 [10]。
3.4 发生严重 ADR 药品种类 发生严重 ADR 的 药品种类以解热镇痛抗炎药、血液系统药、抗肿瘤 药及抗感染药为主,其中解热镇痛抗炎药以阿司匹 林肠溶片为主,多为胃肠道反应,主要是因其在体 内分解成水杨酸,对胃肠道具有强烈的刺激性,且 还可抑制环氧化酶活性,影响胃黏膜生成及血小板 聚集, 导致胃溃疡及胃出血的发生 [11]。血液系统药 以华法林片为主,不良反应多与凝血酶原时间延长 有关,建议临床加强对凝血功能的监测,以减少华 法林的药物不良反应。抗凝治疗可增加患者出血风 险,因此应加强对患者出血风险的评估,且老年患 者应谨慎使用华法林 [12]。抗肿瘤药以金属铂类和 植物来源及其衍生物类为主,本研究主要为顺铂注 射液和多西他赛注射液,严重 ADR 以骨髓抑制居 多。对此建议,应在用药前做好预处理,及时监测 血液指标,及时处理骨髓抑制造成的白细胞和中性 粒细胞减少。抗感染药以喹诺酮类为主,盐酸莫西 沙星氯化钠注射液和左氧氟沙星氯化钠注射液最为 常见, 在临床应用中应重点对用药时间、用药频次、 滴注速度及溶媒选择等进行密切监测 [13-14]。
综上所述,发生严重 ADR 的种类、原因各异, 应加强解热镇痛抗炎药、抗肿瘤药、血液系统药和 抗感染药的临床用药监测及患者用药教育。
参考文献
[1] 中华人民共和国卫生部 . 药品不良反应报告和监测管理办 法 [EB/OL]. (2011-05-24)[2022-06-20]. https://www.nmpa. gov.cn/xxgk/fgwj/bmgzh/20110504162501325_7.html.
[2] 国 家药 品监督 管理局 . 国 家药 品不良反应监测年度 报 告(2018 年 )[EB/OL]. ( 2019-10-18 )[2022-06-20]. https://www.nmpa.gov.cn/directory/web/nmpa/xxgk/ggtg/ qtggtg/20191018151301540.html.
[3] 国家药典委员会 . 中华人民共和国药典临床用药须知:化学 药和生物制品卷(2010年版)[M]. 北京:中国医药科技出版社, 2011:1-29.
[4] 国家药品不良反应监测中心 . 药品不良反应术语使用指南 [M]. 北京:国家药品不良反应监测中心, 2016:9.
[5] 廖明, 韩秋, 李诗, 等 . 我院 263 例药品不良反应报告分析 [J]. 贵州医药, 2016.40(5): 522-523.
[6] 国家药品监督管理局 . 国家药品不良反应监测年度报告(2020 年)[EB/OL].( 2021-03-26)[2022-06-20]. https://www.nmpa. gov.cn/xxgk/fgwj/gzwj/gzwjyp/20210325170127199.html.
[7] 龙丽萍,周于禄,阳国平 . 309 例老年人严重药品不良反应报 告分析 [J]. 中国药物警戒, 2009.6( 1): 26-30.
[8] 赵雪丽,郑咏池,唐仕炜 . 临床药师药品不良反应监测参与度 研究及工作模式探讨 [J]. 中国药业, 2022.31(4): 15-17.
[9] 余知妍 .2060 例药品不良反应报告的总结分析 [J].海峡药学, 2022.34(6): 146-149.
[10] 余玖霞,戎立保 . 基于散点图、帕累托图及鱼骨图分析 354 例药品不良反应情况 [J]. 中医临床研究,2021.13(36): 142-146.
[11] 恽孝利 . 阿司匹林临床应用的不良反应分析 [J].世界最新医学 信息文摘(连续型电子期刊), 2019.19(27): 121-122.
[12] Lakshmi R ,James E ,Kirthivasan R.Study on Impact of Clinical Pharmacist’s Interventions in the Optimal Use of Oral Anticoagulants in Stroke Patients[J]. Indian J Pharm Sci,2013. 75( 1): 53-59.
[13] 马飞,冯亚楠,李科南 .1143 份严重药品不良反应报告回顾性分析 [J]. 临床合理用药杂志, 2022.15(21): 37-40.
[14] 程军平,沈夕坤,胡芳,等 . 某院 2013-2014 年药物不良反应报告分析 [J]. 安徽医药, 2015.19( 11): 2239-2241.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/66733.html