SCI论文(www.lunwensci.com):
摘要:胃食管反流性咳嗽是慢性咳嗽主要病因之一,目前研究表明胃食管反流性咳嗽可能是多种因素共同作用的结果,包括微吸入、食管-支气管反射、神经元功能障碍、免疫介导、精神心理因素、非胃型H+/K+-ATP酶、产酸菌等。
关键词:胃食管反流病;慢性咳嗽;发病机制
本文引用格式:郭宇佳,郑吉敏.胃食管反流性咳嗽发病机制的研究进展[J].世界最新医学信息文摘,2019,19(52):96-97.
Research Progress on Pathogenesis of Gastroesophageal Reflux CoughGUO Yu-jia1,ZHENG Ji-min2*
(1.North China University of Technology,Tangshan Hebei;2 Department of Gastroenterology,Hebei Provincial People’s Hospital,Shijiazhuang Hebei)
ABSTRACT:Gastroesophageal reflux cough is one of the main causes of chronic cough.Current studies have shown that gastroesophageal reflux cough may be the result of multiple factors,including microaspiration,esophageal-bronchial reflex,neuronal dysfunction,immune mediation,psychosocial factors,non-gastric H+/K+-ATPase,acid-producing bacteria and so on.
KEY WORDS:Gastroesophageal reflux disease;Chronic cough;Pathogenesis
0引言
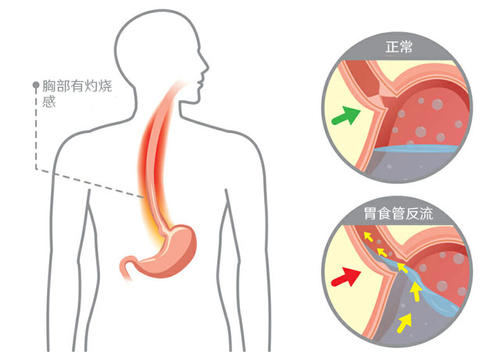
胃食管反流病(gastroesophageal reflux disease,GERD)是指由于胃十二指肠内容物反流入食管引起症状和并发症的疾病[1],咳嗽为常见的GERD食管外症状,而以咳嗽为主要表现的GERD称为胃食管反流性咳嗽。胃食管反流性咳嗽是继哮喘和鼻后滴流综合征之后慢性咳嗽的第3大常见的原因,三者总和占慢性咳嗽病因的90%[2]。
美国对出现食道外症状的GERD患者的一项研究发现,患者中50%有咳嗽症状,估计治疗费用是典型的GERD患者的4至5倍[3]。尽管抑酸剂被广泛大量的使用,仍有很大比例的慢性咳嗽患者被认为是由于GERD抑酸不充分所致的咳嗽无法改善。事实上,多项研究和Meta分析都未能证明抑酸剂治疗慢性咳嗽的疗效[4]。本文现对胃食管反流性咳嗽机制的研究进展进行阐述,旨在为GERD诊断及治疗提供依据。
目前胃食管反流性咳嗽的发病机制尚不明确,其中主要的学说包括微吸入、食管-支气管反射、神经元功能障碍、免疫介导、精神心理因素等。
1微吸入
类似于“吸入性肺炎”,微量的胃食管反流物反流至气管及肺泡,对肺组织造成损伤,进而引起咳嗽等保护性反射,从而导致反流性咳嗽,而相对于吸入性肺炎造成的急性肺损伤,微量胃食管反流物的吸入属于慢性持续性损伤。Herregods,TVK[5]等人的研究表明,较大量的反流和食道暴露于反流物较长时间似乎在诱导咳嗽中起重要作用,而反流物的酸度似乎不太相关。
这项研究结果同时有助于解释大多数慢性咳嗽患者不会从抑酸治疗中获益的观察结果。Herregods等的研究同样证明了这点[6]。
胃内容物在进入气道之前首先必须克服的保护性屏障包括:
①胃排空;②食管胃连接处(食管下括约肌、膈肌脚);③食管运动;④清除反射(吞咽、继发性蠕动);⑤食管上括约肌;⑥增加UES压力的反射(食管-UES收缩反射、咽-UES收缩反射、喉-UES收缩反射);⑦导致声带关闭的反射(食管声门反射、咽下反射);⑧喉内收反射等[7-8]。Phua,S.Y等人的实验显示,与健康人相比,表现为慢性咳嗽的GERD患者降低了喉内收肌反射的机械敏感性下降,这表明酸反流可能会损害咽喉部对气道的保护作用[9]。
反流性咳嗽多于日间直立位时发作,可能与仰卧位更容易引起UES收缩有关[10]。但是一项包括204例吞咽困难患者的研究[11]表明,抽吸的风险取决于咽喉敏感性与咽运动功能障碍之间的平衡。然而,受损的咽部运动功能在其发病过程中更为重要,喉内收肌反射敏感性仅在严重受损或缺失时增加了误吸的风险;所以这方面的理论仍有争议,需要更进一步的研究来加以证实。
另一个潜在的因素是吞咽和呼吸之间的精确协调。健康人在吸气结束时或呼气期间优先吞咽,因此吞咽通常随后呼气,这就降低了吸入咽喉或喉部任何残余物质的风险[12]。在声学监测实验中,胃食管反流性咳嗽患者的咳嗽模式通常由长周期组成,单个咳嗽事件并不常见[13],长时间连续的咳嗽影响吞咽及呼吸之间的精密协调;
此外咳嗽期间腹胸梯度增加,近端反流可能性增加,均可导致微吸入的风险增加。当患者合并慢性阻塞性肺病、哮喘等肺部疾病时,会出现吸气时吞咽,特别是在病情恶化时,进一步增加了吸入的风险[14]。这可能解释了包括亚临床脑血管病(与吸烟有关)或缺氧和/或高碳酸血症(慢性阻塞性肺病严重或在加重期)引起的神经功能障碍[15]。
验证微吸入最直观的方法就是进行下呼吸道标本中胃蛋白酶和胆汁酸的测定,如支气管肺泡灌洗液、气管吸出液、呼气冷凝液和痰,然而从下呼吸道采集的样本很可能受到唾液和咽分泌物的污染,即使是经支气管镜采集时也是如此,所以需要改进研究方法来做进一步的研究。
然而,24小时pH-阻抗监测和咳嗽声学同步监测显示,超过70%的患者表现出咳嗽与远端(而非近端)反流事件之间的时间相关性[16],而远端反流引发的咳嗽无法用微吸入学说解释。
2食管-支气管反射
该学说的理论基础为食管、胃和气道由共同的神经元支配。食管机械感受器AD传入纤维、伤害刺激感受器C纤维与气管快适应感受器(rapid adapting recept,RAR)均来自迷走神经的节状神经节和颈神经节,传入神经纤维都投射到脑干孤束核[17]。
进一步的研究显示,在慢性咳嗽和GERD患者中,与生理盐水对照组相比,将HCL注入食管远端可提高咳嗽反射对辣椒素的敏感性[18]。在无咳嗽的GERD患者和健康对照者的类似实验中,对咳嗽反射的敏感性无明显影响,提示食管-支气管反射可能在慢性咳嗽和GERD患者中有致敏作用。此外,研究还发现,阿托品可以消除这种支气管对食道酸灌注的反应,支持此为迷走神经介导的反射[19][20]。这可能可以用来解释食管高敏感。
GERD患者的抗反流屏障结构与功能异常(如:食管裂孔疝、腹内压增高、食管下括约肌(lower esophageal sphincter,LES)功能障碍、一过性LES松弛)、食管清除作用降低及食管黏膜屏障功能降低[21]均可使食管暴露于反流增加。而反流物如胃酸、胃蛋白酶、胆汁等对食管黏膜造成损伤,食管上皮细胞间隙增宽,黏膜完整性降低,从而增加了对食管-支气管反射感受器的刺激。
食管下端黏膜感受器受到的刺激后,通过食管-支气管反射兴奋咳嗽中枢引起咳嗽,同时引起相应的传出神经末梢通过胞吐作用释放P物质、神经激肽A、钙基因相关肽等神经肽[22][23],引起神经源性炎症或间接通过激活肥大细胞释放组胺、前列腺素E2、前列腺素D2和白三烯等炎性介质,刺激咳嗽感受器而引起咳嗽[24]。而且有研究表明,此反射敏感性一旦建立,即便生理性反流也可引发此反射。
3神经元功能障碍
药物干预为胃食管反流性咳嗽的机制研究提供了更多的思路。小剂量吗啡[25]和加巴喷丁[26]等改善神经元功能的治疗方法已经被证明能改善胃食管反流性咳嗽患者的特异性生活质量。最有趣的是,P2X3受体拮抗剂显示出最大的疗效,比安慰剂[27]降低了75%的日间声记录咳嗽频率。
鉴于质子泵抑制剂在类似患者中的有效性难以被证明,目前的证据支持神经元功能障碍是慢性咳嗽的根源的观点。尽管反流-咳嗽关联最容易解释为中枢神经元通路的功能障碍,但P2X3拮抗剂(af-219/MK-7264)很难穿透血脑屏障,这为外周神经元活动也发挥重要作用提供了令人信服的证据[28]。
4免疫介导
传统的观点认为食管黏膜的炎症反应是由于反流物的化学腐蚀所致,亦即炎症是由黏膜层向粘膜下层方向发展的,但形态学研究发现,反流物刺激食管黏膜后,淋巴细胞数量从上皮层向黏膜下层逐步增高,呈现炎症从黏膜下层向黏膜层发展的现象,因此,新的观点认为,免疫因素参与介导了反流所致食管黏膜损伤及食管功能的改变[29]。
与之相对应,胃食管反流性咳嗽是否也可由免疫反应所介导呢?Heffler,E的研究发现,胃食管反流性咳嗽患者较对照组呼气冷凝物的半胱氨酸-白三烯浓度更高[30],这表明免疫反应可能也介导了胃食管反流性咳嗽的发生。
5精神心理因素
有研究表明,精神心理因素可通过影响食管抗反流屏障、食管动力进而引发咳嗽。曾艳凌等人的研究显示胃食管反流性咳嗽患者存在焦虑抑郁状态,且焦虑抑郁状态与食管上括约肌压力呈负相关[31];王巍等人研究表明胃食管反流性咳嗽患者焦虑、抑郁发病率高,精神心理状态与食管动力之间存在相关性,随着焦虑、抑郁状态加重,食管下端LES静息压及食管运动功能降低[32]。所以,精神心理因素可能是胃食管反流性咳嗽的重要发病机制之一。
此外,还有非胃型H+/K+-ATP酶、产酸菌等学说,同时,咳嗽与反流可互为因果,咳嗽可使腹压增高而引起反流,反流又可通过以上机制进一步加重咳嗽,从而形成恶性循环。
6结论
目前的研究表明,咳嗽可能是多种因素共同作用的结果,包括微吸入、食管-气管反射、神经元功能障碍、免疫介导、精神心理因素、非胃型H+/K+-ATP酶、产酸菌等,仍需继续深入研究为反流性咳嗽的诊治提供指导。
参考文献
[1]中华医学会消化病学分会.2014年中国胃食管反流病专家共识意见[J].中华消化杂志,2014,34(10):649-661.
[2]Ribolsi M1,Savarino E,De Bortoli N.et.al.Reflux pattern and role of impedance-pH variables in predicting PPI response in patients with suspected GERD-related chronic cough[J].Aliment Pharmacol Ther,2014,40(8):966-73.
[3]Francis DO,Rymer JA,Slaughter JC et al.High economic burden of caring for patients with suspected extraesophageal reflux[J].Am J Gastroenterol,2013,108:905-11.
[4]Kahrilas PJ,Howden CW,Hughes N,et al.Response of chronic cough to acid-suppressive therapy in patients with gastroesophageal reflux disease[J].Chest,2013,143:605-612.
[5]Herregods,TVK,Pauwels,A,Jafari,J,Smout,AJPM,et al.Determinants of reflux-induced chronic cough[J].Gut,2017,12,66(12):2057-2062.
[6]Herregods T,Pauwels A,Jafari J,et al.Determinants of reflux-induced chronic cough[J].Gut,2017.
[7]Shaker,R.&Hogan,W.J.Reflex-mediated enhancement of airway protective mechanisms[J].Am.J.Med,2000,108(4):8-14.
[8]Houghton,LA,Lee,AS,Badri,H,Smith,JA.et al.Respiratory disease and the oesophagus:reflux,reflexes and microaspiration[J].Nat Rev Gastroenterol Hepatol,2016,13(8):445-60.
[9]
Phua,S.Y.,McGarvey,L.P.,Ngu,M.C.&Ing,A.J.Patients with gastro-oesophageal reflux disease and cough have impaired laryngopharyngeal mechanosensitivity[J].Thorax,2005,60:488-491.
[10]Babaei,A.et al.Response of the upper esophageal sphincter to esophageal distension is affected by posture,velocity,volume,and composition of the infusate[J].Gastroenterology,2012,142:734-743.
[11]Houghton,LA,Lee,AS,Badri,H,Smith,JA.et al.Respiratory disease and the oesophagus:reflux,reflexes and microaspiration[J].Nat Rev Gastroenterol Hepatol,2016,13(8):445-60.
[12]Bautista,T.G.,Sun,Q.J.&Pilowsky,P.M.The generation of pharyngeal phase of swallow and its coordination with breathing:interaction between the swallow and respiratory central pattern generators[J].Prog.Brain Res,2014,212:253-275.
[13]Houghton,LA;Smith,JA;Gastro-oesophageal reflux events:just another trigger in chronic cough?[J].Gut,2017,66(12):2047-2048.
[14]Shaker,R.et al.Coordination of deglutition and phases of respiration:effect of aging,tachypnea,bolus volume,and chronic obstructive pulmonary disease[J].Am.J.Physiol,1992,263,G750-G755.
[15]Houghton,LA,Lee,AS,Badri,H;Smith,JA.et al.Respiratory disease and the oesophagus:reflux,reflexes and microaspiration[J].Nat Rev Gastroenterol Hepatol,2016,13(8):445-60.
[16]Smith,J.A.et al.Acoustic cough-reflux associations in chronic cough:potential triggers and mechanisms[J].Gastroenterology,2010,139,754-762.
[17]弓三东,崔立红.胃食管反流性咳嗽发病机制的研究进展[J].世界华人消化杂志,2014,22(19):2665-2670.
[18]Smith,J.A.et al.Acoustic cough-reflux associations in chronic cough:potential triggers and mechanisms[J].Gastroenterology,2010,139:754-762.
[19]Herve,P.,Denjean,A.,Jian,R.,Simonneau,G.&Duroux,P.Intraesophageal perfusion of acid increases the bronchomotor response to methacholine and to isocapnic hyperventilation in asthmatic subjects[J].Am.Rev.Respir.Dis,1986,134:986-989.
[20]Andersen,L.I.,Schmidt,A.&Bundgaard,A.Pulmonary function and acid application in the esophagus[J].Chest,1986,90:358-363.
[21]葛均波,徐永健.内科学[M].人民卫生出版社,2015:357.
[22]Brooks SM.Irrit ant-indu ced ch ronic cough:irritant-induced TRPpathy[J].Lung,2008,186(1):88-93.
[23]Koll arik M,Ru F,Undem BJ.Acid-sen siti ve vagal sen sory pathw ay s and cough[J].Pulm Pharmacol T her,2007,20:402-411.
[24]Pauwels A,Blondeau K,Dupont LJ,Sifrim D.Mechanisms of increased gastroesophageal reflux in patients with cystic fibrosis[J].Am J Gastroenter ol,2012,107:1346-1353.
[25]Morice AH,Menon MS,Mulrennan SA,et al.Opiate therapy in chronic cough[J].Am J Respir Crit Care Med,2007,175:312-5.
[26]Ryan NM,Birring SS,Gibson PG.Gabapentin for refractory chronic cough:a randomised,double-blind,placebo-controlled trial[J].Lancet,2012,380:1583-9.
[27]Abdulqawi R,Dockry R,Holt K et al.P2X3 receptor antagonist(AF-219)in refractory chronic cough:a randomised,double-blind,placebo-controlled phase 2 study[J].Lancet,2015,385:1198-205.
[28]Houghton,LA;Smith,JA.Gastro-oesophageal reflux events:just another trigger in chronic cough?[J]Gut,2017,12,66(12):2047-2048.
[29]陈旻湖,周丽雅主编.胃食管反流病诊疗规范与进展[M].人民卫生出版社,2016:25.
[30]Heffler,E,Crimi,C,Brussino,L,Crimi,N,et al.Exhaled breath condensate pH and cysteinyl leukotriens in patients with chronic cough secondary to acid gastroesophageal reflux[J].J Breath Res,2016,11(1):016002.
[31]曾艳凌,林晗,黄胡萍,等.胃食管反流性咳嗽与焦虑、抑郁状态相关性分析[J].中外医学研究,2018(25):1674-6805.
[32]王巍,崔立红,王晓辉,等.胃食管反流性咳嗽患者精神心理因素与食管动力的相关性研究[J].解放军医药杂志,2016,28(08):28-30.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/11700.html