【摘要】目的:研究泰安地区耐万古霉素肠球菌患者的临床特征及其耐药情况。方法:收集自2019年1月—2022年12月于泰安市中医医院的住院感染患者标本,包括血液,尿液,腹水等的细菌培养,共335例。根据其药敏结果分为两组,其中万古霉素耐药肠球菌(vancomycin-resistant enterococcus,VRE)组37例,万古霉素敏感的肠球菌(vancomycin-sensitive enterococcus,VSE)组298例。根据病历,提取患者临床资料,包括性别、年龄、科室等。收集本科室的细菌鉴定及药敏结果。结果:与VSE组相比,VRE在尿液标本中最多,以屎肠球菌最多,重症医学科中检出最多。比较VRE组与VSE组的药敏结果,多项抗生素药敏结果呈临界阳性(P≥0.1)。结论:万古霉素耐药肠球菌多从尿液标本中分离,且屎肠球菌最多,在重症医学科中常见。VRE组与VSE组对不同抗菌药物的耐药率及敏感率差别不大。
【关键词】肠球菌,抗生素,万古霉素,耐药性
肠球菌(enterococcus)是人类和其他动物的非致病性肠道共生细菌,广泛地存在于自然界中[1]。随着近几十年来抗生素耐药性的激增,屎肠球菌和粪肠球菌已经成为医院分离出的最常见的革兰氏阳性致病菌之一[2]。这些医院分离的肠球菌含有固有的抗生素耐药性,而且可以快速获得额外的抗生素耐药性,使得肠球菌感染难以治疗,给医院造成了巨大的负担[3]。研究表明,肠球菌已经获得了共生菌株或环境菌株中通常不存在的定制基因库,并且可能使这些肠球菌在医院环境中持续存在[4]。自1986年首次分离出万古霉素耐药肠球菌(vancomycin-resistant enterococcus,VRE)以来,研究表明,肠球菌已经获得了共生菌株或环境菌株中不存在的基因库,可能使这些肠球菌在医院环境中持续存在[5]。部分VRE在患者体内从头产生,其中,人类共生厌氧胃肠道细菌可能是万古霉素抗性转座子的供体[6]。除了插入序列介导的菌株之间的转座之外,还有供体和受体染色体之间的跨同源区域重组[7]。本研究拟通过分析泰安市中医医院感染肠球菌的住院患者标本中VRE与万古霉素敏感的肠球菌(vancomycin-sensitive enterococcus,VSE)的患者临床特征及其他抗生素耐药情况,以期为下一步合理使用抗生素及控制医院内感染的传播提供理论依据。
1资料与方法
1.1一般资料
收集2019年1月—2022年12月于泰安市中医医院的住院感染患者标本,包括血液,尿液,腹水等的细菌培养,共335例。纳入标准:感染肠球菌的住院患者。排除标准:资料不完整。同一患者同一标本只选用第一株细菌作为研究对象,剔除重复,进行回顾性研究分析。根据其药敏结果分为两组,其中万古霉素耐药肠球菌(VRE)组37例,万古霉素敏感的肠球菌(VSE)组298例。查阅医院病案室资料,收集相应患者的临床基本资料,包括性别、年龄、送检科室等。其中,标本细菌培养共检出屎肠球菌181例,粪肠球菌149例,鹑鸡肠球菌2例,钻黄肠球菌3例。本研究经医院医学伦理委员会批准,患者及家属均知情同意并签署知情同意书。
1.2方法
细菌鉴定及药敏实验采用法国梅里埃VITEK 2 COMPACT全自动鉴定仪,实验所有抗菌药物来自梅里埃配套GP鉴定板卡,GP67药敏卡(生物梅里埃公司,国械注进20172401374 20测试/盒),万古霉素K-B法试剂条(温州市康泰生物科技有限公司,浙械注准20152400139)。采用K-B法复核万古霉素药敏结果,药敏试验结果判定依据美国国家和临床实验室标准化协会(Clinical and Laboratory Standards Institute,CLSI)2022判读标准。
1.3统计学处理
数据均采用SPSS 26.0软件进行统计学分析。计数资料均以例(%)表示,两组间比较采用Fisher精确概率法计算χ2值,3组及以上组间比较采用秩和检验计算Z值。采用stat16计算本实验所需样本量大于本实验目前收集到的样本量,所以,因样本量过小,可以调整水准,以P<0.1为差异有统计学意义。
2结果
2.1两组临床特征比较
VSE组年龄68(57,82)岁,VRE组年龄67(58,84)岁。两组性别、年龄和标本种类比较,差异无统计学意义(P>0.05);两组细菌种类比较,差异有统计学意义(P<0.1),两组送检科室比较,差异有统计学意义(χ2=46.783,P<0.001),见表1、表2。
2.2两组药敏结果比较
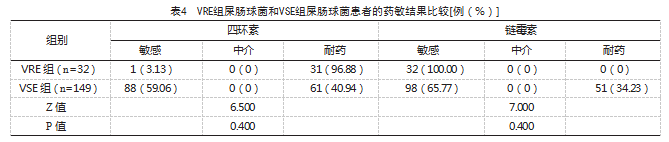
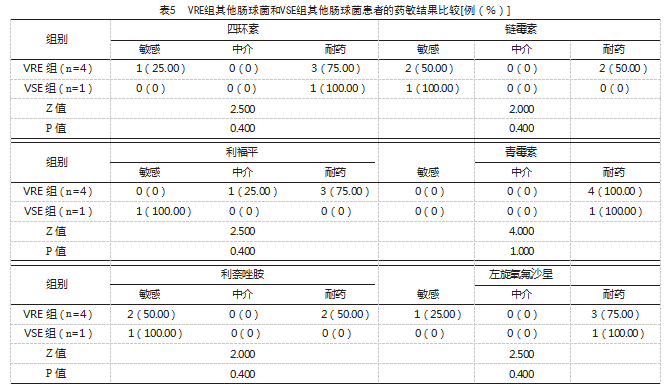
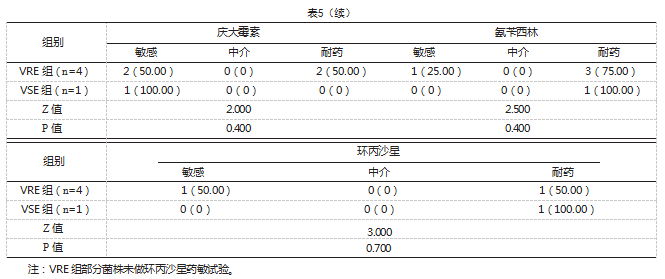
两组分别进行同类细菌药敏结果,多项抗生素药敏统计结果呈临界阳性,差异无统计学意义(P≥0.1),见表3、表4、表5。
3讨论
本研究共收集到335例肠球菌标本,其中万古霉素敏感VSE组298例,万古霉素耐药VRE组37例。VRE组和VSE组的在性别和年龄上无显著差异,因为肠球菌一般表现出低水平的毒力[8]。VRE组和VSE组的标本种类,细菌种类,送检科室分布不同。VRE在尿液标本中最多[9]。本次收集的标本中,屎肠球菌最多。肠球菌更易感染脆弱的患者群体,比如免疫抑制患者,因此在重症医学科中检出率最高[10]。
VRE组,含1例粪肠球菌,32例屎肠球菌,4例其他肠球菌。VSE组,含148例粪肠球菌,149例屎肠球菌,1例其他肠球菌。比较VRE组和VSE组药敏结果,多项抗生素药敏结果呈临界阳性,P≥0.1,因此证实VRE组与VSE组对不同抗菌药物的耐药率及敏感率差异不大。VRE的感染率从1%~55%,取决于环境和患者类别[11]。肠球菌具有极其灵活的基因组,使病原体能够快速适应不断变化的环境[12]。医疗机构和更广泛的社区中持续抗生素暴露的进化反应和各种选择性压力,使肠球菌的耐药性飞速发展[13]。
人类对于其抗生素抗性基因的传播和积累研究甚少[14]。但是,限于本研究收集的标本数量不足,导致部分分组的标本数量不够,以后应尽量采用多中心研究以便于收集更多的标本,进行平行比对结果。
参考文献
[1]HANCHI H,MOTTAWEA W,SEBEI K,et al.The Genus Enterococcus:between probiotic potential and safety concerns-an update[J].Front Microbiol,2018,3(9):1791.Chinese and Foreign Medical Research Vol.22,No.19 July,2024
[2]MILLER W R,MUNITA J M,ARIAS C A.Mechanisms of antibiotic resistance in enterococci[J].Expert Rev Anti Infect Ther,2014,12(10):1221-1236.
[3]JIA W,LI G,WANG W.Prevalence and antimicrobial resistance of Enterococcus species:a hospital-based study in China[J].Int J Environ Res Public Health,2014,11(3):3424-3442.
[4]AHMED M O,BAPTISTE K E.Vancomycin-Resistant Enterococci:a review of antimicrobial resistance mechanisms and perspectives of human and animal health[J].Microbial Drug Resistance,2018,24(5):590-606.
[5]O'DRISCOLL T,CRANK C W.Vancomycin-resistant enterococcal infections:epidemiology,clinical manifestations,and optimal management[J].Infect Drug Resist,2015,24(8):217-230.
[6]AXELRAD J E,LEBWOHL B,CUARESMA E,et al.Gut colonization with vancomycin-resistant Enterococcus and risk for subsequent enteric infection[J].Gut Pathog,2018,10(1):28.
[7]NZABARUSHIMANA E,TANG H.Insertion sequence elements-mediated structural variations in bacterial genomes[J].Mobile DNA,2018,9(1):29.
[8]MONTESERIN N,LARSON E.Temporal trends and risk factors for healthcare-associated vancomycin-resistant enterococci in adults[J].Journal of Hospital Infection,2016,94(3):236-241.
[9]SUN H L,LIU C,ZHANG J J,et al.Molecular characterization of vancomycin-resistant enterococci isolated from a hospital in Beijing,China[J].Journal of Micorobiology,Immunology and Infection,2019,52(3):433-442.
[10]MUTTERS NT,MERSCH-SUNDERMANN V,MUTTERS R,et al.Control of the spread of vancomycin-resistant enterococci in hospitals:epidemiology and clinical relevance[J].Dtsch Arztebl Int,2013,110(43):725-731.
[11]TONER L,PAPA N,ALIYU S H,et al.Vancomycin resistant enterococci in urine cultures:Antibiotic susceptibility trends over a decade at a tertiary hospital in the United Kingdom[J].Investig Clin Urol,2016,57(2):129-134.
[12]GILMORE M S,LEBRETON F,VAN SCHAIK W.Genomic transition of enterococci from gut commensals to leading causes of multidrug-resistant hospital infection in the antibiotic era[J].Current Opinion in Microbiology,2013,16(1):10-16.
[13]GILLINGS MICHAEL.Evolutionary consequences of antibiotic use for the resistome,mobilome and microbial pangenome[J].Frontiers in Microbiology,2013:4.
[14]CHANG D,ZHU Y,AN L,et al.A multi-omic analysis of an Enterococcus faecium mutant reveals specific genetic mutations and dramatic changes in mRNA and protein expression[J].BMC Microbiol,2013,13(1):304.
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/79671.html