摘要:为了有效保证化学检验技术在工业废水成分检测中的应用效果,同时提升检测质量及精度,以工业废水成分中的“氨氮(NH3-N)”以及其对应的检验技术“纳氏试剂检测法”为研究对象,详细阐述其检测原理以及检测实验过程和结果,以此为相关工作人员提供价值参考。
关键词:化学检验技术;工业废水;成分检测;氨氮检测;纳氏试剂
0引言
在工业污染领域中,工业废水是导致生态环境受到污染的重要因素之一,同时也是不易治理的污染类型之一,而在工业废水中,NH3-N又是其成分中的主要污染物质类型。站在人类的角度分析,一旦不慎服用了存在NH3-N物质的水体,水中的物质以及蛋白质便会相互作用产生亚硝胺,该物质对人类的身体健康有着极大威胁,有着较高致癌概率[1]。因此,工业废水成分检测无论是对环境保护还是人类健康维护均有着显著价值。
1基于纳氏试剂检测法的工业废水成分NH3-N检测原理
纳氏试剂检测工业废水成分中的NH3-N是借助红外可见光光度分析技术实现检测目标。其核心检测原理是把碘化汞和碘化钾碱性溶液与氨进行融合,使其相互作用发生化学反应,反应一段时间后就会逐渐产生淡黄色且呈胶状的混合物质,该物质的色度与NH3-N含量存在正比关系[2-3]。通常来讲,吸光度的波长均处于410~425 nm内,NH3-N含量的计算可通过公式(1)—式(3)予以实现。
HgCl2+2KI→HgI2↓(红色)+2KCl.(1)
HgI2+2KI(过量)→K2[HgI4](溶解).(2)
NH4-+2HgI4+4OH=[Hg2O(NH2)]I+7I-+3H2O.(3)
2实验部分
2.1实验材料
取某市某化工厂的工业废水作为实验样本,取样结束后根据相关标准规范对样本予以运输及保存,以供实验。
该检测实验应用到的试剂分别为:较高标准且物质的量浓度为c(NH)=0、参数是500 mL的无氨水;0.5 g/mL浓度的盐酸;0.5 g/mL浓度的硝酸钾;4 mol/L浓度的硼酸溶液;0.5 g/mL的酒石酸钾钠溶液;1.00 mg/mL质量浓度的铵标准贮备溶液;0.010 mg/mL质量浓度铵标准使用溶液;0.5 mg/mL质量浓度的溴百里酚蓝指示液。
该检测实验的核心试剂纳氏试剂不可以直接购买,应该依照实验的真实状况予以自主调配。
未经优化的纳氏试剂配置方法如下,试剂3为配置成果。
试剂1:将100 g碘化钾混合至100 mL无氨水内→添加10 g HgCl2结晶粉末直至出现朱红色沉淀·添加饱和HgCl2溶液直至出现朱红色沉淀·停止添加HgCl2。
试剂2:将20 g氢氧化钾混合至100 mL无氨水内→稀释→放置冷却至常温。
试剂3:试剂1+试剂2融合·静置→转移至容量瓶内并予以密塞保存→完成。
经过优化的纳氏试剂配置方法如下,最终配置成果为试剂8。
试剂4:将20 g氢氧化钾混合至150 mL无氨水内。试剂5:将30 g碘化钾混合至100 mL无氨水内。
试剂6:将20 g HgCl2预加热混合至50 mL无氨水内。
试剂7:试剂2+试剂3融合·搅拌至出现红色沉淀其不再溶解→放置冷却至常温。
试剂8:试剂1+试剂4融合·稀释→静置24 h→转移至容量瓶内并将其置于暗处低温保存→完成。
2.2实验过程
2.2.1实验样本预处理
通过未经优化的纳氏试剂比色技术对工业废水中的NH3-N予以检测阶段,针对色度以及浑浊度高且存在诸多影响物质的取样厂,相关人员普遍会通过蒸馏对实验样本予以预处理,详细过程如下。
预处理过程:取250 mL污水样本→装至容量瓶→添加溴百里酚蓝指示液→用氢氧化钠将混合液的pH值调至7→添加轻质氧化镁以及数粒玻璃珠→连接氮球以及冷凝管→下端插入硼酸溶液之中→加热蒸馏至馏出液达200 mL·定容至250 mL→完成。
该预处理过程能够有效处理掉样本中的各类无关物质,但其也会在一定程度上去除部分NH3-N,进而影响实验效果,基于此,可先于样本内添加0.5 mL的盐酸对其予以定性处理,接着便可实施预处理。
2.2.2绘制标准曲线
通过滴管采集适当数量铵标准使用溶液(0、0.5、1.0、3.0、5.0、7.0、10 mL),再将采集完成的溶液放置在14支特定试管内,保证每2支管内的溶液数量一致,接着全部添加10 mL的无氨水对溶液予以稀释处理,之后添加1.0 mL酒石酸钾钠溶液,借助玻璃棒将其有效混合,完成上述步骤之后,便于前一半相同数量溶液的管内添加2 mL未经优化的纳氏试剂,于后一半相同数量溶液的管内添加2 mL经过优化的纳氏试剂,同样借助玻璃棒予以有效混合,待静置15 min后,于波长400 nm位置,通过光程10 mm比色皿,同时借助紫外可见分光广度计并将无氨水视为依据,检测得出吸光度数值,接着便在此基础上校准曲线予以回归,并精准运算实验样本内的NH3-N含量。
2.2.3实验样本测定
样本测定:分别采集适量且已经通过预处理的工业废水实验样本(注意NH3-N含量需<0.1 mg/g),并将其置于50 mL的特定实验试管内,接着对其予以稀释处理,直到其达到标准刻线,再向其中混入1.0 mL的酒石酸钾纳溶液。分别采集适量且已经通过预处理的工业废水实验样本并将其置于50 mL的特定实验试管内,向其混入适量的氢氧化纳溶液,使其发挥出中和硼酸的作用,同样待其稀释到标准刻线,再混入0.5 mL纳氏试剂,通过玻璃棒高效混合,静置10 min,通过标准曲线步骤测定吸光度。
2.3实验结果分析与讨论
工业废水成分检测实验样本中NH3-N的浓度运算见公式(1)。
式中:ANH3-N为NH3-N的吸光度;Ay为实验样本的吸光度;Ad为对照实验的吸光度。
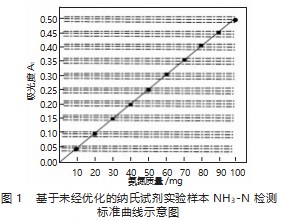
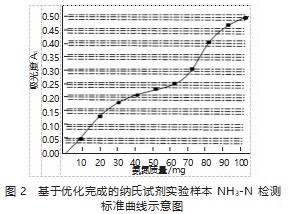
图1、图2所示内容是工业废水实验样本NH3-N检测标准曲线示意图,对图1和图2予以分析,便能准确得知实验样本内的NH3-N含量,之后依照式(2)计算其浓度。
ρ=m×1 000/V.(2)式中:ρ为NH3-N质量浓度,g/mL;m为基于校准曲线获得的实验样本内NH3-N含量,mg/g;V代表的是实验样本体积,cm3。
2.3.1精密度分析
经过实验结果研究,基于优化完成的纳氏试剂比色法对工业废水成分中的NH3-N予以检测,其RSD(相对标准偏差)的数值有明显的下降趋势,而基于未经优化的纳氏试剂比色法,其实验检测结果显示RSD的数值明显高于前者,具体数值是0.8%。且经过对比后得知,基于优化完成的纳氏试剂得出RSD数值相比于未经优化的降低了0.16%,如此便证明应用优化完成的纳氏试剂比色法其实验检测的精密度更佳。
2.3.2精准度分析
借助加标回收率检测明确优化前后的纳氏试剂比色法在工业废水成分检测中的精准度。加标回收率的运算公式见公式(3):
经研究结果表明,基于优化完成的纳氏试剂比色法对工业废水成分中的NH3-N予以检测,加标回收率的平均数值是98%,而基于未经优化的纳氏试剂比色法的加标回收率的平均数值是88%,经过比较,基于优化完成的纳氏试剂得出的加标回收率平均数值显著提升了10%,这代表优化完成的纳氏试剂比色法其实验检测的精准度更佳。
3结语
化工行业的发展不仅为人类社会带来了经济财富,同时也带来了严重的环境污染以及生命健康威胁。为有效治理环境污染和保护人民群众的身体健康,对工业生产排除的废水成分予以检测便至关重要,相关人员务必科学掌握相关化学检测技术,精准得出工业废水成分种类以及含量,以此为污水治理提供重要的参考依据,同时也为现代社会可持续发展奠定条件。
参考文献
[1]张浩.化学检验技术在工业废水成分检测中的有效应用方法[J].化工管理,2023(3):42-44.
[2]曹玲玲.化学检验技术在工业废水检测中的应用[J].清洗世界,2021,37(10):48-49.
[3]陈晓昀,蔡清,刘玉庆.化学检测技术在工业废水检测中的应用[J].化学工程与装备,2023(3):254-256.
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/ligonglunwen/77804.html