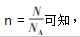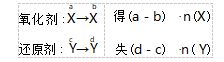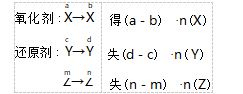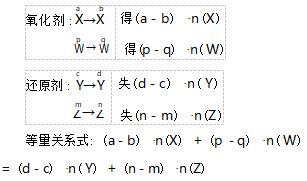SCI论文(www.lunwensci.com)
摘 要 : 在高中化学的学习过程中,复杂型计算往往涉及物质的量、离子反应和氧化还原反应的综合知识应用,其中氧化还原反应中得失电子守恒是建立等量关系式的关键之所在.
1.1 原理
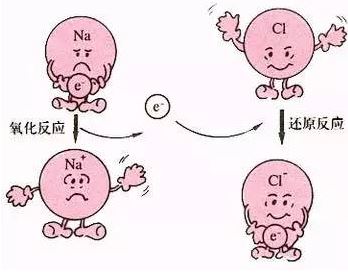
在同一个氧化还原反应中,氧化剂得电子数目等于还原剂失电子数目.再根据
在同一个氧化还原反应中,氧化剂得电子的物质的量等于 还原剂失电子的物质的量.观察到氧化剂中并不是 每种元素化合价都降低,还原剂中并不是每种元素 化合价都升高,所以从本质上来看,是氧化剂中某种 元素化合价降低,还原剂中某种元素化合价升高,因 此在数据处理过程中以原子得失电子建立等量关系式更能够避繁就简,直奔主题.
1.2 等量关系式
基础版 在同一个氧化还原反应中,氧化剂中X 元素化合价由 a 降低到 b ; 还原剂中 Y 元素化合价由 c 升高到 d.
等量关系式: (a-b) ·n(X) = (d-c) ·n( Y)
升级版 1 在同一个氧化还原反应中,氧化剂 中 X 元素化合价由 a 降低到 b ; 还原剂中 Y 元素化合价由 c 升高到 d,Z 元素化合价由 m 升高到 n.
等量关系式: (a-b) ·n(X) = ( d -c) ·n( Y)+ (n-m) ·n(Z)
升级版 2 在同一个氧化还原反应中,氧化剂 中 X 元素化合价由 a 降低到 b,W 元素化合价由 p降低到 q ; 还原剂中 Y 元素化合价由 c 升高到 d.
高级版 在同一个氧化还原反应中,氧化剂中 X 元素化合价由 a 降低到 b,W 元素化合价由p 降低 到 q ; 还原剂中 Y 元素化合价由 c 升高到 d,Z 元素化合价由 m 升高到 n.
2 实践
例 1 现有 24mL 浓度为 0.05mol / L 的 Na2 SO3 溶液恰好与 20mL 浓度为 0.02mol / L 的 K2 Cr2 O4 溶 液完 全 反 应.已 知 Na2 SO3 可 被 K2 Cr2 O4 氧 化 为 Na2 SO4 ,则 元 素 Cr 在 还原产物中的化合价为( ) .
A.+ 2 B.+ 3 2.+ 4 D.+ 5
解 设元素 Cr 在还原产物中的化合价为 b.氧化 还原反应中,氧化剂 K2 Cr2 O4 中 Cr 化合价由 + 6 降低到 b,还原剂 Na2 SO3 中 S 化合价由 +4 升高到 + 6.
上述通过实例分别阐述了基础版、升级版和高 级版等量关系式的用法.并且对于基础版部分做了 更多的介绍,用了更多的实例来阐述,力求读者真正 地理解得失电子守恒在计算中应用的逻辑,真正做到去粗存精,抓住解决问题的关键,快速解决问题!
参考文献 :
[1]王晶,郑长龙.普通高中教科书: 化学必修第一册 [M].北京:人民教育出版社,2019.
[2] 宋心琦.普通高中课程标准实验教科书: 化学必修 1[M].北京:人民教育出版社,2004.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/jiaoyulunwen/69711.html