SCI论文(www.lunwensci.com):
摘要:目的 探讨连花清瘟胶囊中苦杏仁苷的高效液相色谱测定方法,为连花清瘟胶囊的质量控制提供参考。方法 采用高效液相色谱法,色谱柱采用 Diamonsil-C18 色谱柱(4.6mm×250mm,5.0μm),流动相为:乙腈 :0.1% 磷酸溶液 =5:95,检测波长为 210nm, 柱温为 35 ℃,流速为 1.0mL/min。结果 ①连花清瘟胶囊中苦杏仁苷的线性关系方程为:A=0.0893×102C+0.0321×102,苦杏仁苷在 35.17~215.85μg/mL(r=0.9998)范围内线性关系良好;②苦杏仁苷的平均加样回收率为 99.76%,99.75%,99.83%;③检测限为
0.3517μg/mL。结论 高效液相色谱法用于对连花清瘟胶囊中有效成分苦杏仁苷含量进行测定,方法操作简单,对胶囊测定方法的重复性好,准确度高,为连花清瘟胶囊的质量控制提供了科学的参考数据。
关键词:高效液相色谱法;连花清瘟胶囊;苦杏仁苷;线性回归;检测限
陈蕾 , 曾晓红 . 高效液相色谱法测定连花清瘟胶囊中苦杏仁苷的含量 [J]. 世界最新医学信息文摘
Determination of Amygdalin in Lianhua Qingwen Capsules by HPLC
CHEN Lei1, ZENG Xiao-hong2
(1.Xinjiang Autonomous Region Medical Institution Drug Purchasing Center, Urumqi, Xinjiang, China; 2. The First People’s Hospital of Urumqi, Urumqi,
Xinjiang, China)
ABSTRACT:
Objective To explore the HPLC method for the determination of Amygdalin in Lianhua Qingwen capsules and provide reference for quality control of Lianhua Qingwen capsules. Methods HPLC was used. The chromatographic column was Diamonsil-C18 column (4.6mm×250mm, 5.0μm). The mobile phase was acetonitrile: 0.1% phosphoric acid solution=5:95. The detection wavelength was 210nm and the column temperature was 35°C, and flow rate was 1.0 mL/min. Results ① The linear equation of amygdalin in Lianhua Qingwen capsules was: A=0.0893×102C+0.0321×102. The linear relationship of amygdalin was good in therange of 35.17 to 215.85 μg/mL (r=0.9998); ② The average recovery of glycosides was 99.76%, 99.75% and 99.83%; ③ The detection limit was 0.3517 μg/mL. Conclusion HPLC method was used to determine the content of Amygdalin in Lianhua Qingwen capsules, the method is simple, the repeatability of the capsule measurement method is good, and the accuracy is high. It can provide S scientific reference data for the quality control for Lianhua Qingwen capsules.
KEY WORDS: High performance liquid chromatography; Lianhua Qingwen capsules; Amygdalin; Linear regression; Detection limit
0引言
连花清瘟胶囊的中药主要成分有金银花、连翘、炒苦杏仁、炙麻黄、石膏、板蓝根、鱼腥草、大黄、广藿香、绵马贯众、薄荷脑、红景天以及甘草 [1],功能主治为清瘟解毒、宣肺泄热,主要用于治疗流行性感冒属热毒袭肺证,症见发热或者高热,恶寒,肌肉酸痛,鼻塞流涕,咳嗽,头痛,咽干咽痛,舌偏红,苔黄或黄腻等 [2-3],连花清瘟胶囊在抗菌、镇痛、退热、抗炎、止咳、化痰和调节免疫功能的疗效明显,增强了机体的抗病康复能力[4]。连花清瘟胶囊中发挥降气止咳平喘作用的为炒苦杏仁, 同时还有润肠通便的效果,炒苦杏仁中苦杏仁苷是降气止咳平喘的药效成分 [5-6]。目前,以苦杏仁苷作为连花清瘟胶囊的质量控制的研究报道较少,在本次研究中,我们采用了炒苦杏仁中的有效成分苦杏仁苷成为作为高效液相色谱法的测定对象,旨在更好地为连花清瘟胶囊质量进行控制提供数据参考。
1仪器与试药
1.1试验仪器
美国 Waters717 高效液相色谱仪器(配备有恒温自动进样系统、Waters717 色谱工作站),电子分析天平(美国梅特勒公司生产,精密度为 0.0001g),德国 Sartorius 公司生产的电子天平(精密度为 0.1g),美国 Molecular 公司生产的 1260DADVL 型超纯水仪器,天津奥特赛恩斯公司生产的
SA7140BT 超声波清洗仪器(功率为 300W,频率为 40kHz)。
1.2试验试药
连花清瘟胶囊(石家庄以岭药业股份有限公司,生产批号分别为:A170512043、A170623023、A170715018)规格为0.35g/ 粒,苦杏仁苷对照品(中国药品生物制品鉴定所,批号为 110725-20161225,纯度为 93.60%)[7],乙腈、甲醇、水(北京迈瑞达科技有限公司)为色谱纯,水为超纯水,其他试验试剂均为分析纯。
2方法与结果
2.1色谱条件的选择
采用 Diamonsil-C18 色谱 柱(4.6mm×250mm,5.0m),流动相为:乙腈 :0.1% 磷酸溶液 =5:95,检测波长为 210nm,柱温为 35℃,流速为 1.0mL/min,进样量为 15L。理论塔板数按照苦杏仁苷峰计算不低于 25000。
2.2对照品溶液的制备
精密称取苦杏仁苷对照品 5.395mg,精密称定后置于10mL 容量瓶中,以 2.1 项下的流动相溶液作为定容溶液稀释至刻度后摇匀,得到 0.5395mg/mL 的对照品溶液,后置于 -20℃冰箱中备用。
2.3供试品溶液的制备
取同一批次的连花清瘟胶囊适量,将胶囊中的内容物取出后将药物研碎后,取约 2.0g 后进行精密称定,将药末放置于 100mL 具有瓶塞的锥形瓶中,50% 甲醇溶液 50mL 加入锥形瓶中后回流提取 60min,滤过,滤渣加入 50% 甲醇溶液40mL,洗涤 1 次,将 2 次的过滤液体及洗涤液体置于 200mL蒸发皿中,文火蒸干后,将残渣刮净后置于 20mL 刻度容量瓶中,流动相溶液定容至刻度,摇匀后静置即得,置于 -20℃冰箱中储存,备用。
2.4阴性对照品溶液的制备
以连花清瘟胶囊说明书中药材比例和制备工艺为主,将炒苦杏仁药材去除后制备不含炒苦杏仁药材的阴性胶囊样品,按照 2.3 项下供试品溶液的制备方法进行阴性对照品溶液的配制,后放置于 -20℃的冰箱中储存,备用。
2.5系统适应性试验
精密吸取 2.2、2.3 以及 2.4 项下的溶液各 15L,按照 2.1
项下的色谱条件对三种溶液进样测定并将色谱图进行记录, 可得到三种溶液的色谱图,见图 1。由色谱图可知,苦杏仁苷的色谱峰和其他相邻的色谱峰分离清晰,分离度 >1.5,阴性对照品溶液与对照品溶液相应的保留时间点并未有其他的色谱峰出现,即表明了连花清瘟胶囊中的其他中药材中的有效成分对苦杏仁苷的测定无任何影响。
2.6线性关系考察
精 密 吸 取 2.2 项 下 的 对 照 品 溶 液 0.8、1.0、1.4、1.6、1.8、2.0mL 分别置于 5mL 容量瓶中,加入流动相溶液定容至刻度后得不同质量浓度的对照品溶液,精密吸取上述对照组溶液各 15L,按照 2.1 项下的色谱条件分别进行测定,并记录峰面积。以质量浓度 C 作为横坐标,峰面积 A 作为纵坐标进行线性回归方程,苦杏仁苷的回归方程为:A=0.0893×102C+0.0321×102(r=0.9998),苦杏仁苷检测质量浓度线性范围为 35.17~215.85g/mL。
2.7检测限考察
取 2.2 项下储备溶液适量,等倍逐步稀释后分别吸取15L,按照 2.1 项下色谱条件连续进样测定,信噪比为 3:1 时得到苦杏仁苷的检测限 0.3517g/mL。
2.8精密度试验
精密吸取 2.2 项下的储备溶液 15L,2.1 项下的色谱条件进行测定,连续进样 6 次后得到不同的峰面积,苦杏仁苷峰面积的 RSD 值为 0.89%,表明 HPLC 仪器的精密度良好。
2.9稳定性试验
取 2.3 项下的供试品溶液,分别在 0、4、8、12、16、20、24、30、36h 按照 2.1 项下色谱条件测定,苦杏仁苷峰面积的 RSD 平均值为 0.71%,供试品溶液在室温条件下放置 36h 内稳定性较好。
2.10重复性试验
取同一批次的连花清瘟胶囊的内容物适量,共 6 份,按照2.3 项下制备方式配制溶液,以 2.1 项下的色谱条件测定,记录峰面积后对含量进行计算。结果表明苦杏仁苷的平均含量为 1.52mg/g,RSD 值为 0.85%,表明检测方法的重复性好。
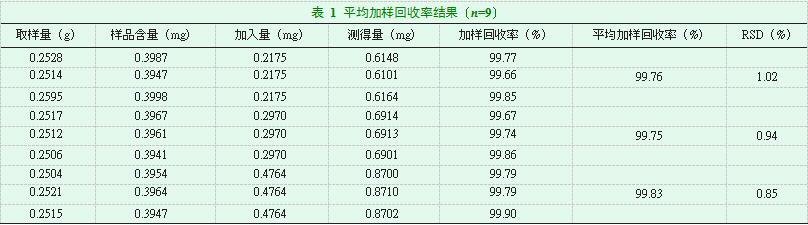
2.11加样回收率试验
取同批次生产批号相同的连花清瘟胶囊样品内容物 0.5g 共 9 份,精密称定后置于 100mL 具有瓶塞的锥形瓶中,分别加入 0.2175、0.2970、0.4764mg 苦杏仁苷对照品,按照 2.3 项下溶液的配方法进行溶液的制备,每个浓度平行制备 3 份后按照 2.1 项下的色谱条件进行测定,记录峰面积并计算加样回收率,见表 1。
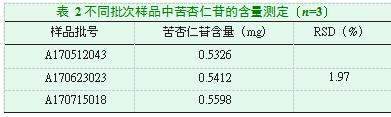
2.12样品含量的测定
取 A170512043、A170623023、A170715018 批号的 3 批样品内容物适量,按照 2.3 项下供试品溶液的制备方式进行配制后,以 2.1 项下的色谱条件进行测定,线性回归方程计算苦杏仁苷的含量,见表 2。
3小结
3.1检测波长的选择
将苦杏仁苷对照品按照 2.2 项下的操作配制成一定浓度的溶液,在 180~450nm 波长处进行紫外扫描,结果表明苦杏仁苷仅在波长为 210nm 处具有吸收峰,因此在试验过程中采用 210nm 作为苦杏仁苷的检测波长 [8]。
3.2流动相的选择
在试验开始之前分别尝试了多种不同比例的乙腈:0.1%磷酸溶液流动相,结果发现乙腈的比例越低则苦杏仁苷的分离效果越好,在进行了 5:95,10:90,20:80,30:70,45:55 几种分配比例后发现,在乙腈 :0.1% 磷酸溶液 =5:95 时,苦杏仁苷与其他组分之间的分离度较好 [9-10]。
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/364.html