SCI论文(www.lunwensci.com):
摘要:系统性EB病毒阳性的T细胞淋巴瘤是一种罕见的发生于儿童及年轻人的恶性肿瘤性疾病,在患者体内会出现活性细胞毒性表型的T细胞受EB病毒感染并克隆性增殖,该病在1978年Virelizier等首次报道,发病率很低,至今40余年来仅有不到50例报道。有明显的人种选择性,亚洲人较其他人种更易患该病。2016年EB病毒淋巴增殖性疾病国际分类会议修订将其命名为:儿童系统性EB病毒阳性的T细胞淋巴瘤,属于EB病毒相关的淋巴细胞增殖性疾病中的一类。本研究报道一例系统性EB病毒阳性的T细胞淋巴瘤通过化疗肿瘤得到缓解。
关键词:病毒阳性;淋巴细胞;病理
本文引用格式:刘颖,万叶明,陈艳,等.系统性EB病毒阳性的T细胞淋巴瘤1例并文献复习[J].世界最新医学信息文摘,2019,19(95):232-233.
1病例资料
14岁男患儿,因发现右侧颈部无痛性包块1+月入院。入院后查体发现右侧颈部可扪及蚕豆大小条形包块,质地较硬,不活动。脾脏肋下3 cm可及。血常规:白细胞3.9×109/L HB 128 g/L PLT 169×109/L.全腹CT提示脾脏稍增大,腹膜后淋巴结显示增多。故入院后行病理活检提示:淋巴结T细胞非霍奇金淋巴瘤,免疫组化提示肿瘤细胞:P-CK(-);TDT(-);MPO(-),CD20(-);CD79a(-);CD3(+);CD2(+)CD4(-)CD43(+);CD5(-);CD8(+);CD23(-),GranzymeB(+)TIA-1(+);Bcl-6(+);MUM1(+);CD56(-);CD68(-);CD10(-);Bcl-2(-);EMA(-);Alk(-);CD30(-);Ki-67(50%+);CD21示FDC网消失,S100(-);CD1a(-);原位杂交:EBER/ISH(+);基因重排检测,显示样本T细胞TCRB、TCRD、TCRG基因克隆重排。EB病毒DNA提示:8.3*103cop/mL。结合形态学、免疫组化、原位杂交及基因重排结果考虑儿童EBV阳性T细胞淋巴瘤。病初更昔洛韦抗病毒治疗,按非霍奇金淋巴瘤(T细胞性IV期)给与P方案(长春地辛、环磷酰胺、强的松)+A方案(长春地辛、环磷酰胺、泼尼松、阿糖胞苷、阿霉素)+BB(异环磷酰胺、依托泊苷、甲氨蝶呤、长春地辛、泼尼松)。同时给与腰穿及鞘内注射防治侵犯颅内,按上述方案治疗3个疗程,颈部包块较前增大、腹部CT+增强提示脾脏较前相比增大,腹部见较多淋巴结。考虑病情无好转、且有进展,回顾病理,考虑患儿为非霍奇金淋巴瘤(系统性EB病毒相关T淋巴型IV期),故调整为smile方案(异环磷酰胺+依托泊苷+甲氨蝶呤+地塞米松+培门冬酶)化疗5个疗程,化疗现结束6月,随访现无病生存。
2讨论
根据造血及淋巴组织肿瘤分类在2008版将儿童系统性EBV阳性T细胞淋巴组织增殖性疾病(CSEBV+-LPD)分为两种亚型[1],儿童系统性EBV阳性T细胞淋巴组织增殖性疾病和牛疸水疱病样淋巴瘤。两者都是与EBV感染相关的累及全身网状内皮系统的恶性疾病,但在病理、临床表现及预后方面有较大的不同。
本文讨论的儿童系统性EB病毒阳性T细胞淋巴瘤可在儿童及青年人发病,其特点是因急性EB病毒或慢性活动性EB病毒感染[3]时,T细胞变异为具有活性细胞毒性表型的T细胞,并出现大量的克隆增殖。一般来说病情较危急、预后差。
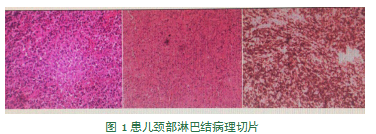
其病理表现为:①淋巴结T区增宽较为明显,可见斑驳区域;浸润的T细胞通常较小,大细胞散在其中。②部分病例可见惰性的淋巴样细胞,细胞中等或较大,细胞核不规则,异型性明显,核分裂象多;③免疫表型显示扩大的T区中常见CD3+的T细胞,典型的免疫表型未CD2+、CD3+、CD56-,TIA+、EBER+。本病例病理结果免疫表型在上诉中均有表现(见图一)。由急性EB病毒感染所致病人CD8+,慢性活动性EB病毒感染病人CD4+,临床上少见CD8及CD4均阳性的病人。本例病人CD8+,提示近期EB病毒感染。
病理是本病确诊的唯一金指标。但淋巴瘤病理表现多样,误诊率高。非霍奇金淋巴瘤亚型多且复杂,诊断较为困难。本型也较为少见。
本例病人病初考虑为T细胞性淋巴瘤(IV期),此病多发生于成年人,儿童及青少年较为少见。病理上见淋巴结结构破坏,T区高内皮小血管及分支状血管均增多,肿瘤细胞弥散性浸润。常有透明细胞及R-S样细胞,内皮细胞肥大的小血管增多。免疫组化多表达CD30,大多数发生在淋巴结的CD4+,CD8-.肿瘤细胞EBV-。故不会出现EBER/ISH(+)。该疾病还需与NK/T细胞淋巴瘤鉴别,该病多见于青年人及儿童,多发于鼻咽部[4]。该病已被证实与EB病毒感染息息相关[5],因NK细胞与T细胞的祖细胞相同,故两者在抗原表达和功能上有相似之处,NK/T细胞淋巴瘤的典型临床病理特征为:凝固样坏死和多种炎症细胞混合浸润的背景上散在或弥漫分布着肿瘤性淋巴样细胞,瘤细胞形成洋葱皮表现,导致血管损伤,伴组织大片坏死,细胞形态以中小细胞为主,但相互差异很大,瘤细胞核型不规则,有皱褶,核仁不明显,背景见大量的炎性细胞[2]。免疫组化可见NK细胞相关抗原表达,如CD2+、CD43+、CD94+、CD56+,T细胞抗原也偶尔可见一些表达如CD7、CD30,但都不表达胞膜CD3、CD4、CD5等。CD56+可与EB病毒阳性T细胞淋巴瘤相鉴别,但也曾有报道CD56+表达的系统性EB病毒阳性T细胞淋巴瘤,曾有学者提出此两者可能即为同一疾病,但2016版尚无相关说明。因两者病理表现及免疫组化的相似性,临床上需仔细反复研读。
该病的治疗目前也尚无明确的方案,主要是采用环孢素或联合细胞毒性化疗药,一般来说常用环磷酰胺+长春新碱(或长春地辛)+强的松的方案。但维持效果不长。本例在最初化疗中每个疗程均有使用上诉药物,但效果欠佳。后改为smile方案效果较为显著,其具体方法为:①甲氨蝶呤2 g/m,24 h持续静脉滴注,第1日②异环磷酰胺1.5 g/m。,第2-4日;③地塞米松40 mg/d,第2-4日;④依托泊苷100 mg/m,第2-4日;⑤培门冬酶,2000U,第8Et,分3-4部位肌肉注射;⑥四氢叶酸钙15 mg/次,每6 h静脉滴注,用MTX后第24小时开始应用,至甲氨蝶呤浓度小于0.1 mmol/L可停用;⑦美司钠300 mg/m2,与异环磷酰胺同步0 h、4 h、8 h,第2-4日;⑧粒细胞集落刺激因子5-10 ug/日,当白细胞小于2.0×109/L开始使用,至白细胞升至5.0×109/L停;⑨若有发热,使用抗生素。4周重复1次。每次化疗前复查血常规、肝肾功能、乳酸脱氢酶,使用培门冬酶前后复查凝血功能、肝肾功能、胰腺功能5个后病情方才有所好转。本案中其余化疗药在之前的方案中均使用过,但效果仍差,后改为smile方案后疗效较好,究其原因,笔者考虑与培门冬酶有关。
左旋门冬酰胺酶(L-AsP)可水解血清中的门冬酰胺,肿瘤细胞缺乏门冬酰胺合成酶,使DNA、RNA及蛋白质合成受抑,发挥抗肿瘤的作用,我们称为肿瘤的“饥饿疗法”。是儿童ALL的一线用药。部分肿瘤细胞如淋巴瘤、白血病细胞本身不能合成L一天冬酰胺(它是合成蛋白质必需的氨基酸),进而影响蛋白合成,最终使肿瘤细胞的增殖受到抑制。淋巴瘤细胞由于缺乏门冬酰胺合成酶,只能依赖外源性门冬酰胺。有学者使用该方案治疗难治复发的NK/T细胞淋巴瘤,取得了不错的疗效[6]。因该患儿经前3个疗程效果差,经家属同意后使用smile方案,一疗程淋巴结明显缩小。现随诊半年,病人无病生存。
Smile方案常用于治疗难治、复发型结外NK/T细胞淋巴瘤,由日本Yamaguchi[7]等同报道的SMILE方案是目前唯一针对NK/T细胞淋巴瘤提出的治疗方案,在I期I临床试验中,共3例Ⅳ期的初治患者和3例复发难治患者,其CR率为50%(3/6),CR+PR为67%(4/6),毒性主要为使用门冬酶后的骨髓抑制作用,毒性可以耐受。本例病人也出现了相关副反应,在层流床保护下未发生严重致命的感染。目前该方案尚无治疗系统性EB病毒阳性的T细胞淋巴瘤的经验,因本病普通化疗均预后差、易复发,故本案例使用smile方案治疗是一次全新的尝试。本病病人停化疗时间尚短,需继续随访。
综上所述,系统性EB病毒阳性的T细胞淋巴瘤是一类EB病毒感染后导致的淋巴细胞增殖性疾病,该病目前来说预后差,对化疗不敏感。如发现对常规化疗效果不好的也可以使用smile方案。
参考文献
[1]周小鸽.EB病毒淋巴增殖性疾病国际分类会议介绍及分类说明[A].中国抗癌协会淋巴瘤专业委员会(The Committee of Malignant Lymphoma,CACA).第十一届中国抗癌协会全国淋巴瘤学术大会教育论文集[C].中国抗癌协会淋巴瘤专业委员会(The Committee of Malignant Lymphoma,CACA):中国抗癌协会,2009:12.
[2]何德平,韩爱军,吴红樱,等.鼻NK/T细胞淋巴瘤68例临床病理分析[J].中国社区医师(医学专业),2013,15(7):247-248.
[3]段红梅,申昆玲.慢性活动性EB病毒感染的诊断标准和治疗[J].实用儿科临床杂志,2006(10):638-640.
[4]何德平,韩爱军,吴红樱,等.鼻NK/T细胞淋巴瘤68例临床病理分析[J].中国社区医师(医学专业),2013,15(07):247-248.
[5]曹玮,李栋梁,杨娅平,等.EB病毒感染对鼻型结外NK/T细胞淋巴瘤临床疗效及预后的影响[J].山东医药,2018(13):62-65.
[6]周颖,蔡清清,林旭滨,等.SMILE方案治疗复发难治NK/T细胞淋巴瘤的初步临床报告[J].白血病·淋巴瘤,2009,18(4):213-215.
[7]Yamaguchi M,Suzuki R,Kwong Y L,et al.Phase I study of de xamethasone,methotrexate,ifosfamide,L-asparaginase,and etoposide(SMILE)chemotherapy for advanced-stage,relapsed or refractory extranodal natural killer(NK)/T-cell lymphoma and leukemia.[J].Cancer Science,2008,99(5):1016-1020.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/24835.html