SCI论文(www.lunwensci.com):
摘要:目的对CS 5100全自动血凝分析仪检测系统检测低分子肝素抗-Ⅹa活性(LMWH抗-Ⅹa活性)进行性能验证。方法参照美国临床实验室标准化协会系列指南文件、卫生行业标准和试剂厂家的要求,对CS5100检测LMWH抗-Ⅹa活性的批内精密度、日间精密度、线性、准确度、携带污染率和参考范围进行性能验证。结果CS5100检测LMWH抗-Ⅹa活性检测的批内精密度、日间精密度、线性范围、准确度、携带污染率、参考范围验证结果均符合要求。结论CS5100检测LMWH抗-Ⅹa活性的主要性能指标均符合厂家及行业标准,可用于临床检测。
关键词:CS5100全自动血凝分析仪;低分子肝素;抗-Ⅹa活性;性能验证
本文引用格式:杨益锋,曾丹,石青峰,等.CS 5100全自动血凝分析仪检测低分子肝素抗-Ⅹa活性的性能验证[J].世界最新医学信息文摘,2019,19(57):201,254.
0引言
本研究根据美国临床实验室标准化协会系列指南文件、卫生行业标准和试剂厂家的要求,对使用Sysmex CS5100全自动血凝分析仪检测低分子肝素抗-Ⅹa活性进行性能验证。
1材料与方法
1.1一般材料
本院的住院患者和未使用低分子肝素的健康志愿者的枸橼酸钠(1:9)抗凝血。
1.2仪器与试剂
1.2.1仪器
Sysmex CS5100全自动血凝分析仪。
1.2.2试剂
配套的CS系列反应杯;OV BUFFER;CLEANⅠ;上海贞元抗-Ⅹa测定试剂盒;上海贞元配套低分子肝素校准品(LMWH Calibrator);质控品(LMWH Control Low,LMWH Control High)。
1.3试验方法
1.3.1精密度验证
(1)批内精密度:收集未使用低分子肝素的健康志愿者枸橼酸钠抗凝血浆作为基质血浆(低分子肝素抗-Ⅹa活性为0 IU/ml),同时收集使用低分子肝素患者的枸橼酸钠抗凝血浆作为高浓度样本(低分子肝素抗-Ⅹa活性接近1.6 IU/ml),将基质血浆和高浓度血浆样本按比例混合制备两个水平的混合血浆,分装并保存于-80℃冰箱。参照CLSI EP15-A2[1]文件和试剂厂家的要求,取2个水平的混合血浆各1份,按照常规方法连续测定20次LMWH抗-Ⅹa活性,计算均值()、标准差(s)和变异系数(CV)。按照厂家的要求,LMWH抗-X a活性检测的批内精密度(CV)应≤8%。(2)日间精密度:参照CLSI EP15-A2文件和试剂厂家的要求,每日取2个水平的混合血浆各一份,每天测定4次,每次间隔时间至少2h,连续测定5d,记录测定结果,计算均值()、标准差(s)和变异系数(CV)。按照厂家标准,LMWH抗-X a活性检测的批内精密度(CV)应≤10%。
1.3.2线性范围验证
参考卫生行业标准WS/T 408-2012[2]的线性验证方法。对于LMWH抗-Ⅹa活性检测,选取接近预期上限的高浓度样本和LMWH抗-Ⅹa活性为0 IU/mL的低浓度血浆样本,将低水平(L)和高水平(H)血浆标本分别按比例(4H、3H+1L、2H+2L、1H+3L和4L)配制5个水平浓度的样本,每个稀释样本检测2次,计算2次检测结果的均值()和每个浓度水平的理论值,将实测均值与理论值进行线性回归分析,得到回归方程Y=aX+b并计算相关系数(r),计算绝对偏差和相对偏差。评价标准:斜率应在0.95-1.05范围内。相关系数(r)和偏差按厂家的要求,在0-1.6 IU/mL线性范围内,相关系数(r)≥0.990,相对偏差≤±15%;在0.1-0.3 IU/mL线性范围内,绝对偏差≤±0.05IU/mL。
1.3.3准确度验证
参考卫生行业标准WS/T 406-2012[3],LMWH抗-Ⅹa活性检测使用厂家提供的LMWH Control Low和LMWH Control High定值质控品各检测1次。计算测定值与靶值的相对偏差。评价标准:相对偏差不超过±15%。
1.3.4携带污染率
参照CLSI H57-A[4]文件,将低值标本(N)置于1和3位置,高值标本(A)置于2位置,每个标本测3次,记录结果,分别标注为N1、N2、N3、A1、A2、A3、N4、N5、N6。携带污染率=[N4-(N1,N2,N3)]/(N1,N2,N3)。评价标准,携带污染率<10%。
1.3.5参考范围验证
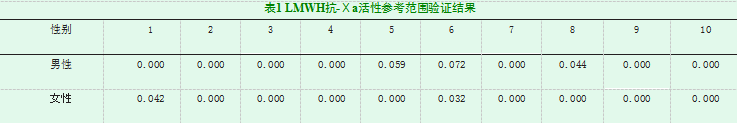
参照厂家说明书和CLSI C28-A2[5]文件,收集未使用低分子肝素的10名男性和10名女性健康志愿者的枸橼酸钠(1:9)抗凝血浆,测定LMWH抗-Ⅹa活性,并计算R值(结果落在参考区间内的样本数/总样本数)。根据厂家说明书要求,未使用低分子肝素的正常人LMWH抗-Ⅹa活性应<0.1 IU/ml。R值≥0.9为验证合格。
2结果
2.1精密度验证
LMWH抗-Ⅹa活性的低值范围的批内精密度为3.17%,批间精密度为6.61%;高值范围批内精密度为1.19%,批间精密度为2.29%。验证结果均符合要求。
2.2线性范围验证
LMWH抗-Ⅹa活性在0-1.549 IU/ml范围内的回归方程为Y=0.995X,r=0.999,相对偏差均≤15%,符合线性要求;在0.1-0.3 IU/ml范围内绝对偏差均≤±0.05 IU/ml,符合线性要求。
2.3准确度验证
LMWH抗-Ⅹa活性的测定值与靶值的低值偏倚为5.56%,高值偏倚为2.68%,相对偏差均≤±15%,符合要求。
2.4携带污染率
LMWH抗-Ⅹa活性的携带污染率为-1.51%,小于±10%,符合要求。
2.5参考范围验证
测定结果均<0.1 IU/mL,R值为1,验证通过,结果见表1。
3讨论
低分子肝素是目前临床上使用最为广泛的抗凝药物之一[6]。使用普通肝素时需监测活化部分凝血酶原时间(APTT),但研究表示在使用低分子肝素时,抗-Ⅹa活性比APTT监测抗凝效果更具优势[7]。由于不同厂家使用不同方法制备低分子肝素,所以其抗凝效果和推荐方案也会有差别[8],因此需要通过抗Xa活性测定来判断其抗凝效果。
目前国内很多实验室并未开展低分子肝素抗-Ⅹa活性测定,相关的性能验证也少见报道。本次研究通过对CS 5100全自动血凝分析仪检测低分子肝素抗-Ⅹa活性的主要指标进行性能验证,验证结果该检测系统的主要分析性能指标均能够满足检测要求,因此可以用于低分子肝素抗-Ⅹa活性测定。
参考文献
[1]Clinical and Laboratory Standards Institute.User Verification of Performance for Precision and Trueness[S].EP15-A2,CLSI,2004.
[2]卫生部临床检验标准专业委员会.临床化学设备线性评价指南:WS/T 408-2012[S].北京:中国标准出版社,2012.
[3]卫生部临床检验标准专业委员会.临床血液学检验常规项目分析质量要求:WS/T 406-2012[S].北京:中国标准出版社,2012.
[4]Clinical and Laboratory Standards Institute.Protocalfor the evaluation,validation and implementation ofcoagulometers[S].H57-A,CLSI,2008.
[5]Clinical and Laboratory Standards Institute.How todefine and determine reference intervals in the clinical laboratory[S].C28-A2,CLSI,2003.
[6]颜明明,刘利月,戴婷婷,等.低分子肝素类药物的临床应用[J].中国医药指南,2018,16(18):39-40.
[7]潘玉卿,陈正辉,冯曜宇,等.抗因子Ⅹa活性及APTT测定在深静脉血栓低分子肝素治疗患者中的应用评估[J].检验医学与临床,2017,14(10):1448-1450.
[8]汪玮,戴秋艳,吴莹,等.不同剂型低分子肝素对急性冠状动脉综合征患者抗Xa活性水平的影响[J].中华内科杂志,2007,46(08):667-668.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/16616.html