[摘要]目的探究白藜芦醇对博来霉素诱导小鼠肺间质纤维化的抗纤维化作用并阐明其潜在机制。方法2023年2—9月在齐齐哈尔医学院附属第三医院动物实验中心将购买的30只8周龄雄性C57BL/6小鼠采用随机数字表法分为3组,对照组,模型组和干预模型组,每组10只,对照组小鼠正常饲养,模型组和干预模型组均给予博来霉素制备肺纤维化动物模型,模型建立成功后干预模型组给予白藜芦醇灌胃,干预组和对照组给予等体积生理盐水灌胃,治疗4周后比较肺泡炎症、肺纤维化程度评分、肺组织中肿瘤坏死因子α(tu⁃mor necrosis factor-α,TNF-α)、白介素1β(interleukin 1β,IL-1β)、白介素6(interleukin 6,IL-6)、前列腺素(prostaglandin,PG)、还原型谷胱甘肽(glutathione,GSH)、羟脯氨酸(hydroxyproline,HYP)、丙二醛(malondialde⁃hyde,MDA)、超氧化物歧化酶(superoxide dismutase,SOD)水平,以及肺组织中转化生长因子β1(transforming growth factor beta 1,TGF-β1)、Samd3、细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK1/2)蛋白表达情况。结果模型干预组肺泡炎症和肺纤维化程度评分分别为(1.40±0.65)分、(1.90±0.57)分,均低于模型组的(3.20±0.74)分、(3.80±0.72)分,差异有统计学意义(t=5.779、6.543,P均<0.05)。与对照组比较,模型组TNF-α、IL-1β、IL-6、PG、HYP、MDA表达水平,以及TGF-β1、Samd3、ERK1/2蛋白表达均较高,差异有统计学意义(P均<0.05);SOD、GSH表达水平降低,差异有统计学意义(P均<0.05);与模型组比较,干预模型组TNF-α、IL-1β、IL-6、PG、HYP、MDA表达水平,以及TGF-β1、Samd3蛋白水平降低,差异有统计学意义(P均<0.05);SOD、GSH表达水平增高,差异有统计学意义(P均<0.05);但ERK1/2蛋白表达变化不明显,差异无统计学意义(P>0.05)。结论白藜芦醇通过调节TGF-β1/Smad3通路发挥抗肺纤维化作用。
[关键词]白藜芦醇,肺间质纤维化,TGF-β1,Smad3
肺纤维化是一种由多种病因引起的慢性进行性间质性肺病,最终会对肺组织结构造成不可逆转的损伤,严重影响呼吸功能,威胁人类健康。目前,临床上主要使用糖皮质激素和免疫抑制剂来治疗肺纤维化,但这些药物的疗效有限,且可能伴随严重不良反应[1]。中药在抗肺纤维化方面具有重要的研究价值和潜在的临床应用。近年来,越来越多的研究表明,中药能够改善或减轻肺纤维化,其中白藜芦醇是一种非黄酮类多酚化合物,作为植物在受到刺激时产生的一种抗毒素,已有研究证实其在肺纤维化、肾纤维化和心纤维化等多种器官纤维化疾病中具有一定的治疗效果[2-3]。然而,白藜芦醇在肺间质纤维化中的具体作用机制尚不明确。因此,研究白藜芦醇防治肺纤维化的药效及其分子机制对于肺间质纤维化的治疗具有重要的临床意义。本研究旨在研究白藜芦醇对肺间质纤维化小鼠炎症反应和氧化应激的影响,并探讨白藜芦醇对肺间质纤维化的保护机制。现报道如下。
1资料与方法
1.1实验动物和主要试剂
30只8周龄雄性C57BL/6小鼠(体质量20~25 g)购自哈尔滨医科大学实验动物学部,所有小鼠均饲养在无特定病原体级(specific pathogen free,SPF)环境中。利用随机数字表法将小鼠随机分为对照组、模型组和干预模型组,每组10只。本研究经齐齐哈尔医学院附属第三医院动物实验伦理委员会审核批准(AECC-2002-006)。
1.2方法
对照组小鼠正常饲养,向模型组小鼠气管插管注入5 mg/kg的注射用盐酸博来霉素(国药准字H20055883;规格:10 mg×10支)以建立肺纤维化模型,盐酸博来霉素处理后第二天开始,对照组和模型组每日给予10 mL/kg生理盐水灌胃,干预模型组每日给予等体积含100 mg/kg白藜芦醇(CAS号:501-36-0)的生理盐水灌胃,于第4周收集各组肺泡灌洗液后处死全部小鼠。
1.3观察指标
1.3.1 HE染色与Masson染色评估肺组织肺泡炎症及肺纤维化程度将肺组织标本依次进行固定、脱水、石蜡包埋处理,切片厚度约为3.5μm。切片脱蜡后,使用梯度醇和蒸馏水洗涤。部分切片经8 min苏木精染色,样品变蓝后用0.5%伊红染色2 min,随后快速脱水并透明化,最后用中性树胶封片。另一部分切片则置于丽春红酸性品红液中染色2 min,经弱酸浸染2 min后,5%磷钼酸分化2 min,再用苯胺蓝染色1.5 min,经过弱酸浸洗、乙醇脱水、二甲苯透明后进行封片处理。依据Szapiel SV等[4]的方法对肺组织的肺泡炎症和肺纤维化程度进行评分。评分根据炎症和纤维化的程度及范围分为4个等级,分别记为1~4分,分数越高表示纤维化程度越严重。
1.3.2试剂盒检测炎性因子和氧化应激相关指标采用酶联免疫吸附法检测各组小鼠肺泡灌洗液中炎症因子肿瘤坏死因子α(tumor necrosis fac⁃tor-α,TNF-α)、白介素1β(interleukin 1β,IL-1β)、白介素6(interleukin 6,IL-6)的表达水平,及小鼠肺组织中的前列腺素(prostaglandin,PG)和还原型谷胱甘肽(glutathione,GSH)。采用碱水解法检测小鼠肺组织中的羟脯氨酸(hydroxyproline,HYP),硫代巴比妥酸法测定肺组织中的丙二醛(malondialdehyde,MDA)含量,WST-1法检测各组小鼠肺组织中的超氧化物歧化酶(superoxide dis⁃mutase,SOD)水平。
1.3.3 Western blot检测TGF-β1/Samd3信号通路相关蛋白从模型组小鼠的肺组织中提取总蛋白,进行蛋白质印迹分析。将提取的蛋白质通过12%SDS聚丙烯酰胺凝胶电泳分离后,转移至聚偏二氟乙烯膜(PVDF膜)上。随后,膜在5%脱脂奶中封闭1.5 h。封闭后的PVDF膜分别与一抗[包括一氧化氮合酶(nitric oxide synthase,NOS)、环氧化酶(cyclo⁃oxygenase-2,COX-2)、转化生长因子β1(transform⁃ing growth factor beta 1,TGF-β1)、Samd3和细胞外调节蛋白激酶(extracellular regulated protein kinases,ERK1/2)]在4°C下孵育过夜。次日加入HRP标记的二抗,孵育1 h后,通过化学发光ECL系统检测免疫反应。
1.4统计方法
采用SPSS 26.0统计学软件对数据进行分析。经Shapiro-Wilk检验,符合正态分布的计量资料(包括肺泡炎症及肺纤维化评分、炎性因子和氧化应激相关指标,以及TGF-β1、Samd3、ERK1/2蛋白的相对表达量)以(±s)表示。两组间比较采用两独立样本t检验,使用单因素方差分析(ANOVA)进行多组间比较,采用LSD法进行多重比较。P<0.05为差异有统计学意义。
2结果
2.1各组肺泡炎症和肺纤维化程度评分比较
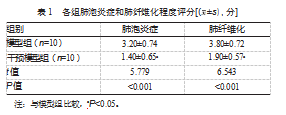
与模型组比较,干预模型组肺泡炎症和肺纤维化程度评分均下降,差异有统计学意义(P均<0.05)。见表1。
2.2各组肺组织中TNF-α、IL-1β、IL-6、PG、GSH、HYP、MDA、SOD表达水平比较
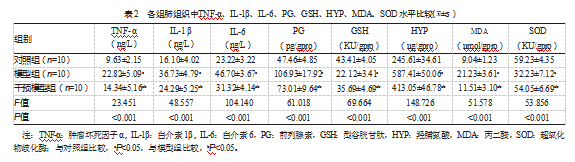
与对照组比较,模型组TNF-α、IL-1β、IL-6、PG、HYP、MDA表达水平均升高,SOD、GSH表达水平降低,差异有统计学意义(P均<0.05);与模型组比较,干预模型组TNF-α、IL-1β、IL-6、PG、HYP、MDA表达水平均降低,SOD、GSH表达水平增高,差异有统计学意义(P均<0.05)。见表2。
2.3各组肺组织中TGF-β1、Samd3、ERK1/2蛋白表达情况
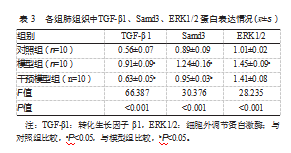
与对照组比较,模型组的肺组织中TGF-β1、Samd3、ERK1/2蛋白表达增高,差异有统计学意义(P均<0.05);与模型组比较,干预模型组肺组织中TGF-β1、Samd3蛋白表达下降,差异有统计学意义(P均<0.05);但是与模型组相比,干预模型组ERK1/2蛋白表达变化不显著,差异无统计学意义(P>0.05)。见表3。
3讨论
肺纤维化是一组慢性、进行性且通常致命的肺部疾病,可以是特发性的或继发于各种疾病,其特征是肺间质中细胞外基质和胶原蛋白的过量产生和大量沉积,导致组织修复异常和持续的肺损伤,最终导致肺纤维化,TGF-β在此过程中起着不可或缺的关键作用,因为它可以直接激活肌成纤维细胞并调节细胞外基质的产生[5]。因此,TGF-β信号传导的抑制作为肺纤维化的潜在且有用的治疗方法而受到关注。白藜芦醇具有抗炎、抗氧化和抗纤维化作用,特别是在肝纤维化和肾脏或心血管疾病的实验模型中,具有很高的安全性和耐受性[6]。如果白藜芦醇能够缓解肺纤维化,那么将提供更多的肺纤维化治疗替代方案。
本研究建模使用博来霉素导致的肺损伤是通过氧化还原反应引起肺损伤,正常的肺组织内存在完整的抗氧化体系,包括GSH、SOD,氧化还原反应可大量消耗GSH和SOD,引发脂质过氧化形成MDA,同时引起炎症细胞的聚集,有研究显示白藜芦醇可以通过增加GSH、SOD活性、降低肺组织中MDA含量、清除过多的氧自由基来抑制细胞外基质异常重塑引起的纤维化,这主要归因于白藜芦醇具有广泛的药理活性,如抗氧化、抗炎等[7]。此外,白藜芦醇还能清除自由基,激活抗氧化酶,维持细胞内谷胱甘肽的动态平衡,从而改善肺纤维化。HYP是胶原蛋白主要成分,HYP可直接反应肺纤维化的程度[8],其也可能通过调节肺组织中胶原蛋白的代谢并减少其在肺间质中的沉积,在肺纤维化的后期发挥有益作用。本研究结果显示,模型干预组肺泡炎症和肺纤维化程度评分分别为(1.40±0.65)分、(1.90±0.57)分,均显著低于模型组的(3.20±0.74)分、(3.80±0.72)分,且与模型组比较,模型干预组IL-6、TNF、MDA、IL-1β、HYP、PGE水平显著降低,GSH、SOD显著提高(P均<0.05),这说明白藜芦醇可减轻肺纤维化的程度,保护肺泡结构,维持肺泡正常呼吸功能,唐琼等[9]研究结果证实100 mg/kg白藜芦醇可显著降低模型组肺泡炎症和肺纤维化程度评分,并抑制肺组织中HYP、IL-18、TNF-α、IL-1β和TGF-β1的表达,这与本研究基本一致。
本研究结果显示与模型组比较,模型干预组TGF-β1、Samd3蛋白表达水平显著降低(P均<0.05),这说明白藜芦醇是通过TGF-β信号传导发挥抗肺纤维化的作用,TGF-β1是广泛参与器官纤维化发展细胞因子,它通过TGF-β/Smad和非Smad信号通路调节肌成纤维细胞的激活、迁移和ECM产生[10]。在TGF-β/Smad途径中,活化的TGF-βRI使得Smad2/3的磷酸化,然后与Smad4整合形成Smad2/3-4复合物,复合物易位到细胞核中,充当转录因子,导致纤维化转录物上调,在非Smad途径中,TGF-β还可以直接激活包括ERK在内的信号通路直接或间接调节纤维化[11-12]。本研究未显示出ERK1/2蛋白显著变化,故推测白藜芦醇是通过TGF-β/Smad3信号通路发挥抗纤维化作用。
综上所述,白藜芦醇对小鼠的肺纤维化具有保护作用,其可能是通过调节TGF-β/Smad3通路发挥抗肺纤维化作用。
[参考文献]
[1]周世琴,骆亚莉,周雯,等.肺纤维化的相关分子机制和治疗现状[J].中国临床药理学与治疗学,2022,27(10):1133-1147.
[2]梁耀丹,井洁,张泰程,等.白藜芦醇通过巨噬细胞源性外泌体调节肝星状细胞活化对肝纤维化的影响[J].广西医科大学学报,2023,40(12):1949-1955.
[3]赵雅欣,范奕好,程阳,等.白藜芦醇通过调控NLRP3/caspase-1信号通路抑制H2O2诱导的心肌纤维化[J].重庆医学,2021,50(21):3612-3616.
[4]Szapiel SV,Elson NA,Fulmer JD,et al.Bleomycin-induced interstitial pulmonary disease in the nude,athymic mouse[J].Am Rev Respir Dis,1979,120(4):893-899.
[5]胡晓玲,陈斯宁,陆珏.中医药靶向TGF-β1/Smads信号通路防治特发性肺纤维化研究进展[J].山西中医,2023,39(2):65-67.
[6]王真,陈立伟.白藜芦醇抗肿瘤药理作用机制研究进展[J].药物评价研究,2023.46(2):445-451.
[7]梁瑾.白藜芦醇对肾脏纤维化的保护作用及相关机制研究[D].苏州:苏州大学,2015.
[8]姜博涵,张宁,郭亚丽,等,补肺活血胶囊对肺纤维化模型小鼠的治疗作用及对PI3K/Akt信号通路的影响[J].现代药物与临床,2023,38(7):1590-1596.
[9]唐琼,厉铭,邢晨,等.白藜芦醇抑制JAK2/STAT3信号通路对矽肺大鼠纤维化的干预[J].中国工业医学杂志2022,35(6):483-488.
[10]王雪纯,江建冰.基于TGF-β1信号通路的抗肾脏纤维化药物研究现状J].实用药物与临床,2023,26(2):158-166.
[11]杨珣,邵松军,崔妙雅,等.抑制TGF-β1/Smads通路中Smad7泛素化降解改善小鼠肺纤维化的作用机制[J].山东医药,2022,62(17):47-51.
[12]刘卫东,高歌,刘函晔,等FTY-720通过TGF-P1/P38MAPK/NF-KB信号通路对小鼠肺纤维化模型的影响[J].中国药理学通报,2020,36(2):250-256.
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/81942.html