SCI论文(www.lunwensci.com)
摘要:目的:观察贝伐珠单抗联合伊立替康+亚叶酸钙+氟尿嘧啶(FOLFIRI)化疗方案治疗晚期转移性结直肠癌(mCRC)患者的效果。方法:选取2018年1月至2019年1月该院收治的92例晚期mCRC患者进行前瞻性研究,按照随机数字表法将其分为对照组和观察组各46例。对照组予以FOLFIRI化疗方案治疗,观察组在对照组基础上联合贝伐珠单抗治疗,比较两组疾病控制率、治疗前后血清肿瘤标志物[癌胚抗原(CEA)、糖类抗原19-9(CA19-9)、表皮生长因子受体(EGFR)、胰岛素样生长因子-1(IGF-1)]水平、治疗期间不良反应发生率和生存期[无疾病进展生存期(PFS)、总生存期(OS)]。结果:观察组疾病控制率为82.61%(38/46),高于对照组的60.87%(28/46),差异有统计学意义(P<0.05),治疗后,两组血清CEA、CA19-9、EGFR、IGF-1等血清肿瘤标志物水平均低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05),两组骨髓抑制、肝功异常、恶心呕吐、神经毒性和皮肤毒性等不良反应发生率比较,差异均无统计学意义(P>0.05),观察组PFS、OS均长于对照组,差异有统计学意义(P<0.05)。结论:贝伐珠单抗联合FOLFIRI化疗方案治疗晚期mCRC患者可提高疾病控制率,降低血清肿瘤标志物水平,延长生存期,效果优于单纯FOLFIRI化疗方案治疗。
关键词:转移性结直肠癌,贝伐单抗,FOLFIRI方案,肿瘤标志物,疾病控制率,不良反应,生存期
Effects of Bevacizumab combined with FOLFIRI chemotherapy regimen on patients with advanced metastatic colorectal cancer
WANG Guiying
(1st Department of Oncology of Jiamusi City Cancer Hospital,Jiamusi 154007 Heilongjiang,China)
Abstract:Objective:To observe effects of Bevacizumab combined with Irinotecan+Calcium folinate+Fluorouracil(FOLFIRI)chemotherapy regimen in treatment of patients with advanced metastatic colorectal cancer(mCRC).Methods:A prospective study was conducted on 92 patients with advanced mCRC admitted to the hospital from January 2018 to January 2019.They were divided into control group and observation group according to the random number table method,46 cases in each.The control group was treated with FOLFIRI chemotherapy regimen,while the observation group was treated with Bevacizumab on the basis of that of the control group.The disease control rate,the serum tumor marker levels[carcinoembryonic antigen(CEA),carbohydrate antigen 19-9(CA19-9),epidermal growth factor receptor(EGFR),insulin-like growth factor-1(IGF-1)]before and after the treatment,the incidence of adverse reactions during the treatment,and the survival time[progression-free survival(PFS),overall survival(OS)]were compared between the two groups.Results:The disease control rate of the observation group was 82.61%(38/46),which was higher than 60.87%(28/46)of the control group,and the difference was statistically significant(P<0.05).After the treatment,the levels of serum tumor markers such as CEA,CA19-9,EGFR and IGF-1 in the two groups were lower than those before the treatment,those in the observation group were lower than those in the control group,and the differences were statistically significant(P<0.05).There was no significant difference in the incidence of adverse reactions such as bone marrow suppression,abnormal liver function,nausea and vomiting,neurotoxicity and skin toxicity between the two groups(P>0.05).The PFS and OS of the observation group were longer than those of the control group,and the differences were statistically significant(P<0.05).Conclusions:Bevacizumab combined with FOLFIRI chemotherapy in the treatment of the advanced mCRC patients can improve the disease control rate,reduce the serum tumor marker levels,and prolong the survival time.Moreover,it is superior to single FOLFIRI chemotherapy regimen.
Keywords:Metastatic colorectal cancer;Bevacizumab;FOLFIRI regimen;Tumor marker;Disease control rate;Adverse reaction;Survival time
结直肠癌(CRC)是常见的消化系统恶性肿瘤,起病隐匿,早期无明显特异性,多数患者在确诊时已为中晚期,预后差[1-2]。晚期转移性结直肠癌(mCRC)患者通常已失去手术根治机会,临床主要采用化疗治疗,伊立替康+亚叶酸钙+氟尿嘧啶(FOLFIRI)化疗方案是晚期mCRC患者的一线化疗方案,抗肿瘤作用显著[3-4]。贝伐珠单抗是一种抗血管生成的靶向药物,可通过抑制血管内皮生长因子(VEGF)与其受体结合,抑制肿瘤新生血管形成,从而抑制肿瘤的生长、转移[5-6]。本文观察贝伐珠单抗联合FOLFIRI化疗方案治疗晚期mCRC患者的效果。
1资料与方法
1.1一般资料选取2018年1月至2019年1月本院收治的92例晚期mCRC患者进行前瞻性研究。纳入标准:经肠镜及病理活检确诊,符合《中国结直肠癌诊疗规范(2017年版)》中晚期mCRC的诊断标准[7];转移灶不能手术切除,且远处转移局限于单个器官或部位;体力状况美国东部肿瘤协作组(ECOG)评分0~2分;预计生存期>3个月。排除标准:合并肠梗阻、肠炎等其他肠道疾病;合并活动性出血性疾病、其他恶性肿瘤。患者及家属了解本研究内容并自愿签署知情同意书,且研究经本院医学伦理委员会审批通过。按照随机数字表法分为对照组和观察组各46例。对照组男25例,女21例;年龄45~79岁,平均(60.22±4.15)岁;临床分期:Ⅲ期24例,Ⅳ期22例;原发灶部位:结肠31例,直肠15例;转移部位:肝26例,肺16例,其他4例。观察组男26例,女20例;年龄44~79岁,平均(60.61±4.37)岁;临床分期:Ⅲ期25例,Ⅳ期21例;原发灶部位:结肠32例,直肠14例;转移部位:肝25例,肺16例,其他5例。两组一般资料比较,差异无统计学意义(P>0.05),有可比性。
1.2方法对照组予以FOLFIRI化疗方案治疗。第1天给予盐酸伊立替康注射液(上海创诺制药有限公司,国药准字H20153067,5 mL∶0.1 g)静脉滴注,180 mg/m2,1.5 h内滴完;第1~2天给予亚叶酸钙注射液(江苏恒瑞医药股份有限公司,国药准字H20020177,5 mL∶50 mg)静脉滴注,180 mg/m2,1 h滴完;第1天给予注射用氟尿嘧啶(海南卓泰制药有限公司,国药准字H20051626,0.25 g),静脉滴注22 h,600 mg/m。每2周为2 1个周期,共治疗3个周期。
观察组在对照组基础上联合贝伐珠单抗注射液(RocheDiagnostisGmbH,注册证号S20170035,100 mg)治疗,5 mg/kg,静脉滴注,每2周为1个周期,给药1次,共治疗3个周期。
1.3观察指标(1)比较两组疾病控制率。完全缓解(CR):靶病灶消失且维持4周;部分缓解(PR):靶病灶最大径之和减小≥30%且维持4周;病情稳定(SD):靶病灶最大径之和减小<30%或增大<20%;病情进展(PD):靶病灶最大径之和增大≥20%或出现新病灶。疾病控制率=(CR+PR+SD)例数/总例数×100%。(2)比较两组治疗前后血清肿瘤标志物水平。于治疗前、治疗3个周期后采集患者3 mL外周静脉血,离心半径8 cm,3000 r/min离心10 min,取血清,以化学发光免疫法测定癌胚抗原(CEA)、糖类抗原19-9(CA19-9)水平,以酶联免疫吸附法测定表皮生长因子受体(EGFR)、胰岛素样生长因子-1(IGF-1)水平。(3)比较两组治疗期间不良反应发生率。(4)比较两组生存期,包括无疾病进展生存期(PFS,接受治疗开始至PD或死亡的时间)和总生存期(OS,从入组至死亡的时间)。
1.4统计学方法应用SPSS 25.0软件进行统计学分析,计量资料以(±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,以P<0.05为差异有统计学意义。
2结果
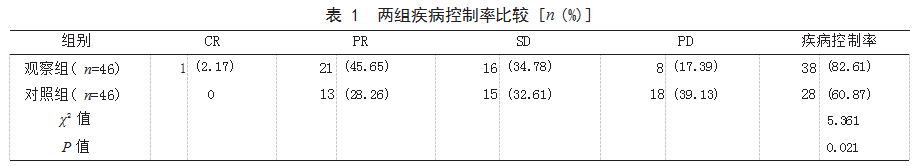
2.1两组疾病控制率比较观察组疾病控制率为82.61%(38/46),高于对照组的60.87%(28/46),差异有统计学意义(P<0.05)。见表1。
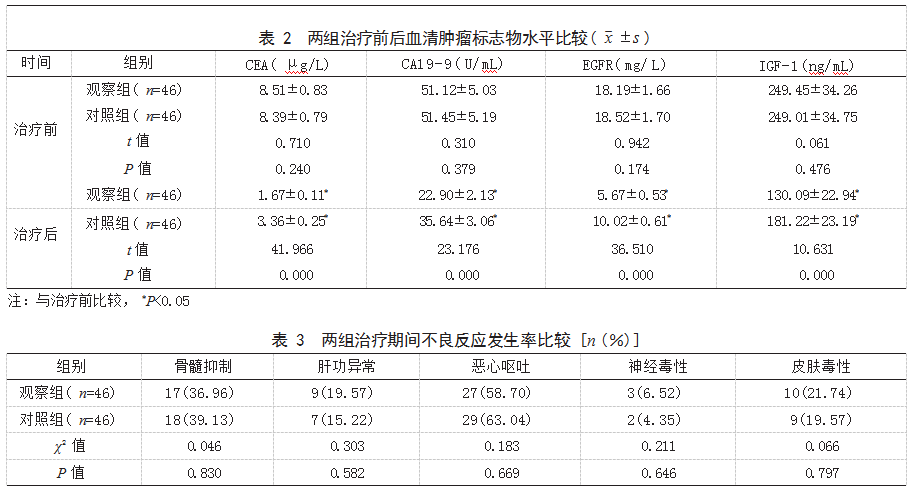
2.2两组治疗前后血清肿瘤标志物水平比较治疗前,两组血清CEA、CA19-9、EGFR、IGF-1水平比较,差异均无统计学意义(P>0.05);治疗后,两组血清CEA、CA19-9、EGFR、IGF-1水平均低于治疗前,且观察组低于对照组,差异有统计学意义(P<0.05)。见表2。
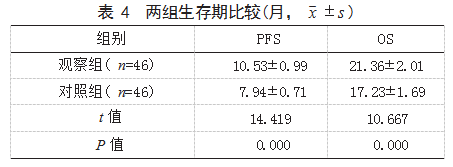
2.3两组治疗期间不良反应发生率比较两组骨髓抑制、肝功异常、恶心呕吐、神经毒性和皮肤毒性等不良反应发生率比较,差异均无统计学意义(P>0.05)。见表3。
2.4两组生存期比较观察组PFS、OS均长于对照组,差异有统计学意义(P<0.05)。见表4。
3讨论
FOLFIRI化疗方案是治疗晚期mCRC的标准方案[8],其中伊立替康为半合成水溶性喜树碱类衍生物,可通过诱导单链DNA断裂,抑制DNA复制和细胞分裂,从而抑制肿瘤细胞的生长、增殖,发挥抗肿瘤作用;亚叶酸钙可增强氟尿嘧啶对脱氧胸腺嘧啶核苷合成酶的抑制作用,从而增强抗肿瘤作用;氟尿嘧啶属于尿嘧啶抗代谢药,经机体吸收后变成氟尿嘧啶脱氧核苷酸,干扰DNA合成,抑制肿瘤细胞的生长、增殖[9-10]。
贝伐珠单抗是一种抗VEGF单克隆抗体,对VEGF受体亲和度较高,可抑制肿瘤新生血管生成,阻断肿瘤的生长、转移,控制疾病进展[11-12]。CEA是表达于某些癌细胞表面的糖蛋白,在肿瘤发生发展中发挥重要作用,体外研究显示其能够增强肿瘤细胞的抗凋亡能力,具有促进肿瘤血管生成和肿瘤转移的作用[13]。CA19-9是一种肿瘤相关抗原,在CRC中广泛表达[14]。EGFR为多种细胞因子的受体,通过激活多种细胞信号通路参与细胞的增殖、迁移、分化过程,参与CRC的发生发展[15]。IGF-1是一种细胞增殖调控因子,参与细胞的增殖、分化过程,有较强的抗凋亡作用,其水平升高与肿瘤增殖密切相关[16]。本研究结果显示,治疗后,观察组疾病控制率高于对照组,血清CEA、CA19-9、EGFR、IGF-1水平均低于对照组,PFS和OS均长于对照组。这一结果与文献报道相吻合[17]。分析原因为贝伐珠单抗联合FOLFIRI化疗方案治疗可发挥协同增效作用,提高抗肿瘤效果,且贝伐珠单抗能够破坏肿瘤血供,可进一步消除或缩小肿瘤病灶,提高治疗效果,降低肿瘤标志物水平,延长生存期。本研究结果同时显示,两组骨髓抑制、肝功异常、恶心呕吐、神经毒性和皮肤毒性等不良反应发生率比较,差异均无统计学意义。提示联合贝伐珠单抗用药未增加安全风险。
综上所述,贝伐珠单抗联合FOLFIRI化疗方案治疗晚期mCRC患者可提高疾病控制率,降低血清肿瘤标志物水平,延长生存期,效果优于单纯FOLFIRI化疗方案治疗。
参考文献
[1]陈昕涛,姚定康.单克隆抗体靶向治疗晚期或转移性结直肠癌研究进展[J].实用临床医药杂志,2020,24(6):11-14.
[2]方琳,刘超,张纯慧,等.转移性结直肠癌维持治疗的研究现状与治疗策略[J].实用肿瘤学杂志,2019,33(2):173-178.
[3]Heinemann V,von Weikersthal LF,Decker T,et al.FOLFIRI plus cetuximab or bevacizumab for advanced colorectal cancer:final survival and per-protocol analysis of FIRE-3,a randomised clinical trial[J].Br J Cancer,2021,124(3):587-594.
[4]王永辉,韩传军,黄剑辉,等.改良CAPIRI与标准FOLFIRI方案二线治疗转移性结直肠癌的疗效与安全性分析[J].中华全科医学,2020,18(5):749-751.
[5]黄满利,王功臣,杨寒,等.FOLFIRI方案对比CAPIRI方案用于晚期结直肠癌患者治疗的临床观察[J].实用癌症杂志,2021,36(6):985-988.
[6]邓文静,余更生,刘爱,等.贝伐珠单抗联合mFOLFOX6治疗转移性结直肠癌的临床疗效及左右半结肠癌的疗效差异[J].现代肿瘤医学,2020,28(5):779-783.
[7]中华人民共和国卫生和计划生育委员会医政医管局,中华医学会肿瘤学分会.中国结直肠癌诊疗规范(2017年版)[J].中华外科杂志,2018,56(4):241-258.
[8]马洪波,周琪,张献全.转移性结直肠癌维持治疗研究进展[J].现代肿瘤医学,2021,29(2):361-364.
[9]何友燕,刘浩,蔡丽君,等.艾迪注射液联合FOLFIRI方案对晚期结直肠癌患者的临床疗效[J].中成药,2021,43(9):2374-2378.
[10]徐宇轩,王文玲,杨远,等.UGT1A1基因不同表型与FOLFIRI方案治疗晚期结直肠癌疗效及毒副反应的相关性[J].现代肿瘤医学,2020,28(22):3920-3925.
[11]何婉.FOLFIRI联合西妥昔单抗或贝伐珠单抗治疗晚期结直肠癌:随机临床试验FIRE-3的最终生存及符合方案分析[J].结直肠肛门外科,2021,27(1):77-79.
[12]李穗华,胡楚璇,范翠苗,等.贝伐珠单抗联合一线化疗方案治疗晚期转移性结直肠癌的效果[J].中国当代医药,2019,26(33):136-138.
[13]曾艳,张力,贺帅.结直肠癌患者血清CEA和CA19-9水平与肝转移的关系[J].癌症进展,2019,17(13):1586-1589.
[14]马琛茹,关泉林,郝建鹏,等.血清Hcy、CEA、CA199对结直肠癌诊断价值及其分期的相关性研究[J].西部医学,2019,31(10):1549-1553.
[15]朱红珍,沈建东,俞志忠.血清表皮生长因子及受体、胰岛素样生长因子和结合蛋白在结直肠癌患者中的表达及其与疾病分期的关系[J].中国医学创新,2021,18(31):147-150.
[16]胡佳莉,陈丕峰,叶萍,等.CyclinD1、VEGF及EGFR在结直肠癌中的表达及临床意义[J].江西医药,2020,55(3):248-252.
[17]刘宁,杨文浩,王晓宇,等.贝伐珠单抗联合FOLFIRI方案对结直肠癌患者Gab2和ZEB1蛋白阳性率的影响[J].中国药业,2021,30(11):27-30.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/59622.html