SCI论文(www.lunwensci.com):
摘要:目的对山羊离体L4椎体分组进行脱钙,建立单椎体骨质疏松压缩性模型,对各组模型注入不同比例的Mendec骨水泥与同种异体骨粉的混合填充物,并分别进行生物力学实验,研究出强化后近似患椎骨折前的强度与刚度的最佳混合比例的骨填充物,从而能有效降低近邻椎体新发骨折的发生率。方法取年龄6-8年的雌性陕南白山羊胸腰段椎体(体重25-27Kg)的L4单椎体脊柱单元50个,将它们随机分为A、B、C、D、E组,每组有10个单椎体,分别测量并记录各组椎体的骨密度,使用EDTA-2Na脱钙液对各组椎体进行脱钙50天,达到骨质疏松标准,测量各组椎体的骨密度,使用力学试验仪对其进行压缩,制作单椎体骨质疏松压缩性骨折模型。将Mendec骨水泥与同种异体骨粉按体积比例制作混合填充物,混合比例分别为1:0、3:2、1:1、2:3、0:1,称为填充物α、β、γ、δ、ε,将五种填充物分别以中央分布的方式注入A、B、C、D、E五组模型中,体积均为3mL,经成形硬化后再次对各模型进行生物力学试验,记录各组模型的骨折前后、强化后以及力学试验后的椎体高度以及强化前后的抵抗极限强度以及刚度。结果五组单椎体单元脱钙前平均BMD为:(1.235±0.034)g/cm3,脱钙50天后平均BMD为:(0.844±0.055)g/cm3,下降率达31.7%,达到骨质疏松骨密度标准,单椎体骨质疏松模型建立成功。A、B、C、D、E五组脱钙前组间骨密度比较P>0.05,脱钙后组间骨密度比较P>0.05,差异无统计学意义,五组椎体压缩高度均达到II度压缩性骨折的标准。而且五组椎体强化前压缩高度组间比较P>0.05,差异无统计学意义,单椎体骨质疏松压缩性骨折模型建立成功。五组椎体在C臂下分别注入α、β、γ、δ、ε五种填充物3mL,填充物在椎体内分布方式控制为中央分布方式。强化后五组椎体恢复高度组间比较P>0.05,差异无统计学意义。因此,五种填充物均能有效恢复患椎高度,有效填充患椎。五组强化后椎体再压缩高度组间比较P>0.05,差异无统计学意义。五组模型强化前,椎体极限抵抗强度、刚度五组间比较P>0.05,差异无统计学意义。五组模型强化后,椎体极限抵抗强度分别为(±s):A组:5722.1±23.1N,B组:5201.2±29.8N,C组:4465.6±57.0N,D组:4210.1±49.8N,E组:3212.4±79.3N,五组间比较P<0.001,差异有统计学意义。而强化后五组椎体刚度分别为(±s):A组:1168.3±43.6N/mm,B组:963.0±11.0N/mm,C组:641.2±6.5N/mm,D组:524.8±7.6N/mm,E组:340.5±10.8N/mm,五组间比较P<0.001,差异有统计学意义。可认为在本实验条件下,随着同种异体松质骨粉比例的增加,强化后椎体的抵抗极限强度及刚度会随之下降。结论通过各组强化后各组椎体的极限抵抗强度和刚度与强化前椎体对比可知道,α、β填充物的强化的椎体模型的抵抗极限强度以及刚度远大于强化前的椎体,γ填充物强化后的椎体最大抵抗强度稍大于强化前的骨质疏松椎体,δ、ε两种填充物强化后模型的极限抵抗强度与刚度均小于强化前的椎体,骨水泥与同种异体骨粉体积比例达1:1时的γ填充物,其生物力学实验结果最接近骨折前的骨质疏松椎体。
关键词:老年性骨质疏松症;椎体骨质疏松模型;生物力学实验
本文引用格式:冯庆裕,谢文伟,王志坤,等.对同种异体骨与骨水泥不同配方制作成椎体成形模型的生物力学研究[J].世界最新医学信息文摘,2019,19(99):253-255,257.
Production of Extracorporeal Osteoporosis Model of Vertebral Body
FENG Qing-yu1,XIE Wen-wei2*,WANG Zhi-kun2,ZHONG huan1,ZHANG Jia-xun1,YIN Yu-chao1
(1.Guangdong Medical University,Zhanjiang Guangdong;2.Dongguan Third People's Hospital,Dongguan Guangdong)
ABSTRACT:Objective Of goats in vitro L4 vertebral grouping decalcified,establishing the model of single vertebral osteoporosis compressibility of each model into different proportion of Mendec bone cement is mixed with allogeneic bone implants,and biomechanical experiments respectively,to study the strengthening after approximation of vertebral fractures in front of the strength and stiffness optimal mix proportion of bone implants,which can effectively reduce the incidence of neighbor vertebral fractures in new cases.Methods Take 6 to 8 years of age in female goat thoracic lumbar vertebral body(weight 25-27 kg)of L4 single vertebral spine unit 50,they were randomly divided into group A,B,C,D,E,each group has 10 single vertebral body,respectively,measure and record each vertebral body bone mineral density,using EDTA-2 na decalcified fluid to decalcified 50 days of each vertebral body,reach the standard of osteoporosis.The bone density of each vertebral body was measured and compressed with a mechanical test instrument.The mixture of Mendec bone cement and allogeneic bone powder is made according to the volume ratio of 1:0,3:2,1:1,2:3 and 0:1,which is called fillerα、β、γ、δandε.Will be five kinds of fillers,respectively,in the form of the central distribution into A,B,C,D,E five groups model,the volume of 3 mL,after forming hardening again to biomechanical test of each model,records of each model,after reinforcement and mechanics test before and after fracture of vertebral body height and strengthening resistance before and after the ultimate strength and stiffness.Results The average BMD before decalcification was(1.235±0.034)g/cm3,and the average BMD after decalcification was(0.844±0.055)g/cm3.The decrease rate was up to 31.7%,which reached the standard of osteoporosis bone density.The bone mineral density of groups A,B,C,D and E before decalcification was P>0.05,and the bone mineral density of groups A,B,C,D and E after decalcification was P>0.05,showing no statistical significance.Comparison of compression height before vertebral body enhancement in the five groups showed no statistical significance(P>0.05),and the single vertebral body osteoporosis compression fracture model was successfully established.The five groups of vertebrae were injected with 3mL of fillers ofα、β、γ、δandεunder the C arm.The distribution mode of fillers in the vertebrae was controlled as the central distribution mode.After the enhancement,the height of vertebral body recovery in the five groups was compared with that in the five groups(P>0.05),with no statistical significance.Therefore,all the five kinds of fillers can effectively restore the height of the affected vertebra and fill the affected vertebra.The height of vertebral body recompression after enhancement in the five groups was P>0.05,with no statistical significance.Before the model enhancement in the five groups,the ultimate resistance strength and stiffness of the vertebral body were compared among the five groups(P>0.05),with no statistical significance.After the model enhancement in the five groups,the vertebral body ultimate resistance strength was(±s):group A:5722.1±23.1N,group B:5201.2±29.8N,group C:4465.6±57.0N,group D:4210.1±49.8N,and group E:3212.4±P<0.001 was compared among the five groups,and the difference was statistically significant.After the enhancement,the stiffness of the vertebral body in the five groups was(±s):1168.3±43.6N/mm in group A,963.0±11.0N/mm in group B,641.2±6.5N/mm in group C,524.8±7.6N/mm in group D,and 340.5±10.8N/mm in group E,P<0.001 was compared among the five groups,and the difference was statistically significant.It
0引言
骨质疏松性椎体压缩性骨折(OVCFs)是老年人常见的骨折,球囊扩张椎体后凸成形术(PKP)是治疗OVCF的常用手术方式[1],而聚甲基丙烯酸甲酯(PMMA)作为手术最常用的骨填充物,它能使被压缩的椎体恢复高度,并起到稳定椎体以及即时止痛的作用[2],但PMMA骨水泥的缺点明显,由于骨水泥硬度以及刚度较椎体大,PKP椎体成形术后的患者会出现邻近椎体新发骨折的现象。Yi X等[3]在研究发现,OVCFs患者在椎体成形术后一年内新发骨折率多达19.59%,而邻近椎体的骨折占55.17%,原因有可能是因为病椎经骨水泥填充强化后,强度增加过大,对相邻椎体产生应力对抗导致。包拥政[4]等人应用三维有限元法分析不同弹性模量骨水泥注射椎体成形后骨折椎体及邻近椎体的应力变化,结果发现降低骨水泥的弹性模量,可以有效降低临近椎体再骨折的发生。因此,寻求一种既能起到病椎强化临床效果,又能减少对相邻椎产生不良干扰的适合强度的填充物显得有必要性。本研究通过将不同比例的同种异体骨与PMMA骨水泥混合,降低填充物的弹性模量,并分别用不同比例的混合填充物对单椎体骨质疏松压缩性骨折模型行PKP手术,术后测定其生物力学性能,通过分析单椎体骨质疏松压缩性骨折模型在不同比例混合的填充物行椎体成形术后的椎体刚度、强度的差异,从而得到近似患椎骨折前强度与刚度的最佳混合比例的骨填充物,由此能有效降低近邻椎体新发骨折的发生率。
1材料
实验材料:模型取自年龄6-8年的雌性陕南白山羊胸腰段椎体(体重25-27Kg),节段为L4,称为单椎体脊柱单元50个,Mendec骨水泥(主要成分聚甲基丙烯酸甲酯),Bio-gene同种异体骨(产品规格:松质骨粉0.05-0.2mm。)。
实验仪器:双能X线吸收骨密度仪(Hologic Discovery Wi,Hologic Inc,Bedford MA,USA)、数字化X线照片机(DR)、C型臂X线机,岛津力学实验仪、Stryker电钻、2 mm钻头、游标卡尺(型号:0~150,上海量具,测量范围:0~150 mm,读数值:0.02 mm)、量筒、天平、pH试纸等。
实验试剂:EDTA-2Na(二乙胺四乙酸二钠,分子量336.21,广州伟达化工有限公司)、NaOH(氢氧化钠,分子量40,广州伟达化工有限公司)、10%甲醛溶液(10%中性缓冲福尔马林,浙江省金华市同和生物科技有限公司)、蒸馏水(25 kg/桶,东莞市仟净环保设备有限公司)。
2实验方法
2.1配制脱钙液
本实验使用EDTA-2Na脱钙液,配制方法为称取EDTA-Na2 165g,NaOH 20g加入800mL蒸馏水,然后剧烈搅拌液体至粉剂完全溶解后定容至1000mL,用PH试纸检测其值≈7.0,浓度为0.4916mmol/L。用此法大量复制脱钙液备用。
2.2实验分组
将50个单椎体随机分为A、B、C、D、E五组,每组有10个单椎体,经过肉眼与DR观察,无明显骨缺损,病变与畸形,去除椎旁肌肉与椎体表面的骨膜,切断横突保留3mm,棘突保留2cm,去除纤维环及关节盘,置于10%甲醛溶液中固定24h;将各组各个椎体的椎弓根与横突移行处作为钻孔点,使用Stryker 2mm钻头的电钻,角度为在矢状面上与椎体棘突成45°的成角,冠状面与椎体间隙平行,为同一人操作,钻孔前游标卡尺测深,打孔至椎体的中前1/3交界处,并使两孔相通,以便更好的为椎体脱钙以及为PKP手术做准备。测量所有椎体平均骨密度(BMD)并记录数值,并对每个单椎体进行标记。
2.3制作模型
2.3.1体脱钙
将A、B、C、D、E五组50个椎体浸泡于配制好的EDTA-Na2脱钙液中,每24小时更换脱钙液,脱钙50天。再次测量椎体平均骨密度(BMD)并记录数值;使单椎体单元达到骨质疏松诊断标准。
2.3.2单椎体压缩性骨折模型制作
使用岛津力学实验仪,使得单元椎的上下两个面与试验仪压缩模具贴合,并用1 mm/min的加载速度预压,力量达到100 N时停止,目的为消除蠕变运动,并且使单元椎充分固定于模具之中,不至于滑脱掉落影响数值的测定,充分固定完毕后试验力调零;采用5 mm/min的负荷加载速度进行压缩,试验力精确度为0.01 N,位移精确度为0.05 mm,试验中严密观察各个椎体变化,记录椎体试验力及椎体位移数据,椎体高度压缩至50%(即Ⅱ度压缩骨折)时停止,整个过程保持室温恒定并使用空针抽取生理盐水不断于单元椎上喷洒以保持湿润,减少误差;
2.3.3分组并调配不同比例的混合填充物
A组:将Mendec骨水泥粉剂及液剂混合,充分搅拌2分钟,得到骨填充物α。
B组:将Mendec骨水泥粉剂及液剂混合,充分搅拌2分钟,取体积为2.5mL的Bio-gene同种异体骨松质骨粉加入7.5mL骨水泥中,充分搅拌,使得骨水泥与同种异体骨粉体积比例达0.75:0.25,得到骨填充物β。
C组:将Mendec骨水泥粉剂及液剂混合,充分搅拌2分钟,取体积为5mL的Bio-gene同种异体骨松质骨粉加入5mL骨水泥中,充分搅拌,使得骨水泥与同种异体骨粉体积比例达1:1,得到骨填充物γ。
D组:将Mendec骨水泥粉剂及液剂混合,充分搅拌2分钟,取体积为7.5mL的Bio-gene同种异体骨松质骨粉加入2.5mL骨水泥中,充分搅拌,使得骨水泥与同种异体骨粉体积比例达0.25:0.75,得到骨填充物δ。
E组:将Bio-gene同种异体骨松质骨粉作为填充物ε。
2.3.4行椎体成形术
在C臂透视下,将穿刺针在双侧椎弓根钻孔处置入到椎体前1/3处,用扩张装置使球囊扩张3mL,退出球囊后,分别注入α、β、γ、δ、ε五组方式配制的骨填充物3mL,并控制为中央分布方式,骨填充物注射后,所有模型用塑料袋保存置入4℃冰箱12h后取出。
2.3.5椎体生物力学测定
将使用岛津力学实验仪,使得单元椎的上下两个面与试验仪压缩模具贴合,并用1 mm/min的加载速度预压,力量达到100 N时停止,目的为消除蠕变运动,并且使单元椎充分固定于模具之中,不至于滑脱掉落影响数值的测定,充分固定完毕后试验力调零;采用5mm/min的负荷加载速度进行压缩,试验力精确度为0.01 N,位移精确度为0.05 mm,试验中严密观察各个椎体变化,记录椎体试验力及椎体位移数据,加压至椎体高度压缩至50%停止,记录试验力大小及发生骨折的椎体的高度改变,整个过程保持室温恒定并使用空针抽取生理盐水不断于单元椎上喷洒以保持湿润,减少误差。
2.4统计分析实验结果
测定指标采用均数±标准差(±s)的形式表示,所有数据的统计分析均采用美国SPSS公司的SPSS 23软件进行分析。两组之间数据比较采用student't检验,多组之间的数据比较采用单因素方差分析。选用P<0.05为统计学显著性界值。
3实验结果
3.1OVCFs建模结果
3.1.1椎体OVCFs建模结果
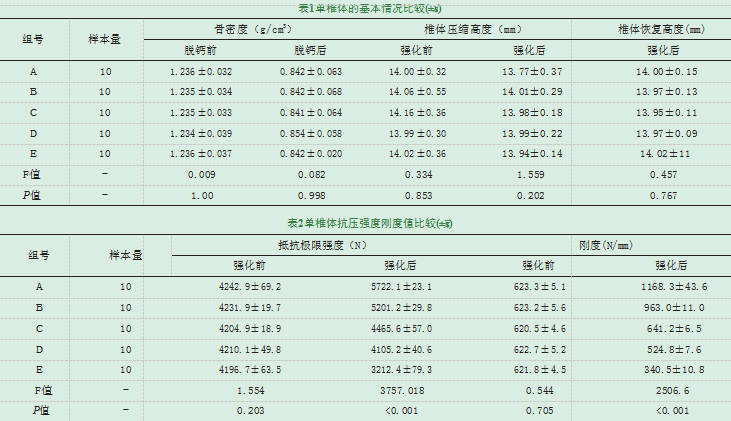
A、B、C、D、E五组50个单椎体单元脱钙前平均BMD为:(1.235±0.034)g/cm3,脱钙50天后平均BMD为:(0.844±0.055)g/cm3,下降率达31.7%,达到骨质疏松骨密度标准,证明单椎体骨质疏松模型建立成功,A、B、C、D、E五组脱钙前组间骨密度比较P>0.05,脱钙后组间骨密度比较P>0.05,差异无统计学意义。
岛津力学实验仪对A、B、C、D、E五组单椎体进行压缩,五组椎体压缩高度分别为(±s):A组:13.77±0.37mm,B组:14.06±0.55mm,C组:14.16±0.36mm,D组:13.99±0.30mm,E组:14.02±0.36mm。各椎体均达到II度压缩性骨折的标准,五组间压缩高度比较P>0.05,差异无统计学意义,单椎体骨质疏松压缩性骨折模型建立成功。
3.2OVCFs模型注入结果
A、B、C、D、E五组椎体在C臂下分别注入α、β、γ、δ、ε五种填充物5mL,填充物在椎体内分布方式控制为中央分布方式。
五组强化后椎体恢复高度分别为( ±s):A组:14.00±0.15mm,B组:13.97±0.13mm,C组:13.95±0.11mm,D组:13.97±0.09mm,E组:14.02±11mm。五组间强化后恢复高度比较P>0.05,差异无统计学意义。因此,五种填充物均能有效恢复患椎高度,有效填充患椎。
3.3生物力学结果
五组强化后椎体再压缩分别为(±s):A组:13.77±0.37mm,B组:14.01±0.29mm,C组:13.98±0.18mm,D组:13.99±0.22mm,E组:13.94±0.14mm。五组间强化后再压缩高度比较P>0.05,差异无统计学意义。
五组模型强化前,椎体极限抵抗强度分别为(±s):A组:4242.9±69.2N,B组:4231.9±19.7N,C组:4204.9±18.9N,D组:4210.1±49.8N,E组:4196.7±63.5N,五组间比较P>0.05,差异无统计学意义。而强化前五组椎体刚度分别为(±s):A组:623.3±5.1N/mm,B组:623.2±5.6N/mm,C组:620.5±4.6N/mm,D组:622.7±5.2N/mm,E组:621.8±4.5N/mm,五组间比较P>0.05,差异无统计学意义。
五组模型强化后,椎体极限抵抗强度分别为(±s):A组:5722.1±23.1N,B组:5201.2±29.8N,C组:4465.6±57.0N,D组:4210.1±49.8N,E组:3212.4±79.3N,五组间比较P<0.001,差异有统计学意义。而强化后五组椎体刚度分别为(±s):A组:1168.3±43.6N/mm,B组:963.0±11.0N/mm,C组:641.2±6.5N/mm,D组:524.8±7.6N/mm,E组:340.5±10.8N/mm,五组间比较P<0.001,差异有统计学意义。可认为在本实验条件下,随着同种异体松质骨粉比例的增加,强化后椎体的抵抗极限强度及刚度会随之下降。
通过各组强化后各组椎体的极限抵抗强度和刚度与强化前椎体对比可知道,α、β填充物的强化的椎体模型的抵抗极限强度以及刚度远大于强化前的椎体,γ填充物强化后的椎体最大抵抗强度稍大于强化前的骨质疏松椎体,δ、ε两种填充物强化后模型的极限抵抗强度与刚度均小于强化前的椎体,可认为γ填充物:骨水泥与同种异体骨粉体积比例达1:1时,其生物力学实验结果最接近强化前的椎体。
4讨论
OVCFs患者PKP术后邻近椎体骨折的原因较为复杂[5],有研究表明,填充物的分布方式、填充物的种类以及注射量与邻近椎体骨折相关[6],强化后的椎体的强度及刚度也与邻近椎体骨折发生率有关[7]。
因此,研究一种既能强化患椎,又不至于因为其强度与刚度过大而增加邻近椎体骨折发生率的填充物有重大的意义。
Lee的研究表明[8],使用EDTA-2Na能在6周内有效建立离体椎体骨质疏松模型,而本研究参考以上方法成功制作单椎体骨质疏松压缩性骨折模型,诊断骨质疏松标准使用骨量丢失百分率诊断法[9]。
本研究使用浓度为0.4916mmol/L的EDTA-2Na作为脱钙液,它能有效鳌合骨骼中的钙离子,而对骨骼的微观结构的损害较少,是目前作为椎体骨质疏松离体模型的主流脱钙剂。并将骨填充物的分布方式控制为中央分布,椎体强化后高度也控制在相同范围,骨填充物注射量也控制在3mL,排除了因填充物的注射量不同、在椎体内的分布方式不同以及填充物的渗漏所导致的干扰,且α、β、γ、δ、ε五种混合填充物恢复患椎的高度相近,而强化后的椎体强度及刚度不同。结果表明,注射α、β填充物的单椎体OVCFs模型的抵抗极限强度以及刚度远大于强化前的椎体,因而推断应用在人体内可能因此而诱发周围椎体再新发骨折,δ、ε填充后的椎体强度与刚度小于骨质疏松模型,不能起到强化椎体的作用,在体内应用可能容易发生患椎再发骨折及腰痛症状不缓解,γ填充物强化后的患椎强度与刚度稍强趋向接近于骨折前的骨质疏松模型椎体,可认为该比例的骨填充物符合达到既能支撑恢复椎体高度,又可使患椎强化前后的强度与刚度相近似于骨折前的实验目的,可向临床试验提供实验依据支持。但是至于γ填充物的比例能否有效减少临近椎体的再发骨折,仍需进一步进行多椎体多模式条件下的实验,以及动物体内实验、甚至以及临床试验才能证明其确实性。
参考文献
[1]刘桂东,陈德喜,李巍,等.经皮椎体成形术与非手术治疗骨质疏松性椎体压缩骨折的疗效的临床对照研究[J].中国骨与关节损伤杂志,2015(1).
[2]王平,王昊,武春雷,等.PMMA和Confidence高粘度骨水泥在老年胸腰椎骨折椎体成形术中的应用效果对比分析[J].中国现代手术学杂志,2016(06):40-43.
[3]Yi X,Lu H,Tian F,et al.Recompression in new levels after percutaneous vertebroplasty and kyphoplasty compared with conservative treatment[J].Archives of Orthopaedic and Trauma Surgery,2013,134(1):21-30.
[4]包拥政,祝周兴,冯云升,等.低弹性模量骨水泥对骨质疏松压缩性骨折椎体及邻近椎体应力的影响:三维有限元分析[J].中国组织工程研究,2016(16).
[5]侯文根,孙晓辉,张超,等.老年椎体压缩性骨折患者经皮椎体成形术后邻近椎体骨折的发生率及相关危险因素分析[J].中国矫形外科杂志,24(20):1909-1911.
[6]Kim J M,Shin D A,Byun D H,et al.Effect of bone cement volume and stiffness on occurrences of adjacent vertebral fractures after vertebroplasty[J].Journal of Korean Neurosurgical Society,2012,52(5):435-440.
[7]任海龙.椎体成形术治疗骨质疏松性椎体压缩骨折的临床及生物力学研究[D].2017.
[8]Lee C Y,Chan S H,Lai H Y,et al.A method to develop an in vitro osteoporosis model of porcine vertebrae:Histological and biomechanical study[J].Journal of neurosurgery.Spine,2011,14(6):789-98.
[9]崔轶,雷伟,吴子祥,等.绵羊椎体骨质疏松性生物力学模型的快速建立[J].中国骨质疏松杂志,2010,16(1):13-18.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/25720.html