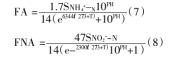摘要:短程硝化反硝化工艺凭借处理效能好、处理成本低等优势受到了广泛关注。基于此,文章首先综述了短程硝化反硝化技术的反应原理;其次重点介绍了短程硝化反硝化工艺的影响因素,包括温度、游离氨和游离亚硝酸盐浓度、pH、溶解氧、间歇曝气和盐度等;最后分析了短程硝化反硝化技术的优势与挑战,以期为短程硝化反硝化技术的推广和应用提供有益参考。
关键词:短程硝化反硝化,废水处理,脱氮工艺
氮元素是所有生命形式的必需营养素。然而,如果地表水氮排放过量,就容易导致藻类异常生长,从而造成溶解氧(DO)消耗。这种现象被称为富营养化,是影响世界各地河流、湖泊及河口水质环境的重要问题。地表水中的氮元素和磷元素主要来源于农业产生的有机废水与家庭及工业排放的污水。生物脱氮(BNR)可有效去除废水中的含氮化合物,使废水达到国家政策规定的排放标准[1]。
其中,短程硝化反硝化技术(SND)能够在特定操作条件下在单个生物反应器中将氮元素完全去除,与在城市污水处理厂单独生物反应器中进行的传统硝化和反硝化工艺截然不同。近年来,短程硝化反硝化技术受到了广泛关注。研究短程硝化反硝化技术的反应原理与影响因素,对于短程硝化反硝化工艺的推广和发展具有积极影响。
1短程硝化反硝化技术反应原理
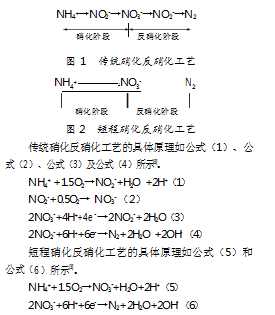
目前,大部分污水处理厂仍采用传统硝化反硝化工艺进行脱氮处理。传统硝化反硝化工艺是通过氨化作用将有机氮转化为氨根离子(NH4+)的过程,具体如图1所示。其中,硝化过程为氨根离子(NH4+)与氧气反应生成亚硝酸盐(NO2-),NO2-再通过氧化反应生成NO3-;反硝化过程为NO3-先还原为NO2-,再由NO2-还原为氮气(N2)[2]。
与传统硝化反硝化工艺相比,短程硝化反硝化工艺优化了中间产物NO2-。具体短程硝化反硝化工艺的原理如图2所示。该工艺通过氨化作用,将有机氮转化为NH4+。其中,硝化过程为NH4+与氧气反应直接生成NO3-;反硝化过程则为NO3-直接还原为N2。
传统硝化反硝化工艺中的硝化反应是在好氧条件下进行的生物过程。具体由两个相应的氧化步骤组成:第一步,氨氧化细菌(AOB)通过消耗1.5 mol氧气(O2)将NH4+氧化为NO2-,涉及氨单加氧酶(AMO)和羟胺氧化还原酶(HAO);第二步,亚硝酸盐氧化细菌(NOB)利用亚硝酸盐氧化还原酶(NXR)将NO2-转化为NO3-,且每转化1 mol NO3-需要消耗0.5 mol O2。短程硝化反硝化工艺中的硝化反应则是消耗1.5 mol O2直接将NH4+氧化为NO3-。由此可见,与传统硝化反硝化工艺相比,短程硝化反硝化工艺中的硝化反应节省了约四分之一的氧气。
传统硝化反硝化工艺中的反硝化反应是在缺氧条件下进行的生物过程。具体由两个相应的还原步骤组成:第一步,通过消耗4 mol外加碳源提供的氢离子(H+),将2 mol NO3-还原为2 mol NO2-;第二步,通过消耗6 mol H+,将2 mol NO2-还原为1 mol N2。短程硝化反硝化工艺中的硝化反应则是通过消耗6 mol的H+,直接将2 mol NO3-还原为1 mol N2。与传统硝化反硝化工艺相比,短程硝化反硝化工艺中的硝化反应节省了约40%的外加碳源。
2短程硝化反硝化工艺影响因素
为促进AOB的生长,同时抑制NOB活性,需要保持特定的工艺参数。实现短程硝化的主要控制条件包括温度、游离氨(FA)和游离亚硝酸盐(FNA)浓度、pH、溶解氧、间歇曝气和盐度等[4]。
2.1温度
短程硝化是一个复杂的反应过程,涉及多种酶的转化和多种中间产物的生成。从生物特性来讲,每个生物反应都有一个最佳反应温度范围。因此,可以通过调控反应器内的温度来控制AOB和NOB的生长速率,从而对AOB进行筛选、对NOB进行淘汰。
研究表明,在温度低于20℃时,NOB的最大比生长率普遍高于AOB。因此,建议将温度设置高于25℃,使AOB的数量超过NOB,并确保短程硝化反硝化工艺能够稳定运行[5]。
2.2游离氨(FA)和游离亚硝酸盐(FNA)
溶液中FA和FNA的浓度分别取决于NH4+和NO2-的浓度。溶液中FA浓度过高,可能会引发质子失衡、缺钾、细胞内pH改变,以及氧化还原反应被抑制等现象。FNA已被证实是一种影响能量产生的抑制剂。其能有效抑制NO2-和NO还原酶的表达。AOB和NOB的抑制阈值不同,且NOB更为敏感。FA在10~605 mgN/L时,会抑制AOB,而处于0.1~5 mgN/L时,则足以抑制NOB。已有检测发现,抑制AOB的FNA质量分数在0.42~1.72 mgN/L之间,而抑制NOB的FNA质量分数则在0.011~0.07 mgN/L[6]。研究表明,FNA质量分数在0.026~0.22 mgN/L时,会完全抑制NOB的活性[7]。
2.3 pH
pH对硝化效率和途径具有一定影响。研究表明,AOB的最佳pH为8.2~8.4,而NOB的最佳pH为7.2~7.9[8]。因此,较高的pH可促进AOB生长并抑制NOB的活性,而这正是短程硝化反硝化工艺所需要的。需要注意的是,在短程硝化反硝化工艺中,硝化过程中会释放H+,而AOB和NOB会消耗碱度,使硝化产生的酸性被反硝化产生的碱性所抵消,从而有效保持环中性的pH[9]。此外,pH改变还会引起溶液中FA和FNA浓度的变化。溶液中FA和FNA的计算公式如公式(7)和公式(8)所示[6]。
2.4溶解氧(DO)
溶解氧(DO)控制已被证实是在温度低于20℃的条件下维持硝化的最有效策略之一。O2是AOB和NOB氧化还原反应的末端电子受体。AOB的DO半饱和常数为0.2~0.4 mg/L,低于NOB的0.7~2.0 mg/L,表明AOB对O2的亲和力比NOB更强,意味着NOB在与AOB竞争DO的过程中往往处于劣势。然而,有研究发现,在低DO质量浓度下长期运行后,NOB对O2的亲和力会显著增强,这会使NOB比AOB更有能力竞争DO。通过维持1.0~1.5 mg/L的DO范围,可筛选出AOB而不是NOB,从而成功保障硝化反应的稳定运行。研究表明,在处理低碳氮比(2.8~3.8)的真实生活废水时,保持好氧阶段低DO质量浓度(1.4~1.6 mg/L),并利用短程硝化反硝化工艺,可以去除约56%的总氮[10]。
2.5间歇曝气(IA)
IA被认为是维持硝化的有效方法。其中,很大一部分原因在于IA对NOB有抑制效果。其抑制机制是将NOB活性从缺氧期滞后到好氧期。在缺氧条件下,NOB会在亚硝酸盐氧化还原酶(NXR)的作用下失活,随后又会在好氧阶段被重新激活。然而,在好氧阶段,AOB活性比NOB活性恢复得更快,导致AOB比NOB更具竞争优势。研究指出,NO2-氧化过程的滞后时间最短为15 min,比NH4+氧化过程中产生滞后时间要长。因此,应将缺氧时间设置为15~20 min,使有氧时间短于NOB滞后时间,保障IA足以抑制NOB的活性[11]。
这一滞后期的时间长度(15 min)被检测到是具有特异性的,取决于生物量在有氧时期所经历的DO水平。适应DO水平为0.9~1.0 mg/L的生物量的滞后期时长明显长于适应于较低DO水平(≤0.4 mg/L)的生物量。相比之下,缺氧时间超过15~20 min以及10~30℃的温度,不会影响滞后期的持续时间。
2.6盐度
盐度过高会对污染物去除产生不利影响,影响溶液中氮的去除效率。NOB对盐的敏感性高于AOB,盐度增加会引起NOB对盐的抑制。研究表明,当盐度为1.6%~2.4%时,短程硝化反硝化是最主要的脱氮途径[12]。以盐度为0%~2.4%的生活污水为进水溶液进行短程硝化反硝化反应,当盐度增加到1.4%~2.4%时,NOB活性受到抑制,因为该盐度下,NO2-会开始在生物反应器中积累。结果表明,高盐度降低了8.5%~17.3%的总氮。同样的,在短程硝化反硝化工艺中,当盐度从1%增加到2%时,NOB种群减少到了几乎无法检测到的水平。由此可见,盐度水平大于1%有利于短程硝化反硝化工艺的实施,尽管可能会由于抑制反硝化导致总氮去除率下降。需要注意的是,研究表明,盐度高于2.5%,也会对AOB活性产生负面影响[13]。
3短程硝化反硝化技术的优势与挑战
硝化和反硝化在中间过程均会产生一种强有力的温室气体,即一氧化二氮(N2O)。在硝化过程中,AOB可通过两种主要途径产生N2O:一种是作为终端电子受体的NO2-被还原为N2O(称为硝化器反硝化途径);另一种是羟胺(NH2OH)的不完全氧化。羟胺首先被化学分解为NO,然后被还原为N2O(羟胺途径)。与硝化作用类似,不完全反硝化也会导致N2O作为过程中间体被积累和排放。与硝化作用不同,反硝化过程中可产生N2O,但也会消耗N2O。
污水处理厂的脱氮工艺通常是依靠反硝化循环实现的。其中,在异养反硝化反应之后,便是有机物与NH4+联合氧化的好氧阶段。然而,该方法被认为是耗能的,且存在结构占地面积大、能源成本高、鼓风机维护难度大以及污泥产量高等问题,在经济上不可持续,无法处理小社区或农村地区产生的废水。近年来,新型生物工艺,如厌氧氨氧化和短程硝化反硝化等受到了广泛关注,其旨在降低污水处理厂的运行成本,同时确保排水符合水体氮排放限值。厌氧氨氧化菌在缺氧条件下可将NH4+直接氧化为N2,并从NO2-氧化为NO3-的过程中获得生长所需的能量。NO2-可通过NH4+的部分硝化(硝化)或NO3-的部分反硝化(反硝化)而产生。
尽管厌氧氨氧化在降低能耗和污泥产量方面具有显著优势,但厌氧氨氧化在主流废水处理中的应用仍会受到以下因素的限制:第一,厌氧氨氧化的最大比生长率较低(0.05~0.33/d));第二,出水中NO3-的排放过量;第三,操作温度高(30~40℃);第四,需要严格控制温度、pH和有机浓度,以提供最佳厌氧氨氧化生长条件。
短程硝化反硝化工艺是污水处理厂中预反硝化的一种合适且有前途的替代方法,可以同时去除C和N。该工艺具有以下优点:第一,碳需求和污泥产量减少了30%以上;第二,反硝化提供的碱度有助于维持中性pH;第三,不需要NO3-再循环;第四,曝气能量更低。
当然,短程硝化反硝化工艺也存在一些潜在缺点,主要包括以下几点:第一,与单独反硝化和硝化相比,N的去除率较低;第二,N2O积累显著;第三,由于系统中共存的不同微生物种类间存在竞争,反应过程并不稳定。
4结论
短程硝化反硝化工艺是一种前景良好的生物工艺,有望取代污水处理厂的传统脱氮工艺。然而,短程硝化反硝化工艺的应用增加了生物脱氮的复杂性。因此,必须对环境和生物因素进行严格控制,以保障AOB的正常生长,同时抑制NOB的活性,维持特定的操作条件。具体而言,应控制合适的温度与pH;保持适当的FA和FNA浓度;调控合适的溶解氧和盐度;进行适当的间歇曝气等。文章简要介绍了短程硝化反硝化工艺的原理和优势及其所面临的挑战,以期对未来的研究提供一定的帮助。
参考文献
[1]THAKUR I S,MEDHI K.Nitrification and denitrification processes for mitigation of nitrous oxide from waste water treatment plants for biovalorization:Challenges and opportunities[J].Bioresource Technology,2019,282:502-513.
[2]王加禄.短程硝化反硝化用于列车集便器污水处理的脱氮性能研究[D].北京:北京交通大学,2022.
[3]罗博,黄安寿,陈海龙.短程硝化反硝化氨氮脱除技术研究进展[J].环境与发展,2020,32(1):130-131.
[4]尹国策,魏佳音,何林锟.短程硝化脱氮技术研究进展[J].石油化工应用,2022,41(12):11-13.
[5]HEEJOON K,TIANJI L.Denitrification mechanism in combustion of biocoal briquettes[J].EnvironmentalScience&technology,2005,39(4):1180-1183.
[6]LU X Y,ADRIAN O,ZHAO J,et al.Insights on biological phosphorus removal with partial nitrification in single sludge system via sidestream free ammonia and free nitrous acid dosing[J].The Science of the Total Environment,2023,895:165174.
[7]韩晓宇,张树军,甘一萍,等.以FA与FNA为控制因子的短程硝化启动与维持[J].环境科学,2009,30(3):809-814.
[8]赵娜.短程硝化—反硝化聚磷菌脱氮除磷技术的研究与应用进展[J].辽宁化工,2017,46(1):99-102.
[9]姜体胜,杨琦,尚海涛,等.温度和pH值对活性污泥法脱氮除磷的影响[J].环境工程学报,2007(9):10-14.
[10]DI CAPUA F,IANNACONE F,SABBA F,et al.Simultaneous nitrification denitrification in biofilm systems for wastewater treatment:Key factors,potential routes,and engineered applications[J].Bioresource Technology,2022,361:127702.
[11]HIDAKA T,YAMADA H,KAWAMURA M,et al.Effect of dissolved oxygen conditions on nitrogen removal in continuously fed intermittent-aeration process with two tanks[J].Water Science and Technology:A Journal of the International Association on Water Pollution Research,2002,45(12):181-188.
[12]XIA Z G,WANG Q,SHE Z L,et al.Nitrogen removal pathway and dynamics of microbial community with the increase of salinity in simultaneous nitrification and denitrification process[J].Science of the Total Environment,2019,697:134047.
[13]SHE Z L,WU L,WANG Q,et al.Salinity effect on simultaneous nitrification and denitrification,microbial characteristics in a hybrid sequencing batch biofilm reactor[J].Bioprocess and Biosystems Engineering,2018,41(1):65-75.
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/ligonglunwen/81334.html