SCI论文(www.lunwensci.com):
摘要:为进一步探究β-苯乙醇制备工艺的可能优化路径,本文参考相关研究资料和实际情况,以环氧苯乙烷加氢方法制备β-苯乙醇,并通过多组平行实验,确定最优实验组合为:环氧苯乙烷用量为2.0 g,催化剂用量为0.04 g,溶剂用量为15 g,反应时间为1.5 h,反应温度为25℃。而后基于该实验组合进行放大实验与分析表征,结果显示,本次实验在产率上相对较优,且副产物较少,具有一定的实际应用价值。
关键词:β-苯乙醇;制备工艺;工艺流程
0引言
β-苯乙醇(β-phenylethanol)是一种具有芳香和鲜花香气的有机化合物,常用于食品、香料、化妆品和药物等领域,应用范围和用量均较广[1-2],因此较多化工企业均对β-苯乙醇的制备工艺方面较为关注,相关研究人员也对此进行了大量研究,涵盖了化学合成法、物理提取法和生物转化法等多种路径,但既有的研究难免存在一定不足之处,因此仍需要结合化工生产的实际情况,对β-苯乙醇制备工艺作进一步的研究与优化。
1实验方法
参考已有研究文献资料,并结合某化工企业的原材料储备情况,决定在本次研究中应用环氧苯乙烷加氢方法制备β-苯乙醇[3-5]。基于该技术模式,本次使用的原材料包括环氧苯乙烷、无水甲醇、Pd/C催化剂、高纯氢气,以上实验试剂级别均为分析纯。
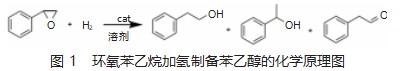
以上实验材料准备就绪后,即通过环氧苯乙烷加氢反应制备苯乙醇,其化学反应原理如图1所示。
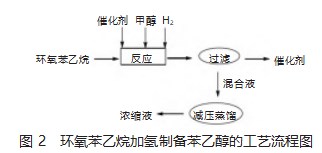
基于此,确定本次β-苯乙醇的制备工艺流程如下:取一定量的环氧苯乙烷、10%的Pd/C催化剂,以及无水甲醇,将上述3种材料均加入到三口烧瓶中,而后通入氢气排尽烧瓶中的空气,使烧瓶内一直保持氢气气氛;在氢气气氛下,启动磁力搅拌器进行搅拌,在一定温度下充分搅拌反应;反应结束后,对混合物进行过滤,滤出固相物质(催化剂),并对液相物质作减压蒸馏处理,以最终得到浓缩液,该浓缩液即为以β-苯乙醇为主成分的混合物。具体来看,本次合成工艺流程图如图2所示。
2不同因素对制备工艺的影响
2.1反应时间对反应收率的影响
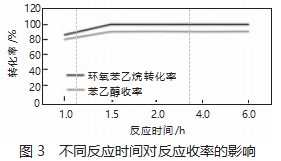
为探究反应时间对合成β-苯乙醇反应收率的影响,设置实验条件如下:环氧苯乙烷加入量为2 g,Pd/C催化剂加入量为0.04 g,无水甲醇(作为溶剂使用,下同)为15 g;反应温度设置为25℃,改变反应时间,分析反应收率的变化,分析结果如图3所示。
根据图3可知,随着反应时间的增加,β-苯乙醇的收率呈现出先增加而后趋缓的特点,而原料环氧苯乙烷的转化率则最终达到100%。初步推断,造成β-苯乙醇的收率在后期基本保持不变的原因是,原料环氧苯乙烷转化完全后,无法继续生成目标产物,因此适宜的反应时间为1.5 h。
2.2催化剂用量对反应收率的影响
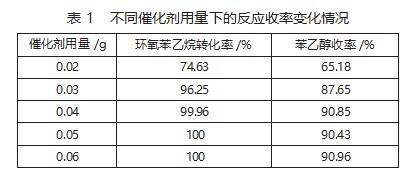
为探究催化剂用量如何影响反应收率,在本环节实验中,设置实验条件如下:环氧苯乙烷加入量为2 g,无水甲醇为15 g,反应温度设置为25℃,反应时间为1.5 h,对Pd/C催化剂用量进行调整,以分析反应收率的变化,得到实验结果如表1所示。
根据表1中的数据变化情况来看,当提升催化剂用量后,环氧苯乙烷转化率逐步增加,最终趋于100%,同时苯乙醇收率也呈现出先增加后趋于稳定的变化趋势。初步推断,造成这种变化趋势的主要原因是,当催化剂用量较少时,催化剂所起到的效果较为有限,收率相对较低;当增加催化剂用量后,反应的活性位点增加,加快环氧苯乙烷原料向目标产物的转化趋势,而随着催化剂用量的进一步增加,受到反应物分子结构的限制,反应的活性位点无法继续增多,因此反应平衡和速率均无法继续移动。就此综合分析后,确定0.04 g为催化剂的最适宜用量。
2.3溶剂用量对反应收率的影响
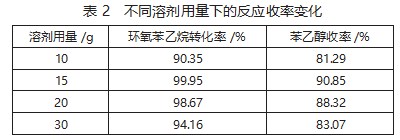
为探究溶剂用量对反应收率的影响,在本环节实验中,设置以下实验参数:环氧苯乙烷加入量为2 g,催化剂用量为0.04 g,反应温度设置为25℃,反应时间为1.5 h。在此基础上,改变有机溶剂甲醇的用量,探究该指标如何影响反应收率,实验结果如表2所示。
通过表2中的数据变化可知,随着溶剂用量的增加,原材料环氧苯乙烷的转化率呈现出先升后降的变化趋势,β-苯乙醇收率的变化也与之类似。这种变化趋势与前文存在一定差异,造成这种情况的主要原因是,溶剂量偏少时,反应物难以在反应环境中均匀分布,部分反应物难以得到充分反应;而当溶剂量过多时,反应物浓度降低,同样不利于部分反应物的有效接触和反应。对此综合分析后,确定合理的溶剂量为15 g。
2.4反应温度对反应收率的影响
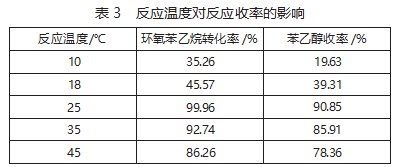
为探究反应温度对反应收率的影响,在本环节实验中设置如下前置条件:环氧苯乙烷加入量为2 g,催化剂用量为0.04 g,溶剂用量为15 g,反应时间为1.5 h。在此基础上,调整反应温度,平行开展5组实验,得到实验结果如表3所示。
根据表3的数据综合分析后可知,随着反应温度的逐步提升,环氧苯乙烷转化率和苯乙醇收率两项指标均表现为先增加后降低的特点,当反应温度为25℃时,两项指标均取得最大值。根据化学反应原理相关理论推断可知,在温度较低时升高温度,有助于提升反应物分子之间的碰撞,以加速目标产物的大量生成。而当温度超过25℃时,由于反应体系内能量较多,导致部分其他化学键断裂,发生副反应,因此也就降低了β-苯乙醇的收率。
2.5环氧苯乙烷投料量对反应收率的影响
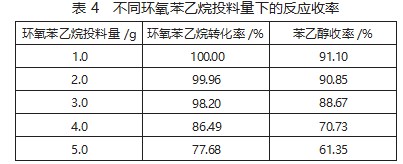
为探究环氧苯乙烷投料量对反应收率的影响作用,设置如下实验参数条件:催化剂用量为0.04 g,溶剂用量为15 g,反应时间为1.5 h,反应温度为25℃,在此基础上,改变环氧苯乙烷投料量,分析其对反应收率的影响,分析结果如表4所示。
根据表4中的数据进行综合分析后可知,环氧苯乙烷的投料量对环氧苯乙烷转化率和苯乙醇收率两项指标均表现为负面影响,相对而言,当投料量未超过3 g时,上述两项指标的下降并不显著。造成这种变化趋势的主要原因是,在该范围内的原材料大部分可转化为目标产物。而当环氧苯乙烷投料量进一步提升后,有限的催化剂已经无法保证所有原材料均可得到完全反应,导致环氧苯乙烷转化率和苯乙醇收率两项指标显著降低。综合分析上述内容后,确定最优投料量为2.0 g。
3分析表征
基于上述实验分析,确定本次β苯乙醇制备工艺的最优参数组合如下:环氧苯乙烷用量为2.0 g,催化剂用量为0.04 g,溶剂用量为15 g,反应时间为1.5 h,反应温度为25℃。基于该参数组合,按照实验流程重复进行β-苯乙醇制备实验,并采用放大实验模式进行,结果显示,苯乙醇收率为83.99%,表明本次实验在放大后仍具有一定的有效性,这为后续的工业实际应用提供了基础。
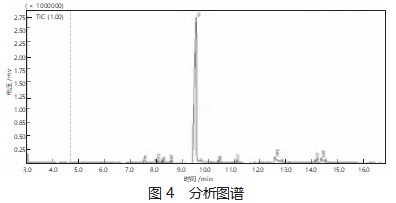
在此基础上,为检验生成产物,采用气相色谱质谱联用分析方法(GC-MS法)进行分析,在本次分析中,色谱柱采用Rtx-5MS型色谱柱,进样温度为220℃,以He为载气,首先在50℃恒温下保持3 min,而后以10℃/min的速率升温至250℃并保持6 min,以完成分析,分析完成后得到的图谱如图4所示。
根据图4中的分析图谱,参考NIST17-1.li数据库中的标准图谱数据进行综合对比分析后,确定本次制备实验所获得的产物中,主成分为β-苯乙醇,副产物为苯甲醇、苯乙醛和α-苯乙醇,这也表明本次制备工艺取得了初步成功。
4结语
整体来看,在本次研究工作中,以化工生产中较为常见的环氧苯乙烷为原材料,通过加氢反应方法制备β苯乙醇,并通过多组平行实验,对β苯乙醇制备工艺参数进行优化,最终确定最优工艺参数组合,以此开展放大实验,证明了本次β-苯乙醇制备工艺的有效性。从表征分析结果来看,本次实验不仅成功制备了β-苯乙醇,且副产物对环境的污染程度较低,较适合工业化生产,具有一定的继续研究价值。
参考文献
[1]申屠有德,金毅强,姚跃良,等.β-苯乙醇连续流合成工艺研究[J].香料香精化妆品,2022(4):79-81.
[2]吴高胜,王传昌,许保云.真空间歇精馏分离提纯天然β-苯乙醇的研究[J].广州化工,2021,49(22):45-47.
[3]朱灵桓.代谢工程改造酿酒酵母生产β-苯乙醇[D].无锡:江南大学,2021.
[4]卢真保,胡武,孙胜南.β-苯乙醇-活性炭颗粒的制备及其卷烟滤嘴加香效应的研究[J].山东化工,2018,47(12):22-24.
[5]王朝阳,姚跃良,李恩帅,等.β-苯乙醇的合成[J].香料香精化妆品,2017(2):12-14.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/ligonglunwen/78012.html