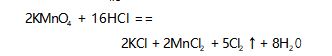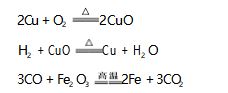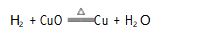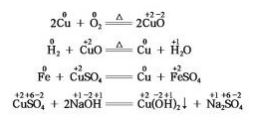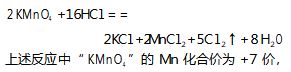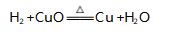SCI论文(www.lunwensci.com)
摘 要:微课是基于信息技术发展而来的教学工具,具有主题突出、针对性强、容量小等特点, 被广泛用于高中各科教学中.以鲁科版高中化学“ 氧化还原反应”教学为例,探讨模型认知下微课的设计以及实施.
1“ 氧化还原反应”内容的解读
“ 氧化反应反应”是高中化学中非常重要的概 念,从宏观以及微观两个角度对化学反应的本质进 行描述[1] . 学生学习该概念不仅有助于其对化学反 应有个更为全新的认识,而且对锻炼与提升其模型 认知核心素养有着积极的促进作用[2] .
鲁科版高中化学课本“ 氧化还原反应”部分共 包含三部分内容:认识氧化还原反应、氧化剂和还原 剂、氧化还原反应的应用.其中“ 认识氧化还原反 应”中主要介绍了氧化还原反应的定义以及本质. “ 氧化剂和还原剂”主要介绍了氧化剂、还原剂两个 概念以及高中阶段常见的氧化剂和还原剂.“ 氧化 还原反应的应用”从研究物质的性质、实现物质转 化、获取能量角度阐述氧化还原反应的应用.
“ 氧化还原反应”知识在高中化学中占有重要 地位,不仅是学生学习的重要知识点,而且是各类测 试的热门考点.该部分内容教学中教师应结合自身 教学经验,做好微课素材的收集以及制作,提高学生 的课堂学习体验,逐渐引导学生在头脑中建立氧化还原模型,深化对氧化还原反应知识的认识与理解, 并能灵活用于分析问题中.
2 模型认识下“ 氧化还原反应”微课设计
2 . 1 微课之氧化还原反应的特征
学生对该部分内容的学习热情以及掌握牢固程 度,会对后续内容学习产生较大影响,因此设计该部 分微课内容时应提升学生的学习体验,给其留下良 好的印象.具体可设计如下微课内容:
展示铜丝在空气中加热、氢气还原氧化铜、铁丝 与硫酸铜溶液反应、硫酸铜溶液与氢氧化钠溶液反 应的实验,要求学生认真观察实验现象,写出对应的 化学方程式.
预留一些空白时间,要求学生标出各反应中对 应元素的化合价,引导其从化合价变化角度对化学 方程式进行归类.
为学生讲解氧化还原反应概念,并分别阐述氧化 反应、还原反应.同时,告知学生化学反应中有元素的 化合价降低,就有元素的化合价升高,即使其认识到氧 化反应和还原反应通常统一于一个化学反应中.
2 . 2 微课之氧化还原反应的实质
为使学生对氧化还原实质有个清晰地认识,为 构建氧化还原反应模型打下坚实基础.围绕该部分 进行如下微课内容的设计:
展示钠在氯气中燃烧的实验.提出问题:氯气、 钠以及氯化钠分别由什么构成?钠在氯气中燃烧过 程中微粒发生了什么变化?展示课本中铁与硫酸铜 溶液反应的实验,要求学生认真观察实验现象,提出 问题:电流表指针为什么发生偏转? 该反应是否为 氧化还原反应?
从微观角度讲解钠在氯气中燃烧以及铁和硫酸 铜溶液反应的过程:钠在氯气中燃烧生成氯化钠,钠 原子变成了钠离子,因失去电子化合价由 0 价变为+ 1 价;氯原子变成了氯离子,因得到电子化合价由0 价变为 - 1 价;铁和硫酸铜溶液反应中铁元素因失去电子化合价由 0 价变为 + 2 价,铜元素因得到电 子化合价由 + 2 价降低至 0 价.提出问题:根据上述 内容的分析,你认为氧化还原反应的本质是什么? 要求学生自主完成课本中“方法导引”内容的学习, 使用两种方法标出以下化学反应中元素化合价的升降以及电子转移的情况:
2 . 3 微课之氧化剂与还原剂
在微课中展示如下化学反应:
提出问题:哪些物质含有的元素反应后化合价 升高、哪些化合价降低? 给学生预留思考时间,而后 讲解氧化剂与还原剂的概念.同时,要求学生指出以 下化学反应中哪些是氧化剂、还原剂? 具备的氧化 性还是还原性? 哪些物质被氧化和被还原?
展示酸性 KMnO4 溶液和 KI 溶液发生反应的实 验操作,要求学生观察实验现象,写出对应的化学方 程式,标出氧化剂、还原剂.另外,要求学生完成课本内容的学习,总结中学化学里常见的氧化剂和还原 剂,并完成以下填空:
中学化学里常见的氧化剂有活泼的非金属单 质,如 、 ;含有较高价态元素的含氧酸,如 、 ;含有较高价态元素的盐,如 、 、 ; 常见的还原剂有 , 以及 和 .在此基础上,预留时间要求学生联系所学,构建 有关氧化还原反应的模型.
2 . 4 微课之氧化还原反应的应用
在微课中要求学生阅读课本“方法导引”中“研 究物质氧化性或还原性的思路”的内容.而后要求 其填写“探究物质的氧化性或还原性”中表格内容 以及课本中“思考”中的问题.同时,要求学生阅读、 自学课本中的内容,要求其归纳影响物质氧化性和 还原性强弱的因素,列举运用氧化还原反应实现物 质转化与获得能量的具体案例,并鼓励其相互交流、 讨论,进一步加深对氧化还原反应作用的认识.同 时,展示如下习题,要求学生思考作答:
已知常温下在溶液中可以发生如下两个反应:
3 模型认识下“ 氧化还原反应”微课实施
3 . 1 氧化还原反应特征的教学
课堂上为学生播放上述设计、制作好的微课视 频.因微课中实验涉及的化学反应学生在初中阶段 已经学习,因此,对学生而言正确写出对应的化学方 程式难度并不大.三个实验对应的化学反应方程式 以及相关元素的化合价如下所示:
前三个实验中涉及的化学反应中,反应前后均 有相关元素化合价的变化,而硫酸铜溶液与氢氧化 钠溶液反应中,反应前后元素化合价没有发生变化, 学生很容易将上述反应划分为两类:元素化合价变 化的反应、元素化合价未变化的反应.在此基础上讲 解氧化还原反应概念,学生很容易掌握[1].
3.2 氧化还原反应实质的教学
在课堂上展示上述微课内容,要求学生认真 观察微课内容并积极思考微课中提出的问题,而 后提问学 生 代 表.显 然 氯 气 由 氯 分 子 构 成,钠 由 钠原子构 成,氯 化 钠 由 钠 离 子 和 氯 离 子 构 成.钠 在氯气中燃烧时钠原子转化成了钠离子,氯分子 转化成了 氯 离 子.同 时,学 生 观 察 微 课 中 铁 和 硫 酸铜溶液反应现象发现电流表的指针发生了偏 转,表明电 路 中 有 电 子 经 过.分 析 反 应 中 元 素 化 合价可 知 其 发 生 了 变 化,即 发 生 了 氧 化 还 原 反 应.联系所 学 的 电 学 知 识,可 知 氧 化 还 原 反 应 中 有电子发 生 了 转 移.经 过 后 续 微 课 内 容 的 学 习, 学生总结出了氧化还原反应的实质为电子转移. 当学生意识到这一 点,也就不难回答微课中给出 的习题.
得到电子化合价变为+2 价,生成产物“ MnCl2 ”,得子化合价变为 0 价,生成产物“Cl2 ”失去 e - × 10;认 识到这一点便不难使用双线桥和单线桥标出电子转 移的情况.
3.3 氧化剂与还原剂的教学
在进行该部分内容教学时,要求学生观察微课 视频,标出反应中相关元素的化合价.在此基础上要 求其认真倾听微课中有关氧化剂和还原剂概念的教 学.而后总结氧化剂、还原剂、氧化反应、还原反应、 氧化产物、还原产物之间的关系,使其彻底搞清楚、 弄明白.针对化学反应:
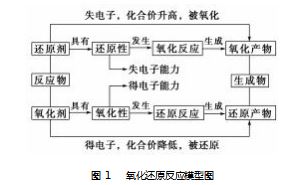
化反应,被氧化;Cu 化合价由 +2 价降低至 0 价, 为氧化剂,发生还原反应,被还原.另外,学生通过 阅读课本中的内容,很容易掌握中学化学中常见 的氧化剂和还原剂.至此学生已经对氧化还原反 应有个较为清晰地认识,而后要求其积极联系所 学,并给予针对性地引导,使其构建如图 1 所示的 氧化还原反应模型.
3.4 氧化还原反应的应用教学
学生 根 据 微 课 中 的 学 习 要 求 、结 合 课 本 内 容,不难填 写 表 格 内 容.其 中 向 双 氧 水 溶 液 中 滴 加酸性高锰酸钾溶液会看到产生气泡,高锰酸钾 溶液褪色,表 明 双 氧 水 具 有 还 原 性.向 双 氧 水 溶 液中滴加 KI 溶液和少量淀粉溶液会看到溶液变 蓝,表明双 氧 水 具 有 氧 化 性.在 此 基 础 上 联 系 所 学的氧 化 还 原 反 应 模 型,可 顺 利 地 回 答 课 本 中 “ 思考 ”部分的问题.另外,考虑到氧化性与还原 性强弱的比较是该部分的重点与难点.教学中要 求根据课本总结影响氧化性 、还原性强弱的因素 有:物质得失电子能力的强弱 、环境条件.在具体 的反应中告知学生以下结论:氧化剂的氧化性强 于氧化产 物 、还 原 剂 的 还 原 性 强 于 还 原 产 物.当 学生掌握上述内容后,便可顺利地完成微课中提 出的问题[ 2].
参考文献:
[1] 蒋闬.“模型认知”思维在高中化学教学运用分析[ J].数理化解题研究,2022(15):134 -136.
[2]徐凡.微课在高中化学概念教学中的应用研究[ J].数理化解题研究,2022(12):143 -145.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/jiaoyulunwen/70548.html