SCI论文(www.lunwensci.com):
摘要:小儿液体疗法是儿科临床上应用非常广泛的一种治疗方法,其中溶液的张力、混合溶液的张力计算、混合溶液的配制以及不同性质脱水的液体选用是公认的难点。针对难点,提出难点突破策略,化难为易,迅速理解和掌握液体疗法。
关键词:液体疗法;难点突破;策略
本文引用格式:文政,文沛莲.小儿液体疗法的难点突破策略[J].世界最新医学信息文摘,2019,19(71):370-371.
0引言
小儿液体疗法在儿科临床上应用非常广泛,历来是儿科学、儿科护理学的重点和难点,其中以溶液的张力、混合溶液的张力计算、混合溶液的配制、不同性质脱水的液体选用这四个方面的内容最为抽象难懂,是广大医学生、护士及基层医生公认的难点。为了突破难点,化难为易,笔者结合多年的临床与教学经验,总结出以下的难点突破策略,供广大医学生、护士及基层医务人员参考。
1溶液的张力
1.1溶液的概念
要理解溶液的张力,首先要弄清楚溶液的概念。溶液是指一种或几种物质(溶质)分散(溶解)到另一种物质(溶剂)里所形成的均一稳定的混合物。故溶液是由溶质和溶剂组成的。临床上用于液体疗法的溶液一般都是水溶液,水溶液是以水作为溶剂,葡萄糖、氯化钠、碳酸氢钠等作为溶质,如0.9%氯化钠溶液100g就是把0.9g氯化钠(分散)溶解于99.1g水里所形成的混合物,5%葡萄糖溶液100g就是把5g葡萄糖(分散)溶解于95g水里所形成的混合物。在实际应用中,常常要准确知道一定量溶液里含有多少溶质,即溶液的浓度,溶质越多,溶液浓度越大,如同量的10%葡萄糖溶液和5%葡萄糖溶液相比较,10%葡萄糖溶液的溶质(葡萄糖)多,浓度大。
1.2溶液渗透压的概念
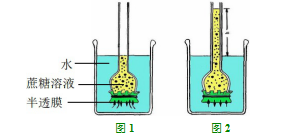
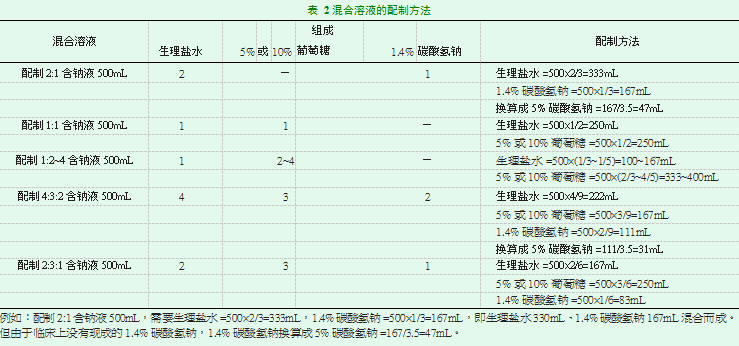
要理解溶液的张力,还需要弄清楚溶液渗透压的概念。儿科教材中未明确解释溶液渗透压的概念。现行的化学教材中渗透压定义是:“将纯溶剂与溶液以半透膜隔开时,为维持渗透平衡所需要加给溶液的额外压力”[1],通俗地说,溶液参透压就是水从纯溶剂或低浓度溶液穿过半透膜进入溶液或高浓度溶液时所产生的压力,也就是说溶液中溶质分子通过半透膜的一种吸引力量。例如:将蔗糖溶液、水分别置于漏斗和烧杯中,在漏斗的底部安置一个半透膜,以隔开蔗糖溶液和水,刚开始时漏斗和烧杯的液面高度相同,经过一段时间后漏斗内蔗糖溶液的液面升高,这说明蔗糖溶液中的蔗糖分子通过半透膜对水产生了吸引力,水通过半透膜进入蔗糖溶液,而蔗糖不能通过半透膜,从而导致漏斗内蔗糖溶液的液面升高、浓度降低,这个吸引力就是渗透压。水总是从水多的地方到水少的地方,即从水到溶液、从低浓度溶液到高浓度溶液。如图1、图2所示。
由此可见,任何溶液都有渗透压,溶液浓度越高,溶质分子对水的吸引力就越大,渗透压就越高。渗透压可以用来表示溶液的浓度,称为渗透浓度。人体血浆中含有电解质、小分子物质等晶体物质以及血浆蛋白,这些溶质分子通过半透膜对水所产生的吸引力称为血浆渗透压。血浆渗透压主要来自溶解于其中的晶体物质,特别是电解质,称为晶体渗透压,故临床上常用血钠浓度(正常为135~145mmol/L)来代表血浆渗透压,晶体物质不能自由通过细胞膜,而可以自由通过有孔的毛细血管,故晶体渗透压决定细胞膜两侧水分的转移,维持细胞内外水平衡;血浆蛋白等大分子胶体物质所产生的渗透压称为胶体渗透压,血浆蛋白不能通过毛细血管,故胶体渗透压决定血管两侧水分的转移,维持血管内外两侧水的平衡。
1.3溶液渗透压与张力关系
张力是指溶液在体内维持渗透压的能力,从某种意义上说张力等同于渗透压[2],临床上一般将溶液中电解质所具有的渗透压作为溶液的张力。人体的钠离子对维持血浆渗透压有着非常重要的作用,故临床上所说的张力,一般都是指钠离子所维持的渗透压。在临床或生理实验使用的各种溶液,其渗透压的高低是以人体血浆渗透压作为标准进行衡量的,血浆渗透压正常值为280~320mmol/L,医学上定为张力1张。与血浆渗透压相等的溶液称为等渗(张)溶液,张力=1张,如0.9%氯化钠溶液、1.4%碳酸氢钠溶液;低于血浆渗透压的溶液称为低渗(张)溶液,张力<1张,如1/2张含钠液;高于血浆渗透压的溶液为高渗(张)溶液,张力>1张,如5%碳酸氢钠溶液,张力为3.5张。临床上常用的5%葡萄糖溶液和10%葡萄糖溶液为非电解质溶液,不是盐溶液,其中5%葡萄糖溶液为等渗溶液,10%葡萄糖溶液为高渗溶液,因为葡萄糖输入体内后很快被氧化成二氧化碳和水,失去其渗透压的作用,故视为无张力溶液[3],可以把葡萄糖溶液当成水看待。
2混合溶液的张力计算
临床上在进行液体疗法时,常常将生理盐水(盐)、5%或10%的葡萄糖(糖)、1.4%碳酸氢钠(碱)中的二种或三种按一定比例配成不同的混合溶液,以满足患儿的病情需要。5%或10%的葡萄糖视为无张力溶液,生理盐水和1.4%碳酸氢钠为电解质等张溶液,都是盐溶液,是有张力的。故混合溶液的张力计算公式为:混合溶液的张力=(盐+碱)/(盐+糖+碱)。如表1所示。
例如:2:1含钠液:由2份生理盐水、1份1.4%碳酸氢钠组成,其张力=(2+1)/(2+1)=1张;4:3:2含钠液:由4份生理盐水、3份1份5%或10%葡萄糖、2份1.4%碳酸氢钠组成,其张力=(4+2)/(4+3+2)=2/3张。有了这样的简便计算公式和表格,混合溶液的张力计算就会变得简单易懂,避免死记硬背。
3混合溶液的配制
常用混合溶液的配制,儿科各种教材中都没有写出具体的配制方法,以至于许多医学生、护士和基层医生不知如何计算。具体配制方法如表2所示。
4不同性质脱水的液体选用
4.1理解脱水性质
要懂得不同性质的脱水的液体选用,首先要理解等渗性脱水、低渗性脱水、高渗性脱水这三种不同性质脱水的概念。脱水性质是指丢失体液时失钠与失水比例,临床上进行液体疗法时,原则是丢失什么就补什么、丢失多少就补多少。为了让抽象变具体,便于理解,可以把丢失的体液比喻成一锅绿豆汤,把体液中的钠(盐)比喻成绿豆,血钠浓度比喻成绿豆汤的均匀浓度,丢失体液相当于是用勺子舀出绿豆汤,绿豆和水量减少。绿豆汤久置后,绿豆会沉积于锅底。等渗性脱水是失钠=失水,血钠130~150mmol/L,就好比是充分搅匀后再舀出绿豆汤,舀出的绿豆和水的比例一样,绿豆汤的稀稠度没变;低渗性脱水是失钠>失水,血钠<130mmol/L,就好比是从锅底舀出绿豆汤,舀出的绿豆比水多,绿豆汤变稀了;高渗性脱水是失钠<失水,血钠>150mmol/L,就好比是从上面舀出绿豆汤,舀出的水比绿豆多,绿豆汤变稠了[4]。在临床上应重点监测血钠浓度,根据血钠浓度来确定脱水性质,血钠浓度130~150mmol/L为等渗性脱水,血钠<130mmol/L为低渗性脱水,血钠>150mmol/L为高渗性脱水。
4.2液体的选用
4.2.1等渗性脱水液体的选用
由于等渗性脱水是失钠(盐)=失水,应该补钠(盐)=补水,故应选用1:1含钠液或2:3:1含钠液,即1/2张含钠液。1:1含钠液中含有1份钠盐和1份糖水,2:3:1含钠液中含有3份钠盐(2份生理盐水和1份1.4%碳酸氢钠)和3份糖水,钠盐与水的比例相等,补液时可做到补钠(盐)=补水,用于纠正等渗性脱水。
4.2.2低渗性脱水液体的选用
由于低渗性脱水是失钠(盐)>失水,即以丢失钠(盐)为主,应该补钠(盐)>补水,故应选用4:3:2含钠液,即2/3张含钠液。4:3:2含钠液中含有6份钠盐(4份生理盐水和2份1.4%碳酸氢钠)和3份糖水,钠盐比水的比例多,补液时可做到补钠(盐)>补水,即以补钠盐为主,用于纠正低渗性脱水。
4.2.3高渗性脱水液体的选用
由于高渗性脱水是失钠<失水,即以丢失水为主,应该补钠<补水,故应选用1:2~4含钠液,即1/3~1/5张含钠液。1:2~4含钠液中含有1份钠盐和2~4份糖水,钠盐比水的比例少,补液时可做到补钠(盐)<补水,即以补水为主,用于纠正低渗性脱水。
5总结
综上所述,小儿液体疗法这些难点变得通俗易懂,难点得到了突破,使得广大医学生、护士和基层医生对液体疗法不再畏惧,同时还提高了他们对液体疗法的学习兴趣,迅速理解和掌握液体疗法,液体疗法不再是难题。
参考文献
[1]魏祖期.基础化学[M].北京:人民卫生出版社,2004.
[2]李冬燕.小儿液体疗法难点教学设计[J].世界最新医学信息文摘,2016,16(42):189-193.
[3]崔焱.儿科护理学[M].北京:人民卫生出版社,2013.
[4]文政.小儿腹泻液体疗法的教学设计及技巧[J].世界最新医学信息文摘,2015,15(93):313-316.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/22370.html