SCI论文(www.lunwensci.com):
摘要:目的了解甲磺酸阿帕替尼(apatinib)对晚期不能耐受化疗的恶性肿瘤患者的疗效及不良反应。方法将晚期不能耐受化疗的恶性肿瘤患者56例,随机分成治疗组和对照组。治疗组给予起始计量500mg/天单药阿帕替尼治疗并辅以对症及支持治疗,对照组仅给予对症及支持治疗,观察两组患者的临床疗效、中位无进展生存期、中位总生存期及药物相关不良事件。结果获得PR 5例,SD 9例,DCR 46.7%,RR 16.7%。对照组患者中,SD 7例,PD 19例(每2月复查评效,2个月时进展5例,4个月时进展9例,6个月时进展4例,10个月时进展1例),DCR 26.9%,RR为0。结论单药阿帕替尼对晚期不能耐受化疗的恶性肿瘤患者有较好的治疗效果,延长了患者的无进展生存期,大多数患者对500mg/天的阿帕替尼单药治疗耐受性良好。
关键词:阿帕替尼;不能耐受化疗;晚期恶性肿瘤;疗效;不良反应
本文引用格式:郑璐瑶,王迎利,苏乌云.阿帕替尼对晚期不能耐受化疗的恶性肿瘤患者的治疗价值[J].世界最新医学信息文摘,2019,19(66):33-35,38.
Therapeutic Value of Apatinib in Patients with Advanced Malignant Tumor Who Can not Tolerate Chemotherapy
ZHENG Lu-yao 1,WANG Ying-li 2,SU Wu-yun 3*
(1.Inner Mongolia Medical University,Hohhot Inner Mongolia;2.Department of General Internal Medicine,Baotou Cancer Hospital Inner Mongolia;
3.Department of Oncology,Affiliated Hospital of Inner Mongolia Medical University,Hohhot Inner Mongolia)
ABSTRACT:Objective To investigate the efficacy and adverse reactions of apatinib mesylate(apatinib)in patients with advanced malignant tumors who could not tolerate chemotherapy.Methods Fifty-six patients with advanced malignant tumor who could not tolerate chemotherapy were randomLy divided into treatment group and control group.The treatment group was treated with single drug apatinib combined with symptomatic and supportive treatment,while the control group was treated with symptomatic and supportive treatment only.The clinical efficacy,median progression-free survival,median overall survival and drug-related adverse events were observed in the two groups.Results There were 5 patients received 9 with SD,DCR 46.7%and RR 16.7%.In the control group,7 patients received SD and 19 patients received PD(The results were reviewed every 2 months from the beginning of treatment.5 patients made progress at 2 months,9 patients at 4 months,4 patients at 6 months,and 1 patient at 10 months),DCR 26.9%,RR 0.Conclusion Single apatinib has a good therapeutic effect on patients with advanced malignant tumor who can not tolerate chemotherapy,prolongs the progression-free survival time of patients,and most patients have good tolerance to single apatinib treatment with 500mg/days.
KEY WORDS:Apatinib;Chemoradiotherapy Intolerance;Advanced malignant tumor;Efficacy;Side effects
引言
根据2017年国家肿瘤登记处收集的数据,全国31省、市、自治区肿瘤登记资料汇总后发现,全国范围内新发恶性肿瘤病例数为380.4万例,相当于平均每天均有超过10,000名被确诊患有癌症的人,恶性肿瘤已经成为中国乃至全世界最大的医学问题之一[1]。在中国,不论是城市还是农村,恶性肿瘤都是居民的主要死亡原因之一,且对于晚期不能耐受化疗的恶性肿瘤患者,尤其是高龄患者,治疗效果差难度大、患者对化疗药物的依从性及耐受性欠佳而不适合联合化疗,疾病后期生存质量较差,目前尚无标准有效的维持治疗方案。2014年12月13日,中国首个完全自主研发的小分子血管内皮生长因子受体-2(vascular endothelial growth factor receptor-2,VEGFR-2)抑制剂甲磺酸阿帕替尼(apatinib)在中国上市[2,6]。研究表明,阿帕替尼可以在较低浓度下有效抑制VEGFR。Cheng-Ming Li等人的研究已经证明其在胃癌治疗中的有效性[3-5]。目前有关阿帕替尼在其他晚期不能耐受化疗的恶性肿瘤中的应用报道较少,本文以我院及包头市肿瘤医院收治的56例晚期不能耐受化疗的恶性肿瘤患者为研究对象,分析单药阿帕替尼对晚期不能耐受化疗的恶性肿瘤患者的临床疗效及药物相关不良事件。
1资料与方法
1.1入组及排除标准
1.1.1入组标准
年龄在30-85岁之间;二线及以上化疗失败或不能耐受化疗;至少有一个可测量病灶;ECOG评分2-3分;预计生存期≥3个月;主要器官(心脏、肝脏、肾脏、肺等)功能正常;育龄期妇女需尿hCG试验阴性;所有患者均自愿服用阿帕替尼,并向患者家属明确说明服药期间可能出现的并发症和风险;所有患者签署知情同意书。
1.1.2排除标准
合并其他致死性疾病的患者;生育期无可靠避孕措施的女性;存在消化道梗阻的患者;有血栓病史的患者(PICC引起的除外);II级以上重要脏器功能不全的患者;阿帕替尼过敏者;有严重出血风险的患者;伴有甲状腺功能减退者;近期有手术或外伤史且伤口未愈合的患者;非正常死亡患者。
1.2一般资料
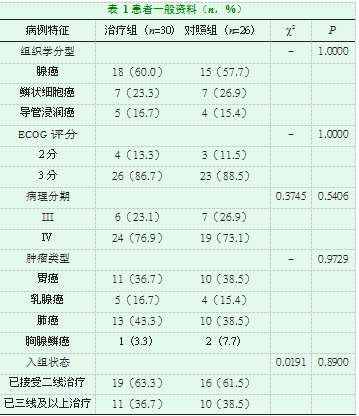
纳入2017年1月到2018年5月我院及包头市肿瘤医院中晚期不能耐受化疗的恶性肿瘤患者56例,所有患者均符合入组标准。治疗组30例,男性13例,女性17例,年龄36-81岁,平均年龄(58.76±4.59)岁;疾病类型:胃癌11例、乳腺癌5例、肺癌13例、胸腺鳞癌1例;病理类型:腺癌18例、鳞癌7例、导管浸润癌5例;TNM分期:III期(包括III期的所有亚组)6例,IV期(包括IV期的所有亚组)24例;ECOG评分:2分4例,3分26例;已接受二线化疗者19例,已接受三线及以上治疗者11例。对照组26例,男性16例,女性10例,年龄34-83岁,平均年龄(56.45±4.23)岁,疾病类型:胃癌10例、乳腺癌4例、肺癌10例、胸腺鳞癌2例;病理类型:腺癌15例、鳞癌7例、导管浸润癌4例;TNM分期:III期(包括III期的所有亚组)7例,IV期(包括IV期的所有亚组)19例;ECOG评分:2分者3例,3分者23例;已接受二线化疗者16例,已接受三线及以上治疗者10例。化疗进展至服用靶向药物时间:<2个月2例;2~4个月5例;4~6个月13例;大于6个月10例。一般资料的卡方检验结果显示,P均大于0.05,差异无统计学意义,尚无理由认为治疗组和实验组组间有差别,即实验组和对照组对比无差别(详见表1)。
1.3治疗方案
治疗组患者给予起始剂量500mg/d的阿帕替尼(国药准字H20140105)治疗,餐后30min口服,每4周为1个治疗周期,每个治疗周期允许停药不超过2次,累计不超过14天。在每个治疗周期,随时评估患者耐受性并对药物计量进行调整(具体原则参照《阿帕替尼治疗胃癌的临床应用专家共识》[7]),下调剂量为250mg/次,剂量下调后不可再回调至上一水平,受试者最多允许进行一次剂量调整,不允许再次进行剂量的上调或下调。
1.4疗效评价
根据RECIST 1.1版进行疗效评价,完全缓解(CR):患者的靶病灶完全消失,并保持4周以上;部分缓解(PR):患者所有靶病灶直径总和缩小程度>30%,并维持4周;稳定(SD):靶病灶直径之和增加程度<20%,或者缩小<30%;进展(PD):靶病灶的直径之和增加>20%。有效率(RR)=(CR+PR)/总例数×100%,疾病控制率(DCR)=(CR+PR+SD)/总例数×100%。采用NCI CTC 3.0版标准评估药物相关不良事件。
1.5随访
随访于2019年3月停止,通过电话及门诊进行患者随访。无进展生存期(progression-free survival PFS)定义为患者从服用阿帕替尼治疗直至出现进展或死亡的时间。
1.6统计学分析
采用SPSS 20.0版软件进行统计学分析,计量资料表示为(±s),组间比较用t检验,计数资料以率(%)表示,组间比较用2检验及Fisher确切概率法,生存分析采用Kaplan-Meier法,P<0.05表示差异有统计学意义。
2结果
2.1治疗经过及疗效
在治疗组中,30例患者的最短治疗时间为10天(因不能耐受而中断),最长者为10个月。其中2例患者治疗时间少于2个月,(2例均因疾病进展或死亡而停药);5例患者接受了2-4个月的治疗,(1例因药物不良反应而中断,4例因疾病进展或死亡停药),13例患者接受了4-6个月的治疗,(3例因药物的不良反应中断,10例因疾病进展或死亡而停药),10例患者治疗时间大于6个月,(3例因药物的不良反应而中断,7例因疾病进展或死亡而停药)。治疗组30例患者经阿帕替尼单药治疗后未出现完全缓解的病例,PR 5例,SD 9例,DCR 46.7%,RR 16.7%;在对照组的患者中,无完全缓解和部分缓解的患者,PD 19例(5名在2个月评效为PD,9名在4个月评效为PD,4例在6个月评效为PD,1例在10个月评效为PD),7例评效SD(见表2)。
2.2随访结果
通过Kaplan-Meier法对治疗组和对照组的无进展生存期(PFS)绘制生存曲线(见图1),2=15.290,P<0.001,差异有统计学意义,治疗组mPFS为6.800(5.854,7.746)个月,对照组mPFS为5.100(4.056,6.144)个月(详见表3及表4)。治疗组和对照组的总生存期(OS)绘制生存曲线(见图2),2=14.428,P<0.001,差异有统计学意义,治疗组mOS为10.000(3.996,16.034)个月,对照组mOS为5.100(4.110,6.090)个月(详见表5及表6)。
2.3不良事件
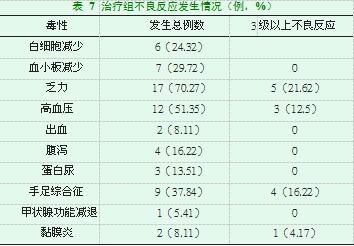
研究表明,阿帕替尼治疗恶性肿瘤相关的不良事件包括血液学毒性(白细胞减少症、血小板减少症等)和非血液学毒性(乏力、高血压、出血、腹泻、蛋白尿、甲状腺功能减退症、黏膜炎和手足综合征等)[8-10]。在本研究治疗组的30例患者中,共24例出现药物相关不良事件,其中10例出现2种及以上的不良事件。不良事件均为1-3级,无与药物相关的4级不良事件发生。最常见的药物相关不良事件为:乏力(17例,发生率为70.27%)、高血压(12例,发生率为51.35%)、手足综合征(9例,发生率为37.84%)、血小板减少(7例,发生率为29.72%),其余的不良反应有:白细胞减少(6例,发生率为24.32%)、腹泻(4例,发生率为16.22%)、蛋白尿(3例,发生率13.51%)、出血(2例,发生率为8.11%)、黏膜炎(2例,发生率为8.11%)和甲状腺功能减退症(1例,发生率为4.17%)。3级不良反应例包括乏力(5例,发生率为21.62%))、手足综合征(4例,发生率为16.22%)、高血压(3例,发生率为12.5%)、黏膜炎(1例,发生率为4.17%。出现不良反应后给予阿帕替尼减量和(或)对症治疗。高血压的发生均在2-4周,可以使用ACEI/ARB类药物,每日监测血压。蛋白尿均在4周左右出现,给予口服金水宝或尿毒清颗粒,一周监测一次尿常规及24小时尿蛋白定量。出现皮肤反应患者,轻者给予地塞米松软膏,重者联合使用手足平1号。大多数药物相关不良事件可通过下调剂量和(或)对症支持治疗来控制,并可以继续接受阿帕替尼治疗(见表7)。
3讨论
随着社会的发展及人们生活方式的改变,中国恶性肿瘤的发病率逐年上升,恶性肿瘤发病年龄逐渐趋于年轻化同时就诊时即被诊断为晚期的风险也在逐年增加,对于晚期恶性肿瘤患者来说,身体状况欠佳、疾病进展迅速、对化疗药物的依从性和耐受性差成为晚期恶性肿瘤患者治疗的主要问题。患有晚期恶性肿瘤的患者,特别是那些经过多线化疗的患者,最终因机体产生抗药性而导致治疗失败或不能继续耐受化疗,治疗手段有限。分子靶向药物的出现为晚期恶性肿瘤患者的治疗提供了新的策略[11]。
早在1971年,Folkman等人提出了肿瘤的血管生成理论[6],此后,肿瘤的抗血管治疗一直是研究的热点。2014年12月13日我国首个完全自主研发的小分子血管内皮生长因子受体-2(vascular endothelial growth factor receptor-2,VEGFR-2)抑制剂甲磺酸阿帕替尼被批准在中国上市。阿帕替尼的作用靶标为血管内皮生长因子途径,可高度选择性地竞争细胞内ATP的结合位点,以抑制VEGFR-2酪氨酸激酶活性,阻断血管内皮生长因子信号通路并抑制肿瘤组织内血管的形成。研究表明,阿帕替尼在较低浓度即可有效抑制VEGFR[13-18]。目前有关阿帕替尼的报道主要集中在胃癌、乳腺癌、肺癌和肝癌中[19-23],它在胃癌Ⅱ期和Ⅲ期的临床试验中均显示出良好的客观缓解率和生存获益。在大型单中心Ⅲ期临床试验中,实验组给予起始剂量阿帕替尼(850mg,日1次),其OS较安慰剂组延长了1.8个月,而死亡风险降低约30%;DCR分别为42.05%和8.79%。从安全性的角度来说,其不良事件的类型和发生率与已上市的其他同类药物类似,且通过调整剂量和(或)对症治疗可控制和逆转大多数不良事件[3-5]。基于此,2014年10月17日,国家食品药品管理监督总局(CFDA)批准甲磺酸阿帕替尼(apatinib)用于晚期胃癌或胃食管连接部腺癌三线和三线以上治疗。
在本研究纳入2017年1月到2018年5月我院及包头市肿瘤医院中晚期不能耐受化疗的恶性肿瘤患者56例,随机分为治疗组和对照组。治疗组给予初始计量500mL/d的阿帕替尼治疗,最长观察时间为10个月。结果显示治疗组30例患者经阿帕替尼单药治疗后未出现完全缓解的病例,PR 5例,SD 9例,DCR 46.7%,RR 16.7%;在对照组的患者中,无完全缓解和部分缓解的患者,PD 19例(5名在2个月评效为PD,9名在4个月评效为PD,4例在6个月评效为PD,1例在10个月评效为PD),7例评效SD。治疗组46例患者中,mPFS为5.60个月,mOS为8.65个月。对照组45例患者中,mPFS为3.86个月,mOS为5.96个月。同时,服药大于6个月的患者,mPFS为4.78个月;小于6个月者为2.94个月(2=15.683,P<0.005)。总的来说,与对照组相比治疗组的DCR和RR均显著增高,无进展生存期及总生存期也均有延长,且P<0.05,差异具有统计学意义;同时本研究发现治疗组30例患者中,服药时间大于6个月者较服药时间小于6个月者mPFS明显延长。上述结果表明,阿帕替尼对晚期不能耐受化疗的恶性肿瘤患者有良好的治疗效果。从药物相关不良事件而言,本研究治疗组的30例患者中,最常见的不良反应为:乏力、高血压、腹泻及蛋白尿,出现3级及以上不良反应患者较少,且绝大多数患者经减量或者对症治疗后可继续接受阿帕替尼治疗。
本研究发现,单药阿帕替尼对晚期不能耐受化疗的恶性肿瘤患者有较好的疗效,多数患者对500mg/天阿帕替尼单药治疗耐受性良好,为晚期不能耐受化疗的恶性肿瘤患者提供了新的治疗思路。
参考文献
[1]Chen W,Sun K,Zheng R,et al.Cancer incidence and mortality in China,2014[J].Chin J Cancer Res,2018,30(1):1-12.
[2]Tian S,Quan H,Xie C,et al.YN968D1 is a novel and selective inhibitor of vascular endothelial growth factor receptor‐2 tyrosine kinase with potent activity in vitro and in vivo[J].Cancer science,2011,102(7):1374-1380.
[3]姚艺玮,何义富,胡冰.阿帕替尼治疗晚期胃癌临床观察[J].中华肿瘤防治杂志,2017,24(06):389-393.
[4]周雷,孙延沙,王小龙,等.阿帕替尼联合替吉奥在晚期胃癌二线及以上治疗中的临床疗效观察[J].当代医学,2018(5):52-54.
[5]Cheng-Ming Li,Zhi-Chao Liu,You-Ting Bao.Extraordinary response of metastatic pancreatic cancer to apatinib after failed chemotherapy[J].世界胃肠病学杂志:英文版,2017:7488.
[6]Folkman J.Tumor angiogenesis:therapeutic implication[J].N Engl J Med,1971,285:182-186.
[7]秦叔逵,李进.阿帕替尼治疗胃癌的临床应用专家共识[J].临床肿瘤学杂志,2015,20(9):841-847.
[8]时佳琪,刘超,张艳桥,等.甲磺酸阿帕替尼治疗恶性肿瘤的临床不良反应分析[J].中国肿瘤临床,2018,45(4):191-195.
[9]詹海燕,杨健,戎佩佩.某院甲磺酸阿帕替尼片超说明书用药及其不良反应分析[J].药物流行病学杂志,2018(3).
[10]李嫱,崔慧娟,彭艳梅.阿帕替尼引起的手足皮肤反应的文献系统综述[J].中国新药杂志,2018,27(22):124-128.
[11]Folkman J.Opinion:Angiogenesis:an organizing principle for drug discovery?[J].Nature reviews Drug discovery,2007,6(4):273.
[12]Wen S,Shao G,Zheng J,et al.Apatinib regulates the cell proliferation and apoptosis of liver cancer by regulation of VEGFR2/STAT3 signaling[J].Pathology-Research and Practice,2019,215(4):816-821.
[13]佚名.阿帕替尼对晚期非小细胞肺癌患者的疗效及VEGFR2-906T>C多态性位点的影响[J].中华医学杂志,2019,99(2):105.
[14]Ferrara N,Gerber H P,LeCouter J.The biology of VEGF and its receptors[J].Nature medicine,2003,9(6):669.
[15]Longo R,Gasparini G.Challenges for patient selection with VEGF inhibitors[J].Cancer chemotherapy and pharmacology,2007,60(2):151-170.
[16]Holmes K,Roberts O L,Thomas A M,et al.Vascular endothelial growth factor receptor-2:structure,function,intracellular signalling and therapeutic inhibition[J].Cellular signalling,2007,19(10):2003-2012.
[17]Mirabella T.Stimulation of Therapeutic Angiogenesis Using Amniotic Fluid Stem Cells[M]//Perinatal Stem Cells.Springer New York,2014:125-138.
[18]Gang H,Yan W,Bi W,et al.Effects of vascular endothelial growth factor expression on pathological characteristics and prognosis of osteosarcoma[J].Clinical&Experimental Medicine,2015,16(4):1-8.
[19]Li Wang,Juan Lu,Yi Liu.A retrospective analysis of the safety and efficacy of apatinib in treating advanced metastatic colorectal cancer[J].肿瘤学与转化医学(英文),2017(5).
[20]Li Wang[1],Juan Lu[1],Yi Liu[1].A retrospective analysis of the safety and efficacy of apatinib in treating advanced metastatic colorectal cancer[J].肿瘤学与转化医学:英文版,2017(3):216.
[21]陈玲娟,伍钢,董晓荣.阿帕替尼二线及二线以上治疗晚期肺癌26例[J].医药导报,2018,37(05):551-554.
[22]Liu K,Ren T,Huang Y,et al.Apatinib promotes autophagy and apoptosis through VEGFR2/STAT3/BCL-2 signaling in osteosarcoma[J].Cell Death&Disease,2017,8(8):e3015.
[23]Jing Ding,Xiao-yan Cheng,Shuang Liu,et al.Apatinib exerts anti-tumour effects on ovarian cancer cells[J].Gynecologic Oncology,2019,153(1).
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/18633.html