SCI论文(www.lunwensci.com)
【摘要】 目的:比较抗体 22C3 与 SP263 检测非小细胞肺癌标本程序性死亡分子 1 配体(PD-L1)水平的一致性。方法: 选取 2020 年 1 月至 2021 年 8 月该院病理科检测的 40 例肺非小细胞肺癌标本进行前瞻性研究,均进行免疫组织化学检测,比较抗体 22C3 与 SP263 检测(不同病理分型、不同 T 分期)非小细胞肺癌标本 PD-L1 水平的结果判定难度等级、阳性检出率,采用 Kappa 检验分析抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 水平的一致性。结果: 抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 水平的结果判定难度等级比 较,差异无统计学意义(P>0.05) ;抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 阳性检出率比较,差异无统计学意义(P>0.05); 抗 体 22C3 与 SP263 检测不同病理分型非小细胞肺癌标本 PD-L1 阳性检出率比较,差异无统计学意义(P>0.05); 抗体 22C3 与 SP263 检测不同 T 分期非小细胞肺癌标本 PD-L1 阳性检出率比较,差异无统计学意义(P>0.05);Kappa 检验结果显示, 抗体 22C3 与 SP263 检测非小细胞肺 癌标本 PD-L1 水平的一致性高(Kappa 值 =0.823.P<0.05)。 结论: 抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 水平的一致性高。
【关键词】 PD-L1;22C3,SP263,非小细胞肺癌标本,免疫组织化学法,阳性检出率,一致性
Comparison of consistency of antibody 22C3 and SP263 in detection of PD-L1 level in non-small cell lung cancer specimens
WANG Baoqiang, SHAO Qiongyi, SUN Bo*
(905 Hospital of People’ Liberation Army Navy, Shanghai 200050. China)
【Abstract 】 Objective: To compare consistency of antibody 22C3 and SP263 in detection of PD-L1 level in non-small cell lung cancer specimens. Methods: A prospective study was conducted on 40 non-small cell lung cancer specimens detected by the department of pathology of the hospital from January 2020 to August 2021. All were detected by immunohistochemical method. The difficulty level of result judgment and the positive detection rate of PD-L1 level in the non-small cell lung cancer specimens detected by antibody 22C3 and SP263 (different pathological types and different T stages) were compared. Kappa test was used to analyze the consistency of antibody 22C3 and SP263 in the detection of the PD-L1 level in the non-small cell lung cancer specimens. Results: There was no significant difference in the difficulty level of result judgment of the PD- L1 level in the non-small cell lung cancer specimens between antibody 22C3 and SP263 (P>0.05). There was no significant difference in the positive detection rate of PD-L1 in the non-small cell lung cancer specimens between antibody 22C3 and SP263 (P>0.05). There was no significant difference in the positive detection rate of PD-L1 between antibody 22C3 and SP263 in different pathological types of non-small cell lung cancer (P>0.05). There was no significant difference in the positive detection rate of PD-L1 between antibody 22C3 and SP263 in different T stages of non-small cell lung cancer (P>0.05). Kappa test results showed that the consistency of antibody 22C3 and SP263 in the detection of the PD-L1 level in the non-small cell lung cancer specimens was high (Kappa value =0.823. P<0.05). Conclusions: The consistency of antibody 22C3 and SP263 in the detection of the PD-L1 level in the non-small cell lung cancer specimens is high.
【Keywords】 PD-L1; 22C3; SP263; Non-small cell lung cancer specimen; Immunohistochemistry; Positive detection rate; Consistency
免疫组织化学检测结果可为临床诊疗提供参 考 [1-2] 。程序性死亡分子 1 配体(PD-L1)通路激 活,可加速恶性肿瘤免疫逃逸,通过靶向 PD-L1 进行抗肿瘤免疫治疗,可获得满意的治疗效果 [3-4]。 为提高 PD-L1 的检测效果,实现精准治疗的目的,本文比较抗体 22C3、SP263 检测非小细胞肺癌标本 PD-L1 水平的一致性。
1 材料与方法
1.1 材料 选取 2020 年 1 月至 2021 年 8 月本院 病理科检测的 40 例肺非小细胞肺癌标本进行前瞻 性研究。纳入标准:获取肺癌标本前患者未经抗肿 瘤治疗。患者及家属对本研究内容了解且自愿签署 知情同意书,研究经本院伦理委员会审批通过。所 有组织样本用 3.7% 甲醛溶液固定,固定时间 24 h, 利用 Leica ASP6025 全自动组织处理仪进行组织样本脱水、透明、浸蜡、HE 染色。所有组织样本细 胞形态完好,无退变,组织样本无污染。
1.2 方法 组织样本连续切片,厚度 4 μm。光镜 观察病理组织学形态,选取无出血、坏死的肿瘤组 织进行免疫组织化学检测,抗体 22C3 检测器械为 Dako 公司产的 Autostainer Link 48 型免疫组织化学 染色仪、Dako 公司产的 PTLink抗原修复仪;抗体 SP263 检测器械为 Ventana 二抗体系及全自动染色 仪,采用 PD-L1 标准试剂盒检测。
结果判读:由两名高年资病理医师采用双盲 法独立阅片,免疫组织化学阳性反应物定位于细胞 膜。两种抗体互换cut-off值,筛定出公共cut-off值。 阴性:阳性细胞 / 总细胞数比例 <1%;低表达:阳 性细胞 / 总细胞数比例为 1%~50%;高表达:阳性 细胞 / 总细胞数比例 >50%[5] 。结果判定难度等级:Ⅰ 级:容易判断; Ⅱ级:判断难度一般,经比较 后可判定; Ⅲ级:判读困难,仔细判断仍存在一定 难度。
1.3 观察指标 (1) 比较抗体 22C3 与 SP263 检 测非小细胞肺癌标本 PD-L1 水平判定难度等级。
(2)比较抗体 22C3 与 SP263 检测非小细胞肺癌 标本 PD-L1 阳性检出率。(3) 比较抗体 22C3 与 SP263 检测不同病理分型非小细胞肺癌标本 PD-L1 阳性检出率。(4) 比较抗体 22C3 与 SP263 检测 不同 T 分期非小细胞肺癌标本 PD-L1 阳性检出率。
(5) 采用 Kappa 检验分析抗体 22C3 与 SP263 检测 非小细胞肺癌标本PD-L1水平的一致性。一致性好: Kappa 值 >0.75;一致性一般:Kappa 值为 0.4~0.75; 一致性差:Kappa 值 <0.4.
1.4 统计学方法 应用 SPSS 20.0 软件进行统计学 分析,计量资料以( x(—) ±s )表示,采用 t 检验,计 数资料以率(%)表示,两种抗体检测非小细胞肺癌标本 PD-L1 阳性检出率比较采用 χ2 检验,两种 抗体检测不同病理分型、不同 T 分期的非小细胞肺 癌标本 PD-L1 阳性检出率比较采用 Fisher 确切概 率法,两种抗体检测非小细胞肺癌标本 PD-L1 水 平的一致性分析采用 Kappa 检验,以 P<0.05 为差 异有统计学意义。
2 结果
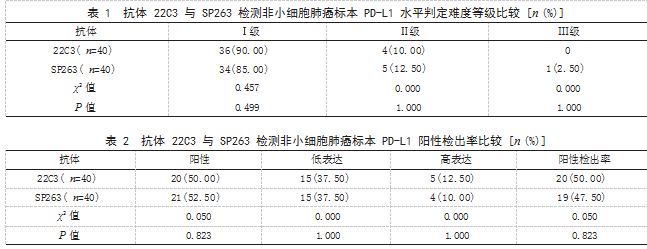
2.1 抗 体 22C3 与 SP263 检 测 非 小 细 胞 肺 癌 标 本 PD-L1 水平判定难度等级比较 抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 水平判定难度 等级比较,差异无统计学意义(P>0.05)。见表 1.
2.2 抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 阳性检出率比较 抗体 22C3 和 SP263 检测 非小细胞肺癌标本 PD-L1 的阳性检出率比较,差 异无统计学意义(P>0.05)。见表 2.
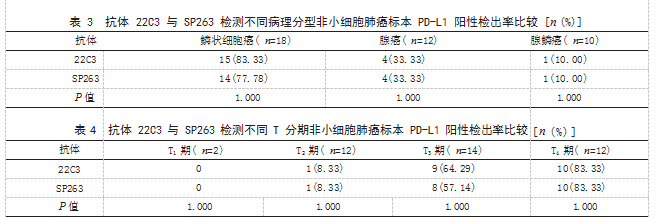
2.3 抗体 22C3 与 SP263 检测不同病理分型非小细 胞肺癌标本 PD-L1 阳性检出率比较 40 例非小细 胞肺癌标本中鳞状细胞癌 18 例,腺癌 12 例,腺鳞 癌 10 例。抗体 22C3 和 SP263 检测不同病理分型非 小细胞肺癌标本 PD-L1 的阳性检出率比较,差异 无统计学意义(P>0.05)。见表 3.
2.4 抗体 22C3 与 SP263 检测不同 T 分期非小细胞 肺癌标本 PD-L1 阳性检出率比较 40 例非小细胞 肺癌患者 T1 期 2 例,T2 期 12 例,T3 期 14 例,T4 期 12 例。抗体 22C3 与 SP263 检测不同 T 分期非 小细胞肺癌标本 PD-L1 阳性检出率比较,差异无 统计学意义(P>0.05)。见表 4.
2.5 一致性分析 Kappa 检验结果显示,抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 水平 的一致性好(Kappa 值 =0.823. P=0.000)。
3 讨论
准确、可靠的 PD-L1 检测结果可为非小细胞肺癌患者免疫治疗的选择提供参考 [5-7] 。免疫组织 化学法是检测 PD-L1 水平的主要方法,可真实反 映抗原蛋白表达状态,有效识别及预测患者能否从 抗肿瘤免疫治疗中获益 [8-10]。
22C3 和 SP263 均为免疫组织化学检测非小细 胞肺癌标本 PD-L1 的常用抗体,使用 22C3 抗体 检测时可只观察标本肿瘤细胞膜染色情况判读结 果,SP263 抗体检测结果判读标准与 22C3 抗体基 本相同,但若 SP263 抗体检测结果显示仅肿瘤细胞 基底膜染色不可作为阳性细胞,需同时侧膜染色才 可判为阳性 [11-13] 。本研究结果显示,抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 阳性检出率比 较,差异无统计学意义;抗体 22C3 与 SP263 检测 不同病理分型非小细胞肺癌标本 PD-L1 阳性检出 率比较,差异无统计学意义;抗体 22C3 与 SP263 检测不同 T 分期非小细胞肺癌标本 PD-L1 阳性检 出率比较,差异无统计学意义;Kappa 检验结果 显示, 抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 水平 的一致性好(Kappa 值 =0.823)。 这 一结果与文献报道相吻合 [14] 。提示抗体 22C3 与 SP263 检测非小细胞肺癌标本 PD-L1 的一致性高, 且不受患者病理分型、肿瘤分期影响。
本研究结果同时显示,抗体 22C3 与 SP263 检 测 PD-L1 判定难度等级比较,差异无统计学意义。 提示两种免疫抗体均能清楚显示 PD-L1 阳性表达 状态。值得注意的是,肿瘤细胞标本免疫组化检测 结果的判定需通过人为、半定量手段,故主观性较 强,应由高资质的病理医师判断为宜 [14]。
综上所述,抗体 22C3 与 SP263 检测非小细胞 肺癌标本 PD-L1 水平的一致性高。
参考文献
[1] 刘静,张克强 . FLOT-1 在人类实体肿瘤中的研究进展 [J]. 中国肿瘤临床,2018.45(13):695-698.
[2] 周疆帆, 单云峰 . 免疫检查点 PD-1/PD-L1 抑制剂与 CAR-T治疗在肝癌中的研究进展 [J]. 肝胆胰外科杂志, 2020. 32(2): 7-12.16.
[3] 韦俐, 蒋敬庭 .PD-L1 表达及其调控在胶质瘤免疫治疗中作用的研究进展 [J]. 中国肿瘤生物治疗杂志,2020.27(5):104-108.
[4] 中国抗癌协会肿瘤病理专业委员会肺癌学组,中国抗癌协会肺癌专业委员会,PD-L 检测共识专家组 . 非小细胞肺癌 PD-L1 免疫组织化学检测规范中国专家共识 [J]. 中国肺癌杂 志,2020.23(9):733-740.
[5] Lou SK,Ko HM,Kinoshita T, et al. Implementation of PD-L1 22C3 IHC pharmDxTM in Cell Block Preparations of Lung Cancer: Concordance with Surgical Resections and Technical Validation of CytoLyt Prefixation[J]. Acta Cytol,2020.64(6):577-587.
[6] 姜玉勃, 刘昱辰, 黄勇, 等 . PD-1/PD-L1 免疫检查点抑制剂抗肿瘤治疗现状及其疗效预测标志物的研究进展 [J]. 癌症进 展,2018.16(11):6-14.
[7] 袁培,郭嫦媛,李媛,等 . 晚期肺腺癌活检标本 PD-L1 免疫组织化学多平台检测一致性研究 [J]. 中华病理学杂志,2018. 47(11):840-844.
[8] Kim T,Cha YJ,Chang YS. Correlation of PD-L1 Expression Tested by 22C3 and SP263 in Non-Small Cell Lung Cancer and Its Prognostic Effect on EGFR Mutation-Positive Lung Adenocarcinoma[J]. Tuberc Respir Dis(Seoul),2020.83(1):51-60.
[9] Tsao MS, Kerr K M, Kock x M, et al. PD-L1 immunohistochemistry comparability study in real-life clinical samples: results of blueprint phase 2 project [J]. J Thorac Oncol,2018.13(9): 1302-1311.
[10] 江悦,宋国新,张炜明,等 . 两种免疫组织化学平台和抗体检测 PD-L1 表达的一致性分析 [J]. 中华病理学杂志,2019. 48(11):867-872.
[11] 张大川,史勇强,闫战涛,等 . 非小细胞肺癌内 PD-L1 表达及其与肺腺癌新分类的关系 [J]. 中华病理学杂志,2020.49 (6) :607-609.
[12] 李凯旋,李建强 . PD-1/PD-L1 免疫检查点抑制剂在非小细胞肺癌中的诊疗进展 [J]. 临床肺科杂志, 2020. 25(7) :1105-1109.
[13] 骆新兰,罗陆侨,何娇,等 . 免疫组织化学检测条件对PD-L1(22C3) 染色结果的影响 [J]. 中华病理学杂志,2020. 49(11):1108-1113.
[14] 李梅,陈龙云,李冬梅,等 . 非小细胞肺癌肿瘤细胞不同抗体 PD-L1 免疫组织化学染色一致性分析 [J]. 中华病理学杂志, 2020.49(11):1174-1176.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/61922.html