SCI论文(www.lunwensci.com):
摘要:目的 探索微柱凝胶法直接抗球蛋白试验用 IgG 型阳性质控品的制备方法。 方法 采用 IgG 型抗 D 试剂致敏 O 型 Rh(D) 抗原 阳性红细胞的方法来制备阳性质控品。通过三组试验来评估制作阳性质控品时 IgG 型抗 D 试剂的最适加入量、最佳反应温度和最佳反应 时间,然后对制作的阳性质控品进行连续 60 d 试验来监测其稳定性。结果 在取自血站血辫的 2 mL 全血标本中,IgG 型抗 D 试剂的最 适加入量为 125 μL,最佳反应温度为室温, 最佳反应时间为 20 min。制备的阳性质控品在连续监测 60 d 内直接抗球蛋白试验结果稳定, 为 3+ 凝集强度。结论 采用 IgG 型抗 D 试剂致敏来自血站血袋血辫中的 O 型 Rh(D) 抗原阳性红细胞的方法制备的直接抗球蛋白试验阳 性质控品,结果稳定可靠,可以应用到日常直接抗球蛋白试验工作中。
关键词: 直接抗球蛋白试验; 质控品; 微柱凝胶法
Preparation and clinical applications about positive control materials for the direct anti-globulin test of IgG type in micro- column gel immune-assay method
CHEN Lilong1, WANG Houfang2, YU Junfeng2
( 1.Department of Laboratory, United Family Women’s & Children’s Hospital, Beijing 100101, China; 2.Department of Laboratory, Beijing United Family Hospital, Beijing 100015, China )
Abstract: Objective To explore the preparation method of positive quality control materials for the direct anti-globulin test(DAT) of IgG type in Micro-column gel immune-assay. Methods Type O and Rh(D) antigen - positive erythrocytes were sensitized with IgG - D reagent. Three groups of tests were performed to evaluate the optimal amount of IgG anti-D reagent, the optimal reaction temperature and the optimal reaction time during the preparation of positive quality control products, and then the stability of the positive quality control products was monitored by continuous tests for 60 days. Results The optimal amount of IgG anti-D reagent was 125μL, the best reaction temperature was room temperature and the best reaction time was 20 min. The DAT results of the produced positive quality control products were stable with 3+ agglutination strength for 60 consecutive days. Conclusion DAT positive quality control products prepared from type O and Rh(D) antigen positive red blood cells induced by IgG anti-D reagent is stable and reliable. It can be used in daily direct anti-globulin tests.
Keywords: Direct anti-globulin test(DAT); Control materials; Micro-column gel immune-assay
直接抗球蛋白试验(direct anti-globulin test, DAT ), 是用来检测红细胞(RBC)表面是否包被了免疫球蛋白或 (和)补体的一项简易试验 [1]。该试验主要用来辅助诊断迟 发性溶血性输血反应 [2]、自身免疫溶血性贫血(AIHA) [3-4]、 胎儿和新生儿溶血症 [5]、药物所致的免疫性溶血 [6] 等,应 用十分广泛。
目前 DAT 的检测方法主要有试管法、微柱凝胶法、 U 型板法等。微柱凝胶技术具有敏感度高、操作简便、结果易判读的优点 [7] ;而且全自动仪器微柱凝胶法用于直接 抗人球蛋白试验初筛具有操作标准化、结果清晰可保存、 敏感度高的优点 [8] ,所以微柱凝胶法应用十分广泛。为保 证 DAT 结果的准确性,该试验需使用阳性质控品来验证 阴性结果的有效性 [9- 10]。目前临床常用的 DAT 检测类型主 要包括单抗 IgG 型和单抗 C3d 型及二者的混合型(多特异 度), 可辅助临床诊断和治疗 [11]。目前试管法与 U 型板法 有商品化的 IgG 型阳性质控品, 但尚无商品化的适合微柱凝胶法的质控品。因此,我们通过以下试验,探索制备应 用于微柱凝胶法 DAT 的 IgG 型阳性质控品。
1 材料与方法
1.1 标本来源 标本来自北京市通州区中心血站的 O 型 供者血袋所附血辫中的全血标本,标本符合无溶血、无 异常凝集 [12], 血浆部分无明显乳糜, 采集时间为 10 d 以 内。留取血辫中全血标本,然后对标本进行多特异度(抗 IgG&C3d)DAT 筛查试验,结果为阴性者可以使用。
1.2 试剂和仪器 IgG 型抗 D 试剂,上海血液生物医药 有限公司,批次: 20180626,测定抗体滴度为 1 ∶ 256; DG Gel DC Scan 抗人球蛋白检测卡,简称 Scan 卡(包 含单抗 IgG、单抗 C3d、多特异度 IgG&C3d),Diagnostic Grifols,S.A. 公司,批次: 18002.01;DG Gel Coombs 抗 人球蛋白检测卡,简称 Coombs 卡(只含有多特异度抗 IgG&C3d),Diagnostic Grifols,S.A. 公司,批次: 18006.01; 贝索配血专用离心机(台湾贝索,型号: 2005 - 2 )、 GRIFOLS 配血专用离心机( Diagnostic Grifols,S .A . 公 司)、全自动配血及血型分析仪( Diagnostic Grifols, S .A . 公司,国械注进 20183401737,型号: WADiana Compact)、加样枪、37 ℃水浴箱、4 ℃冰箱、一次性吸头、 吸管、试管、低离子液、生理盐水等。
1.3 方法 微柱凝胶法手工操作,严格按照 Diagnostic Grifols,S.A. 公司试剂说明书进行。全血标本 1 000 r/min 条件下离心 3min,取 10 μL 压积红细胞到 1 mL 配套低离 子液( DG Gel Sol)中, 配成 1% 红细胞悬液, 混匀, 取 1% 红细胞悬液 50 μL 加到相应微孔管中,在 GRIFOLS 配 血专用离心机心后判读结果。结果判读,以红细胞留在微 柱上端或分布在凝胶中为阳性 [7]。
使用全自动配血及血型分析仪操作,严格按照仪器操 作手册进行。全血标本 1 000 g 离心 3 min 后直接上机操 作。结果判读,以红细胞留在微柱上端或分布在凝胶中为 阳性 [7]。
1.3.1 通过试验探索致敏红细胞的方法 累计挑选 2018 年 5 月至 2020 年 2 月北京和睦家医院血库收到来自血 站的 O 型 Rh(D) 抗原阴性献血员标本 20 例,挑选 O 型 Rh(D) 抗原阳性献血员标本 20 例,每例 2 mL 全血。每份 标本中加入的 IgG 型抗 D 试剂 400 μL,轻轻混匀,室温 放置 20 min,1 000 g 条件下离心 3 min。然后使用两种抗 球蛋白检测卡手工加样进行试验。Scan 卡(包含单抗 IgG、 单抗 C3d、多特异度 IgG&C3d)和 Coombs 卡(只含有多 特异度抗 IgG&C3d)。
1.3.2 设计三组试验,筛选制作阳性质控品时最佳致敏条 件 (IgG 型抗 D 试剂的最适加入量、最适反应温度、最 适反应时间)
1.3.2.1 IgG 型抗 D 试剂最适加入量试验 挑选 Rh(D) 抗 原阳性标本 20 例,每例 2 mL 全血。把每例 2 mL 全血平 均分为 10 份,每份 0.2 mL。室温条件下,在每份 0.2 mL 标本中顺序加入 IgG 型抗 D 试剂 5 μL、10 μL、12.5 μL、 15 μL、20 μL 、25 μL 、30 μL、35 μL、40 μL、45μL;相当于 每 2.0 mL 标本对应加入 IgG 型抗 D 试剂 50 μL、100 μL、 125 μL、150 μL、200 μL 、250 μL 、300 μL、350 μL、400 μL、 450 μL。然后轻轻混匀,放置 20 min。1 000 g 条件下离心3 min。由于标本量较少,然后使用 Coombs 卡手工加样进 行试验。
1.3.2.2 IgG 型抗 D 试剂最适反应温度选择试验 挑选 Rh(D) 抗原阳性标本 20 例,对每份标本留取 3 mL,再 各自平均分为 3 份,每份 1.0 mL。把 20 例标本的 3 份样 本,分别放置在 4 ℃冰箱、室温(约 25 ℃ )、37 ℃温浴 条件下 1 h,然后在每份标本中各加入 IgG 型抗 D 试剂 62.5 μL(相当于每 2 mL 标本对应加入 IgG 型抗 D 试剂 125 μL)。然后轻轻混匀,维持标本所处温度条件不变, 放置 20 min。1 000 g 条件下离心 3 min。然后使用 Coombs 卡手工加样进行试验。
1.3.2.3 IgG 型抗 D 试剂最佳反应时间试验 挑选 Rh(D) 抗原阳性标本 20 例,每例 2 mL 全血。室温条件下,在 每例标本中各加入 IgG 型抗 D 试剂 125 μL。然后轻轻混 匀,1 000 g 条件下离心 3 min。为保证反应时间准确,分 别在反应时间(从加入 IgG 型抗 D 试剂算起)为 5 min、 10 min、20 min、30 min、60 min、350 min,然后使用 Coombs 卡手工加样进行试验。
1.3.3 监测质控品的稳定性 阴阳性质控品各 20 例标本 连续监测数据为北京和睦家京北妇儿医院 2018 年 5 月至 2020 年 9 月每天进行试验累计完成。使用全自动配血及 血型分析仪 [Diagnostic Grifols, S. A,国食药监械械(进) 字 2011 第 3402485 号,型号:WADiana Compact GRIFOLS Compact,Coombs 卡 ],进行 DAT 阴阳性质控检测。 1.3.3.1 监测阴性质控品的稳定性 累计挑选 2018 年 5 月 至 2020 年 9 月北京和睦家京北妇儿医院收到的来自血站 的 O 型献血员标本 20 例,每例 2.0 mL ,不添加任何试剂, 在 1 000 g 条件下离心 3min 后,保存在 2~8 ℃冰箱,作为 阴性质控品。每天用全自动配血及血型分析仪( GRIFOLS Compact)进行多特异度(抗 IgG&C3d)DAT 试验。做完 后标本立刻放入冰箱。每天进行一次试验并进行连续监 测,直到标本由于保存时间变长红细胞逐渐破坏,血浆层 由清晰的黄色转为轻微红色时继续试验,出现严重红色时 由于红细胞破碎导致出现拖尾现象时(结果 +/- )终止试 验。每次仪器做完后在阴性微孔中手工加入 1% 阳性质控 品 50 μL,离心后结果为阳性,说明阴性结果有效。
1.3.3.2 监测阳性质控品的稳定性 累计挑选 2018 年 5 月至 2020 年 9 月北京和睦家京北妇儿医院收到的来自 血站的 O 型 Rh(D) 抗原阳性标本 20 例,每例 2.0 mL。在 每例标本中分别加入的 IgG 型抗 D 试剂 125 μL,轻轻混 匀,室温放置 20 min,1 000 g 条件下离心 3 min 后,作 为阳性质控品。用全自动配血及血型分析仪( GRIFOLS Compact)进行多特异度(抗 IgG&C3d)DAT 试验。每天 进行一次试验连续监测,每次试验完毕标本放回 2~8 ℃冰 箱保存,连续监测 60 d。血浆层由清晰的黄色转为轻微红 色或加深时,仍继续试验至 60 d。
2 结果
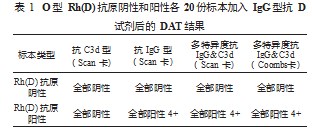
2.1 探索致敏红细胞方法的试验结果 结果分析:① 20 份 O 型 Rh(D) 抗原阴性标本,加入 IgG 型抗 D 试剂后, 所有类型的 DAT结果全部为阴性; 20 份 O 型 Rh(D) 抗原 阳性标本,加入 IgG 型抗 D 试剂后,单 IgG 型和多特异 度(抗 IgG&C3d)DAT 结果全部为阳性,单 C3d 型 DAT 结果全部为阴性,表明 IgG 型抗 D 试剂能够致敏 Rh(D) 抗原阳性的红细胞。使用 IgG 型或含有 IgG 型的直接抗 球蛋白试剂检测时,DAT 结果全部阳性。②微柱凝胶法单 抗 IgG 型与多特异度(抗 IgG&C3d)DAT 结果之间无试 验准确性和凝集强度的差异,且致敏红细胞的是 IgG 型 抗 D,与 C3d 无关。所以后续试验均采用多特异度(抗 IgG&C3d)微柱凝胶卡(即 Coombs 卡),见表 1。
表 1 O 型 Rh(D) 抗原阴性和阳性各 20 份标本加入 IgG 型抗 D2.2 设计三组试验,筛选最佳致敏条件 包括 IgG 型抗 D 试剂的最适加入量、最适反应温度、最适反应时间。
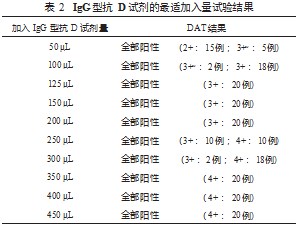
2.2.1 20 例标本,按每 2.0 mL 血标本加入 IgG 型抗 D 试 剂量计算 结果分析:参照汪德清和于洋编写的《输血相 容性检测 试验室质量控制与管理》,凝集强度为 3+ 是理想 的质控品效果 [12] 。且 IgG 抗体与 RBC 表面的蛋白抗原反 应,虽然不像 IgM 抗体那样直接导致 RBC 凝集,但是当 抗体黏附于细胞时,RBC 细胞膜发生物理性改变,可导致 阳离子渗透性异常,破坏 RBC 稳定性 [6] 。所以制备凝集 强度 3+ 的阳性质控品时, 微柱凝胶法每 2 mL 全血标本加 入 IgG 型抗 D 试剂最适当加入量选择 125 μL,见表 2。
2.2.2 选择最适反应温度的试验结果 20 例标本,在 4 ℃ 冰箱、室温(约 25 ℃ )、37 ℃温浴条件下, 结果都是 3+, 无差异。虽然 IgG 属于温抗体,最适反应条件为 37 ℃。
但该试验的结果表明: 3 种温度下,反应 20 min,制作的 阳性质控品结果无差异。因此,为了方便,可以在室温条 件下制作质控品,且使用前不需要先恢复至室温。质控品 使用后要及时放回 4 ℃冰箱保存。这样可降低细菌污染概 率,利于长期保存使用。
2.2.3 选择最适最佳反应时间试验结果 20 例标本, 加 入 IgG 型抗 D 试剂 5min 后,出现 5 例 3+w、15 例 3+ 三种 结果,可见并不稳定。加入 IgG 型抗 D 试剂 10 min 及以 后,10 例标本 DAT 结果均为 3+,试验结果能够达到比较 稳定的状态。为了保证反应效果更加充分,在制作阳性质 控品时,选择最佳反应时间为 20 min。
2.3 监测质控品的稳定性
2.3.1 阴性质控品的稳定性 20 例阴性质控品标本,DAT 结果从阴性到由于红细胞逐渐破坏而出现拖尾现象,都 分布在 50~60 d 内。阴性标本结果能够稳定 50d 以上。有 12 例标本在 45 d 时标本上部血浆层出现轻微红色, 但并 不影响试验结果 [13] 。当出现严重红色时,说明红细胞破 坏严重,结果出现拖尾现象后,不能继续使用。
2.3.2 阳性质控品的稳定性 20 例阳性质控品标本, 为 期 60 d 的连续监测 DAT 结果,红细胞凝集强度都是 3+。 说明 DAT 阳性质控结果在 60 d 内稳定性良好。有 10 例 标本大约在 45 d 时标本上部血浆层开始出现轻微红色, 但并不影响试验结果 [13] 。有 4 例标本在 50 d 时转至红色, 直到 60 d 试验结束,试验结果都是 3+ ,结果未受影响。
3 讨论
微柱凝胶试验明显不同于传统的试管法检测技术,微 柱凝胶试验提供了一个清晰的凝集强度判断标准,各凝集 强度之间可用肉眼鉴别, 操作标准化, 重复性好, 试验结果 清晰、稳定、客观,并可对结果进行拍照,存入计算机, 作为资料保存。而传统的试管法,凝集强度的判定不易掌 握,受主观因素影响较大,试验结果重复性不理想,且结 果不可保存;微柱凝胶法不需洗涤受检细胞,敏感度高,对致敏红细胞检出率大大提高 [14],所以微柱凝胶法应用广 泛。为了保证微柱凝胶试验的准确性,质控品的使用是十 分必要的。
IgG 型抗体一般在体温条件下与 RBC 表面的蛋白抗原 反应, 因此, 将其称为“温凝集素”,IgG 型抗体很少直接 导致 RBC 凝集。 IgG 型抗体引起的 AIHA 原理比较复杂, 简单描述如下: IgG 分子可能与 RBC 表面的抗原和细胞 毒细胞上的 Fc 受体结合。通过免疫黏附(尤其是IgG-FcR 介导的免疫黏附)可刺激一系列反应,导致吞噬作用,但 发生反应需较长时间的相互作用。免疫黏附导致的吞噬作 用可完全吞食靶 RBC, 通过内部的吞噬体破坏 RBC。然 而,这种吞噬常为部分吞噬,导致 RBC 的表面积 - 体积 比降低,使其变为球形红细胞。球形红细胞(由于其可变 形性降低)无法穿过脾血窦壁上的小裂孔,因此在脾脏的 Billroth 索中破坏 [6]。血辫中的血为离开人体后的血液, 不 像人体中的血能在不断循环流动,所以被免疫黏附吞噬的 几率很小, 只是结合了 IgG 抗体, 而不引起破坏;另外, 也不会再经过脾脏,所以能够被完整地保存下来,只呈现 致敏的状态。所以制作的阳性质控品中与 IgG 型抗体结合 的红细胞可以保存较长的时间。
试验所用血液标本来自血站的血袋小辫,为带有保养 液的全血标本。原因及注意事项如下:①标本容易得到, 利用悬浮红细胞发出后的血袋剩余血辫标本就可完成; ②作为献血员标本,在血站对传染病项目已做过双重检测, 可最大限度的保证其制作和使用安全 [15]; ③另外血站对献 血员做过贫血筛查,基本能够保证标本为正常的红细胞和 血浆比例;④献血员全血标本中已经有适量的枸橼酸盐抗 凝剂,磷酸盐缓冲液,为红细胞提供能量物质的葡萄糖和 腺嘌呤等物质,有利于质控品的长期保存;⑤为减少细菌 污染,标本保存在带帽的洁净无添加试管中;⑥对标本进 行多特异度(抗 IgG&C3d) DAT 筛查试验,结果为阴性 者,可以使用;阳性者不能使用。因为据统计,在正常献 血者中, Coombs 试验的阳性率为 1 ︰ 36 000~1 ︰ 1 000[6] 。 另外, 如果 C3 也沉积于 RBC 表面, 那么 IgG 抗体可固定 补体, 可加速标本溶血 [6]。也有文献报道献血员 DAT 阳性 率为 0.008%[16]。
综合以上试验及分析, 得出适用于微住凝胶法 IgG 型 直接抗球蛋白试验质控品制作的步骤及注意事项:①选择 标本: 按照上文提到的试验标本筛选方法(来自血站 O 型 悬浮红细胞血袋的血辫 10 d 内全血标本,无溶血、无异 常凝集、多特异度 DAT筛查结果阴性) ; Rh(D) 抗原阳性 的标本均为正常 D。非正常 D 抗原阳性标本不建议使用。 ②制作步骤:各试验室可根据需要选择是否配制阴性质控 品。阴性质控品, 选择 Rh(D) 抗原阳性或阴性的标本, 留取 2 mL 标本保存在带帽的无添加试管中。 1 000 g 条件下 离心 3 min。阳性质控品,选择 Rh(D) 抗原阳性标本,留 取 2 mL 标本保存在带帽的无添加试管中。加入 IgG 型抗 D 试剂 125 μL,混匀,室温放置 20 min 。1 000 g 条件下 离心 3 min。③制作完成后,使用常规检测方法连续检测 3 次来确定相关靶值 [12] :阴性质控红细胞凝集强度为 0, 阳性质控红细胞凝集强度为 3+,且阳性质控日常使用中的 强度偏差最多为 1+。④有效期: 阴性质控品的为 45d,阳 性质控品为 60 d。而且微住凝胶法使用质控品的量很少, 如果每个月制作一次,可以满足日常工作需求。⑤质控品 手工与上自动化仪器结果无差异,离心后可以应用在自动 化仪器上,手工方法使用时需先配制成 1% 红细胞悬液。 ⑥质控品可直接应用在单抗 IgG 型 DAT 质控试验和作为 多特异度(抗 IgG&C3d) DAT 的参考质控品。⑦质控品保 存在 2~8 ℃冰箱,建议在有效期内使用。由于不受温度影 响,所以使用前不必等标本恢复到室温。每次使用前要认 真检查质控品外观,不能出现严重溶血,轻度溶血不影响 试验结果 [13]; 每次使用前不需要重复混匀和离心, 减少对 红细胞的破坏;使用后及时放回 2~8 ℃冰箱,降低细菌污 染概率,利于其长期保存使用。⑧在制作和使用质控品过 程中,要对质控标本按照具有潜在的传染物品对待。⑨各 个试剂厂家的产品结果可能存在差异。如果应用其他厂家 试剂,需要做验证试验。通过调整制作阳性质控品时 IgG 型抗 D 试剂的加入量和验证靶值后再使用。
参照汪德清和于洋编写的《输血相容性检测 试验室 质量控制与管理》,检验室制作的室内质控品保存期达到 40 d 以上 [12] 。试验室自制的质控品保存期 >40 d,稳定性 良好,所以可以满足日常使用。
在日常临床试验中, 如果需要验证 DAT 阴性结果的有 效性,把阳性质控品配制成 1% 红细胞浓度,加入到试验 结果阴性孔中离心即可。通常 DAT 只需要阳性质控品, 但 是我们对自动化仪器进行室内质控时同时设置了阴性质控 品,认为增加阴性质控也是有必要的 [17]。
通过试验室较长时间的探索和完善,所制备的质控品 可以满足日常 DAT 试验室内质控的需求。同时, 制备原料 来源途径稳定、易得,而且选择的血液采集时间较短,可 较大限度保证质控品的使用时间, 减少制备次数 [18],有助 于完善 DAT 检测试验室的室内质量控制体系, 适宜各试验 室开展。各试验室可根据需要选择是否配制阴性质控品。
参考文献
[1] 美国输血协会技术手册编委会 . 输血技术手册 [M]. 肖星甫 , 季阳 , 尚书颂 , 等译 . 北京 : 人民卫生出版社 ,1985: 497.
[2] 张勤 , 郑皆炜 , 王中英 , 等 . 抗 cE 抗体引起的迟发性溶血性输血反应病例分析 [J]. 实用检验医师杂志 , 2019, 11(4): 244-246.
[3] 王显荣 , 李育 , 许立 , 等 . 直接抗人球蛋白试验阳性的类型鉴别及临床意义 [J]. 中国实验诊断学 , 2004, 8(4): 340-341.
[4] 刘凌 , 李流娇 , 莫水群 . 微柱凝胶直接抗人球蛋白试验对自身免疫性溶血性贫血诊断的应用 [J] 中国医药 , 2012, 7(4): 426-427.
[5] 杨冬梅 , 李志坚 . 微柱凝胶试验法在新生儿溶血病直接抗人球蛋白试验检测中的应用价值 [J]. 中国药物与临床 , 2020, 20(9):1554- 1556.
[6] 中华医学会血液学分会红细胞疾病 ( 贫血)学组 . 自身免疫性溶血性贫血诊断与治疗中国专家共识 (2017 年版 )[J]. 中华血液学杂志 , 2017, 38(4): 265-267.
[7] 闫芳 , 苗天红 , 孙云 , 等 . 微柱凝胶技术对新生儿溶血病直接抗人球蛋白的检测效果 [J]. 北京医学 , 2019, 31(11): 691-692.
[8] 顾晨晨 , 曹敏凤 , 戎瑞明 , 等 . 全自动微柱凝胶法用于直接抗人球蛋白试验初筛的临床观察 [J]. 中国临床医学 , 2019, 26(6): 896-899.
[9] 临床输血规范流程协作组 . 输血相容性试验标准检测流程 [J]. 中国输血杂志 , 2012, 25(9): 815-817.
[10] 尚红 , 王毓三 , 申子瑜 . 全国临床检验操作规程 [M]. 4 版 . 北京 :人民卫生出版社 , 2014: 128.
[11] 张静 , 刘婷婷 , 李平 . 86 例直接抗人球蛋白试验阳性病例分析 [J]. 当代医学 , 2019, 25(7): 66-69.
[12] 汪德清 , 于洋 . 输血相容性检测 实验室质量控制与管理 [M]. 北京 : 人民军医出版社 , 2011: 125- 127.
[13] 于洋 , 马春娅 , 冯倩 , 等 . 输血相容性检测室内质控品制备技术优化与性能评价 [J]. 中国输血杂志 , 2011, 24(1): 26-30.
[14] 罗广平 , 骆宏 , 汪传喜 , 等 . 凝胶直接抗球蛋白试验在自身免疫性溶血性贫血实验诊断中的应用 [J]. 热带医学杂志 , 2009, 9(7):745-768.
[15] 中华人民共和国卫生部、中国国家标准化管理委员会 . 献血者健康检查要求 : GBl8467-2011[S]. 2011.
[16] PURI V, CHHIKARA A, SHARMA G, et al. Critical evaluation ofdonor direct antiglobulin test positivity: Implications in crossmatching and lessons learnt[J]. Asian J Transfus Sci, 2019, 13(1):70-72.
[17] 于洋 , 汪德清 . 输血相容性检测室内质量控制体系建设 [J]. 中国输血杂志 , 2009, 22(10): 790-792.
[18] 汪维 . 输血相容性检测室内质控品自制及应用探讨 [J]. 临床输血与检验 , 2016, 18(4): 389-393.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/48203.html