SCI论文(www.lunwensci.com):
摘要:目的评价和验证Procleix PANTHER核酸检测系统在使用前,其检测性能和操作性能可以满足血液筛查的要求,同时也进一步验证试剂厂家提供的试剂参数能够在本实验室得到重现。方法根据IS015189和中华人民共和国卫生行业标准(WS/T)相关文件,进行检出限、仪器比对和抗干扰能力的验证。结果Procleix PANTHER核酸检测系统HBV、HCV、HIV-1 95%检出限分别为10.33IU/mL、7.09 U/mL、5.21IU/mL;Procleix PANTHER核酸检测系统与在用检测系统仪器比对结果为“通过”;脂肪血浆和溶血血浆对低浓度的HBV、HCV、HIV-1检出均无显著影响。结论新仪器Procleix PANTHER的检测性能和操作性能符合要求,可以满足血站血液筛查需求。
关键词:Procleix PANTHER;性能验证;检出限
本文引用格式:侯云,冯秋霞,张龙穆.Procleix PANTHER核酸检测系统使用前性能验证[J].世界最新医学信息文摘,2019,19(71):22-23.
Evaluation on Analysis Function of Procleix PANTHER Systems before Performing Nucleic Acid Test
HOU Yun,FENG Qiu-xia,ZHANG Long-mu
(Clinical laboratory,Shandong Qingdao blood center,Qingdao Shandong)
ABSTRACT:Objective To confirm if the detection performance and operation performance of the Procleix PANTHER nucleic acid test system can meet the requirements of blood screening before the system is implemented in laboratory,At the same time,the reagent parameters provided by the reagent manufacturer can be reproduced in the laboratory.Methods According to the ISO15189,the People’s Republic of China health industry standard(WS/T),detection limit,instrument comparison and anti-interference capability were tested.Results In the Procleix PANTHER nucleic acid detection system,the detection limits of HBV,HCV and HIV-1 95%were 10.33IU/mL,7.09 U/mL and 5.21IU/mL respectively.The result of Procleix PANTHER nucleic acid detection system was“pass”compared with the instrument of the detection system.Fat plasma and hemolytic plasma had no significant effect on HBV,HCV and HIV-1 detection at low concentrations.Conclusion The detection performance and operation performance of the new instrument Procleix PANTHER meet the requirements and can meet the needs of blood screening in blood stations.
KEY WORDS:Procleix PANTHER systems;Performance verification;Detection limits
0引言
按《血站质量管理规范》、《血站实验室质量管理规范》、《血站技术操作规程(2015版)》的要求,血液检测大型关键性设备在投入正式使用前需进行设备确认[1]。近年来,血液筛查核酸检测在血液制品行业和血站血液筛查领域全面展开,目前我站在运行的核酸检测设备主要有Roche s 201系统和Procleix TIGRIS系统,已通过使用前的设备确认运行稳定。为满足血液核酸检测需要我站新引进Procleix PANTHER核酸检测系统,本文就Procleix PANTHER核酸检测仪器的使用前确认方法进行探讨,确认该系统在本实验室、本地区的适用性,确保其高效率、高质量、平稳、有序的完成常规NAT检测工作。
1材料与方法
1.1标本来源
1.1.1阴性试验标本
对献血者全血标本进行血清学检测和Procleix TIGRIS试剂单检模式检测,将检测结果呈HBsAg、抗-HCV、抗-HIV、HBV DNA、HCV RNA、HIV-1 RNA阴性的标本进行汇集,作为试验用阴性血浆。
1.1.2阳性试验标本
采用血液病毒核酸检测HBV DNA质控品(浓度:100IU/mL,批号201701001)、HCV RNA质控品(浓度:500 IU/mL,批号201701001)HIV-1 RNA质控品(浓度:100 IU/mL,批号201701001),均为北京康彻思坦公司生产,作为阳性试验标本。
1.1.3其它标本
脂血标本来源于因脂血报废的正常人血浆,血清学及核酸检测结果均呈阴性,经仪器测定TG约6mmol/L为重度脂血标本,TG约2mmol/L为轻度脂血标本。溶血标本来源于不足量报废的血液标本在-80℃下冷冻8min制得,血清学及核酸检测结果均呈阴性,依据厂家提供的参数选取血红蛋白5g/L为轻度溶血标本,血红蛋白10g/L为重度溶血标本。
1.2仪器与试剂
Procleix PANTHER全自动核酸检测分析仪、Procleix TIGRIS全自动核酸检测分析仪。Procleix Ultrio Elite Assay试剂盒(美国Grifols公司,批号:167043),Procleix Ultrio Plus Assay(美国Grifols公司,批号:183363)。
1.3方法
1.3.1检出限验证
将病毒检测质控品用阴性血浆进行梯度稀释,HBV浓度稀释为:50IU/mL、25 IU/mL、12.5 IU/mL、8.33IU/mL、6.25IU/mL;HCV浓度稀释为18.33IU/mL、9.16IU/mL、4.58 IU/mL、2.29IU/mL、1.72IU/mL;HIV-1浓度稀释为25IU/mL、16.67 IU/mL、8.33 IU/mL、4.17IU/mL、2.08 IU/mL。每个标本重复检测10次,使用统计软件分析该系统对HBV、HCV、HIV-1的95%检测限及置信区间。
1.3.2仪器比对
选取10份阴性标本、10份阳性标本(至少含弱阳性5份、强阳性1份)。标本的阴阳性尽可能随机排列。同一个操作者在两台核酸检测全自动系统进行检测,比较这些样本在两台仪器上得到的实验结果。
1.3.3干扰实验
将已知低浓度的HBV、HCV、HIV-1阳性质控品按照一定比例分别加入到脂血血浆(TG=2mmol/L,TG=6mmol/L),溶血血浆(FHb=5g/L,FHb=10g/L)和正常阴性血浆中,使HBV、HCV、HIV-1质控品在血浆中终浓度分别为:40 IU/mL、12 IU/mL、20 IU/mL,使用Procleix PANTHER系统检测这些样本,每个样本重复20次,验证该系统的抗干扰能力。
1.3.4统计方法
使用SPSS 19.0软件进行Probit回归分析,计算该系统HBV、HCV、HIV-1的95%检测限及置信区间。采用卡方检验比较脂肪血浆、溶血血浆和正常血浆检出率的差别,P<0.05为差异有统计学意义。
2结果
2.1检出限验证结果
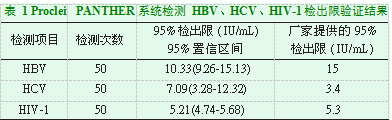
HBV、HCV、HIV-1 95%检出限分别为10.33IU/mL、7.09 U/mL、5.21IU/mL,其中HBV、HIV-1 95%检出限低于厂家提供的检出限,而HCV 95%检出限高于厂家提供的检出限(表1)。
2.2仪器比对结果
两台仪器检测的同一样本若同为阴性或阳性,则判断为一致,若一阴一阳,则判断为不一致,试验结果的一致性应≥80%。本实验同一样本结果的一致性为100%,判断为一致,则判定该仪器比对结果为“通过”。
2.3抗干扰能力结果
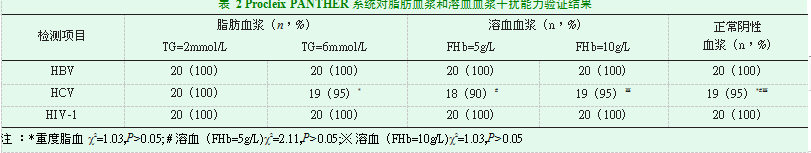
在重度脂肪血浆(TG=6mmol/L)和溶血血浆(FHb=5g/L,10g/L)中HCV的检出率较低,分别为95%、90%和95%,与正常阴性血浆检出率(95%)比较,差异无统计学意义(2值分别为1.03、2.11和1.03,P值均>0.05)。在脂肪血浆、溶血血浆及正常阴性血浆中HBV、HIV-1检出率均为100%,脂肪血浆和溶血血浆对低浓度的HBV、HCV、HIV-1检出均无影响(表2)。
3讨论
自2010年血站核酸检测试点工作开展以来,全自动化的核酸检测系统在采供血机构中大量运用,实验室人员希望借此提高血液检测的准确性、高效性、和安全性[2]。根据规定新的或者经过维修后,可能影响检测结果的关键设备在正常使用之前应经过确认。参照我们之前的TIGRIS核酸检测系统性能验证方案,通过检出限,仪器比对和抗干扰能力等参数来确认新仪器的检测性能和操作性能。
检出限的确认,检出限为系统能检测到的分析物的最小含量或最低浓度。目前验证方法有两种,一种是选用卫生部临床检验中心或者有资质生产企业等部门生产的室内质控品进行倍比稀释(如稀释到原浓度的2、4、6、8、12、16倍…)后进行检测,每个标本重复检测20次以上,使用统计软件分析核酸试剂对HBV、HCV、HIV-1的95%检出限。另一种是选用有资质生产企业等部门生产的血清盘,重复检测后使用统计软件分析核酸试剂对HBV、HCV、HIV-1的95%检出限。这也是目前进行核酸检测验证检出限的通用方法[3]。本验证实验将病毒检测质控品进行梯度稀释,根据检测结果选取出现反应性和非反应性浓度范围之内的五个浓度倍数,进行重复10次检测统计分析该系统对HBV、HCV、HIV-1的95%检出限。该验证方法可以一定程度上避免试剂的浪费,同时可以得到95%最低检测限数值,使其与厂家提供的数值有可比性。结果显示该系统HBV、HCV、HIV-1检出限分别为10.33IU/mL、7.09 U/mL、5.21IU/mL,其中HBV、HIV-195%检出限低于厂家提供的检出限,而HCV95%检出限高于厂家提供的检出限,但是达到了FDA对NAT血液筛查HBV(100 IU/mL)、HCV(100 IU/mL)、HIV(100 copies/mL)分析灵敏度要求(单人模式检测)[4]。造成这种现象的原因可能有两点:一是可能由于验证方法的差异所致,厂家进行检出限确认时每个浓度的标本进行了183次的单人模式检测,而在我们的验证中只进行了50次检测,因此得到的95%检测限会有所偏差。二是检测试剂由厂家进行检出限确认时使用的是HCVWHO标(06/100),而我们所用的是有资质的生产企业生产的室内质控品。这种因为样本和样本数量的不同引起的偏差在其他研究者验证检出限时也有类似的情况[5]。仪器比对是为了确认新进Procleix PANTHER核酸检测系统与实验室原有核酸检测分析系统对同一项目的检验结果具有可比性。本实验根据新进设备的单检模式,选用与其检测模式一致的Procleix TIGRIS核酸检测系统进行比对,在阳性样本选择时至少选择5份弱阳性标本,即为检出限3-5倍浓度的阳性标本,以比较仪器之间对低浓度标本的检测一致性,结果显示两台仪器比对结果一致。
抗干扰能力验证,本实验结果显示脂肪血浆、溶血血浆对Procleix PANTHER核酸检测系统的检测能力没有显著影响,该结果与厂家的研究结果一致,与姚凤兰对Procleix Ultrio Assay核酸检测系统的研究结果一致[5]。
本实验根据既有核酸检测仪器Procleix TIGRIS检测系统性能验证方案,从检出限、仪器比对和抗干扰能力等参数来确认新仪器Procleix PANTHER的操作性能和检测性能,结果显示均符合要求,满足血站血液筛查需求。
参考文献
[1]中华人民共和国国家卫生和计划生育委员会.血站技术操作规程(2015版),2015-12.
[2]Roth W K,Busch M P,Schuller A,et al.International survey on NAT testing of blood donations:expanding implementation and yield from 1999 to 2009[J].Vox Sang,2012,102:82-90.
[3]Enjalbert F,Krysztof DE,Candotti D,et al.Comparison of seven hepatitis B virus(HBV)nucleic acid testing assays in selected samples with discrepant HBV marker results from United States blood donors[J].Transfusion,2014,57(10):2485-2495.
[4]US Food and Drug Administration.Draft guidance for industry:nucleic acid testing(NAT)for human immunodeficiency virus type 1(HIV-1)and hepatitis C virus(HCV):testing,product disposition,and donor deferral and reentry,2010-05.
[5]姚凤兰,汪德海,查祎,等.Procleix TIGRIS核酸检测系统分析性能及操作性能确认研究[J].中国输血杂志,2014,27(4):361-367.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/19961.html