SCI论文(www.lunwensci.com):
摘要:目的探讨复方斑蝥胶囊联合替莫唑胺胶囊治疗高级别胶质瘤的临床疗效。方法回顾性分析65例高级别胶质瘤术后放疗后的临床资料。结果依据治疗方法的不同,分为复方斑蝥胶囊联合TMZ组和TMZ组,复方斑蝥胶囊联合TMZ组的临床疾病控制率79.42%,高于TMZ组的疾病控制率61.29%,差异具有统计学意义(P<0.05)。治疗后两组KPS评分均有所提高,且复方斑蝥胶囊联合TMZ组KPS评分显著高于TMZ组,差异具有统计学意义(P<0.05)。复方斑蝥胶囊联合TMZ组在轻度骨髓抑制方面低于TMZ组,两组差异具有统计学意义(P<0.05)。两组在胃肠道不良反应方面差异无统计学意义(P>0.05)。结论复方斑蝥胶囊联合替莫唑胺胶囊具有较好的临床疗效,明显改善患者生活质量,减轻替莫唑胺对骨髓的抑制作用,具有一定的临床推广价值。
关键词:复方斑蝥胶囊;替莫唑胺;高级别胶质瘤
本文引用格式:王金静,赵林.复方斑蝥胶囊联合替莫唑胺治疗高级别胶质瘤术后放疗后的临床疗效[J].世界最新医学信息文摘,2019,19(63):
0引言
胶质瘤是中枢神经系统最常见的原发性肿瘤,起源于神经上皮组织,约占颅内肿瘤的40%-50%[1]。胶质瘤包括星形细胞肿瘤、少突角质细胞肿瘤、混合型胶质细胞肿瘤和室管膜肿瘤[2],依据世界卫生(WHO)将胶质瘤分为I-IV四个等级,WHOI-II属于低级别胶质瘤,一般手术切除后,预后较好,WHIII-WHO IV,属于高级别胶质瘤,包括弥漫性星形细胞瘤、胶质母细胞瘤、部分室管膜肿瘤等,预后较差[3]。据一项在瑞士的人口调查,胶质母细胞瘤的1年生存期只有17%左右[1]。现在高级别胶质瘤常规治疗方案为尽可能的手术切除,术后放疗,辅助替莫唑胺(TMZ)化疗。虽然联合运用,但患者预后仍然较差,并伴随一些副作用,如患者术后脑出血,放射性脑水肿,严重的骨髓抑制等。复方胶质瘤具有抗肿瘤、提高机体免疫力的作用[4],对肺癌[5]、胃癌[6]、卵巢癌[7]等具有明显的抑制作用。因此,本文回顾性分析65例复方斑蝥胶囊在胶质瘤方面的临床资料。
1资料与方法
1.1一般资料
选取2017年01月至2018年02月在山东省立医院收治的65例胶质瘤的患者,依据治疗方法分为的不同分为复方斑蝥联合TMZ组和TMZ组。所有患者均符合王忠诚主编的《神经外科学》[8]中胶质瘤诊断标准。
1.1.1纳入标准
(1)所有患者均是高级别胶质瘤患者术后,病理分级为WHOⅢ-IV级;
(2)所有患者均完成术后的辅助放疗;
(3)KPS评分均不低于60分,预期生存期大于6个月;
(4)排除化疗禁忌症、不合并心衰、肾衰等其他疾病者;
(5)患者及家属知情同意并自愿签知情同意书者。
1.1.2排除标准
(1)胶质瘤患者术后病理为WHO I-II级;
(2)胶质瘤患者术后没有进行放疗治疗者,或放射治疗中途放射者;
(3)KPS评分低于60分;
(4)患有精神疾病或妊娠期妇女,或合并心衰、肾衰其他疾病者;
(5)中途自行停药或经济原因等依从性差的患者。
1.2药物与治疗方法
复方斑蝥胶囊由贵州益佰制药股份有限公司生产,规格0.25g/粒;替莫唑胺(蒂清)由江苏天士力帝药业有限公司生产,规格50mg/粒。28天为一个治疗周期,共进行6周期。
TMZ组:早晨空腹服用TMZ,连续口服5天,间隔23天,第一周期剂量为150mg/m2/d,若患者中性粒细胞数超过3×109个/L、血小板计数超过100×109个/L,第2个周期剂量可加至200mg/m2/d,任一周期内,若中性粒细胞计数少于3×109个/L,替莫唑胺剂量减少为50mg/m2/d,但替莫唑胺最小剂量不得低于100mg/m2/d。
复方斑蝥胶囊联合TMZ组在TMZ组基础上口服复方斑蝥胶囊,一天2次,每次3粒,化疗间歇期继续口服复方斑蝥胶囊。
1.3分组
将入选患者依据随机数字表法分为复方斑蝥胶囊联合TMZ组(n=34)和TMZ组(n=31)。复方斑蝥胶囊联合TMZ组34例患者,男性23例,女性11例,年龄34-71岁,平均51.9±14岁,病理WHOⅢ级19例,WHOⅣ级15例,全切除21例,部分或近全切13例;TMZ组共31例患者,男性19例,女性12例,年龄31-69岁,平均51.2±11.3岁,病理WHOⅢ级17例,WHOⅣ级14例,全切除19例,部分或近全切12例。两组患者在性别、年龄、病理类型等一般资料比较差异无统计学意义,具有可比性。
1.4观察指标
1.4.1临床疗效评判[9]
将定期复查颅脑MRI或颅脑CT(平扫+增强)的结果与治疗前进行对比。完全缓解(CR):占位病灶完全消失,且持续时间超过四周;部分缓解(PR):病灶缩小超过30%,且维持四周以上;稳定(SD):病灶缩小不到30%或增大不超过20%,无新发病灶;疾病进展(PD):病灶增大超过20%,或有新发病灶,或临床症状恶化。客观有效率(ORR)=(CR+PR)/总例数X 100%,控制率(CBR)=(CR+PR+SD)/总例数×100%。
1.4.2生活质量评估KPS评分(Karnofsky评分)
将高级别胶质瘤患者治疗前后的KPS评分对比。治疗后KPS评分高于治疗前10分为生活质量改善;低于治疗前10分为生活质量下降,波动在10分之内为生活质量稳定。
1.4.3骨髓抑制、肝肾毒性
定期复查血常规、肝功、肾功,观察两组治疗前后白细胞下降、血小板减少、贫血、肌酐、转氨酶情况。
1.4.4胃肠道反应
观察两组恶心、呕吐等胃肠道反应情况。
1.5统计分析
所有数据资料采用SPSS 20.0统计软件进行分析。计数资料采用2检验,计量资料用(±s)表示,采用t检验,以P<0.05差异具有统计学意义。
2结果
2.1临床疗效
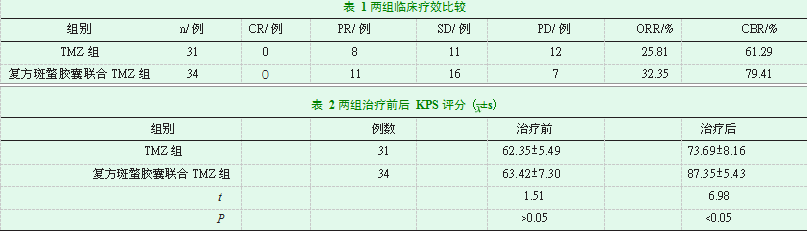
TMZ组PR8例,SD11例,PD12例,客观有效率为25.81%,疾病控制率为61.29%,复方斑蝥胶囊联合TMZ组PR11例,SD16例,PD7例,客观有效率32.35%,疾病控制率79.42%,两组临床疗效比较,具有统计学意义(P<0.05),见表1。
2.2生活质量评估KPS评分
两组治疗前KPS评分无显著性差异,治疗后两组均有所提高,且复方斑蝥胶囊联合TMZ组KPS评分显著高于TMZ组,差异具有统计学意义(P<0.05),见表2。
2.3骨髓抑制、肝肾毒性
TMZ组出现11例轻度骨髓抑制,复方斑蝥胶囊联合TMZ组出现8例轻度骨髓抑制,两组均无出现严重的肝肾毒性,TMZ组骨髓抑制率35.48%,复方斑蝥胶囊联合TMZ组轻度骨髓抑制率23.53%,两组差异具有统计学意义(P<0.05)。
2.4胃肠道反应
TMZ组出现13例恶心呕吐,复方斑蝥胶囊联合TMZ组出现15例恶心呕吐,TMZ组骨髓抑制率41.93%,复方斑蝥胶囊联合TMZ组轻度骨髓抑制率44.12%,两组差异无统计学意义(P>0.05)。
3讨论
胶质瘤为神经系统最常见的原发性肿瘤,高级别胶质瘤具有高发病率、高死亡率、高复发率,低治愈率的特点,造成预后较差[10]。高级别胶质瘤易在肿瘤原发灶2cm范围内浸润性生长,外加血脑屏障,给治疗带来一定困难[11]。现在高级别胶质瘤治疗的金标准是手术尽可能的全切除后放疗,辅助化疗,能延长患者的无进展生存期。
替莫唑胺(TMZ)是新型的第二代烷化剂,口服易吸收,能通过血脑屏障,生物利用度高,是治疗高级别胶质瘤术后辅助化疗的常用药[12]。复方斑蝥胶囊是具有活血化瘀、攻毒蚀疮的中成药,由斑蝥、三棱、半枝莲、人参、黄芪、刺五加、山茱萸、熊胆粉等组成。研究表明,中药斑蝥中含有斑蝥素,具有抗肿瘤的作用[13,14],人参、黄芪具有抗肿瘤、提高机体免疫力的作用[15,16],符合中医扶正祛邪理论。广泛运用在肺癌、肝癌、消化道肿瘤等方面[17-21],在中枢神经系统肿瘤中尚缺乏研究。
本研究结果显示中,复方斑蝥胶囊联合TMZ组的临床疾病控制率79.42%,高于TMZ组的疾病控制率61.29%,差异具有统计学意义(P<0.05)。治疗后两组KPS评分均有所提高,且复方斑蝥胶囊联合TMZ组KPS评分显著高于TMZ组,差异具有统计学意义(P<0.05)。复方斑蝥胶囊联合TMZ组在轻度骨髓抑制方面低于TMZ组,两组差异具有统计学意义(P<0.05)。两组在胃肠道不良反应方面差异无统计学意义(P>0.05)。
综上所述,复方斑蝥胶囊联合替莫唑胺具有较好的临床疗效,明显改善患者生活质量,减轻替莫唑胺对骨髓的抑制作用,具有一定的临床推广价值。由于本样本数量较少,观察周期时间较短,未对患者进行长期随访,需要大样本随机、对照、双盲实验进一步研究证实。
参考文献
[1]Ostrom Q T,Gittleman H,Liao P,et al.CBTRUS statistical report:primary brain and central nervous system tumors diagnosed in the United States in 2007-2011[J].Neuro-oncology,2014,16Suppl4(iv1-63.
[2]段国升.脑胶质瘤临床治疗的进展[J].中华神经外科杂志,2004,(02):9-11.
[3]Louis D N,Perry A,Reifenberger G,et al.The 2016 World Health Organization Classification of Tumors of the Central Nervous System:a summary[J].Acta neuropathologica,2016,131(6):803-20.
[4]夏恪迪,张赢予,张馨木,等.复方斑蝥胶囊体内抗肿瘤作用的实验研究[J].中国药业,2007,(15):13-4.
[5]宋展,周丽荣,王晓晟,等.复方斑蝥胶囊联合奥沙利铂治疗非小细胞肺癌的疗效观察[J].现代药物与临床,2019,34(05):1525-8.
[6]李莹,王季堃,李巍.复方斑蝥胶囊联合化疗治疗老年晚期胃癌的疗效观察[J].中国实用医药,2017,12(10):115-7.
[7]田静,刘乐佳,王莉.复方斑蝥胶囊联合DP方案治疗晚期卵巢癌的疗效观察[J].现代药物与临床,2018,33(08):2050-4.
[8]王忠诚.神经外科学[M].北京:科学出版社,2000.
[9]Watanabe H,Okada M,Kaji Y,et al.[New response evaluation criteria in solid tumours-revised RECIST guideline(version 1.1)[J].Gan to kagaku ryoho Cancer&chemotherapy,2009,36(13):2495-501.
[10]Sathornsumetee S,Rich J N,Reardon D A.Diagnosis and treatment of high-grade astrocytoma[J].Neurologic clinics,2007,25(4):1111-39.
[11]赵艳红,徐保锋,游洪,等.高度恶性胶质瘤治疗的研究进展[J].癌症进展,2019,17(09):1008-10.
[12]Yung W K.Temozolomide in malignant gliomas[J].Seminars in oncology,2000,27(3 Suppl 6):27-34.
[13]Yu M,Zhao Y.Cantharis by photosynthetic bacteria biotransformation:Reduced toxicity and improved antitumor efficacy[J].Journal of ethnopharmacology,2016,186(151):8.
[14]Yang X,Tong J,Guo L,et al.Bundling potent natural toxin cantharidin within platinum(IV)prodrugs for liposome drug delivery and effective malignant neuroblastoma treatment[J].Nanomedicine:nanotechnology,biology,and medicine,2017,13(1):287-96.
[15]张蔷,高文远,满淑丽.黄芪中有效成分药理活性的研究进展[J].中国中药杂志,2012,37(21):3203-7.
[16]黎阳,张铁军,刘素香,等.人参化学成分和药理研究进展[J].中草药,2009,40(01):164-6.
[17]谭扬,赵福友,吴穷.复方斑蝥胶囊联合化疗治疗老年晚期胃癌的疗效[J].重庆医学,2013,42(04):393-5.
[18]李兆元,宁四清,易铁男,等.复方斑蝥胶囊联合化疗及放疗治疗中晚期原发性肝癌的疗效观察[J].中华全科医学,2013,11(08):1250-1.
[19]金冰.复方斑蝥胶囊联合手术治疗早期非小细胞肺癌的临床疗效[J].中药药理与临床,2015,31(06):186-8.
[20]陈军,陈典.复方斑蝥胶囊联合三维适形放疗治疗中晚期原发性肝癌临床观察[J].现代肿瘤医学,2012,20(01):114-6.
[21]车建华,颜永清,劳小芳.复方斑蝥胶囊联合FOLFOX4方案对晚期消化道恶性肿瘤患者免疫功能及生活质量的影响[J].中国实验方剂学杂志,2013,19(16):312-5.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网! 文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/17870.html