摘要:为解决工业酸性废水处理难题,研究了氢氧化钙与电石渣在酸性废水处理中的效能,对比了两者对废水中铁离子与锰离子的去除效率。实验表明,在相同投加量及反应时长下,电石渣展现出更优的效果。使用1.4 g/L的电石渣相比同等浓度的氢氧化钙,能更高效地降低废水中铁、锰离子浓度。电石渣在短时间内迅速提升废水pH值,还着高效的去除能力和稳定性,验证了电石渣的环保价值,促进了工业废弃物的资源化利用。
关键词:电石渣,Ca(OH)2,酸性废水,去除效率
0引言
在工业加工过程中,往往会产生大量酸性废水,其中富含铁锰等重金属离子。这些废水如果直接排放会对环境造成严重的污染。为了解决这个问题,选择合适的中和材料来调节废水的酸碱度并有效去除铁锰离子显得尤为重要。高浓度的铁锰离子会严重影响水体的色度,并破坏河道两岸的生态环境,影响周边土壤肥力[1]。因此,需要一种高效、稳定的处理方法将酸性废水中高浓度的铁锰金属离子去除。目前,处理酸性废水的方法有很多,包括自然生态处理法、中和法、接触氧化法等[2]。其中,自然生态处理法是通过模拟自然界中生态系统的运作方式,利用微生物和植物等生物体对废水进行处理,达到净化的效果。中和法是通过加入碱性物质来中和废水中的酸性物质,使pH值达到中性或接近中性的水平。接触氧化法是通过向废水中通入氧气或空气,使铁锰离子与氧气发生化学反应生成沉淀物而被去除。
1实验材料分析
氢氧化钙是一种广泛使用的中和剂,它具有强碱性、成本低廉并且容易获得的特性。因此,成为了传统上用于调节酸性废水酸碱度的首选材料。其强碱性特质使其能够快速中和酸性废水,提高废水的pH值,为后续的金属离子沉淀过程提供有利的环境条件。在废水处理工艺中,氢氧化钙的应用主要基于其与酸反应时释放的大量氢氧根离子(OH-)。能与废水中的重金属离子反应生成难溶性的氢氧化物沉淀,从而实现重金属离子的有效去除[3]。
随着工业废弃物资源化利用理念的兴起,研究人员发现电解工业副产品—电石渣,其内含超过50%的氧化钙成分[4]。电石渣在溶解于水后展现出强烈的碱性特性,与氢氧化钙相似。但是它的颗粒高度分散,拥有较大的比表面积,其溶解过程迅速而高效。当电石渣与酸性废水接触时,其中的氧化钙会迅速溶解并与酸性物质发生中和反应,去除铁锰离子[5]。电石渣的使用还可以促进工业废弃物的资源化利用,减少对自然资源的消耗,并降低废物处理的成本。
2实验与分析
2.1 Ca(OH)2用量对溶液pH和铁锰离子率的影响
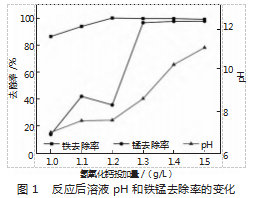
在已调节至酸性的废水处理实验中,采用不同浓度的氢氧化钙作为中和剂,具体质量浓度分别为1.0、1.1、1.2、1.3、1.1、1.5 g/L。为了确保反应物能够充分接触并避免生成的沉淀物沉降,过程中使用了一台机械搅拌器,设定转速为100 r/min,持续搅拌了60 min。经过充分反应后,记录了不同Ca(OH)2投加量对原酸性废水pH值的影响,测量不同投加量下铁离子和锰离子的去除效率。如图1所示,不同的Ca(OH)2投加量反应的废水pH值的变化趋势,还对比了不同投加量下铁锰元素的去除效果。
通过对图1数据的分析,观察到酸性废水处理过程中,氢氧化钙的投加量与废水pH值之间存在显著的正相关关系。验证了Ca(OH)2在中和酸性废水中的效果,其溶解后释放的大量氢氧根离子(OH-)与废水中的氢离子(H+)反应,导致溶液pH值的显著提升。当Ca(OH)2的投加量超过1.2 g/L时,总铁的去除效率稳定维持在95%以上的水平,在此浓度范围内,Ca(OH)2不仅有效中和了废水中的酸性,还促进了Fe2+向Fe(OH)2的转化,形成的沉淀便于分离。当Ca(OH)2投加量为1.3 g/L时,锰的去除率为96%比1.2 g/L的去除率有很大的提高。原因由两个方面进行解释:首先,随着pH值的进一步升高,溶液条件变得更有利于Mn2+向Mn(OH)2的转化,当pH值接近或超过Mn2+开始沉淀的阈值(约pH 8)时,Mn(OH)2的生成速率急剧增加;其次,生成的Fe(OH)2作为沉淀物去除了Fe2+,过程中发生了絮凝,促进了Mn2+的共沉淀和去除,形成了对锰去除的协同效应。基于上述分析,并结合实际工程应用的考量,确定了1.4 g/L为最优的Ca(OH)2投加量。
2.2电石渣用量对溶液pH和铁锰离子率的影响
采用了与2.1中设定的相同浓度梯度的六组电石渣,分别将它们加入到酸性废水中,并维持反应时间60分钟。测量不同电石渣投加量下,废水pH值的变化情况和铁锰离子去除效率,如图2所示。
根据图2可知,随着电石渣投加量的递增,溶液的pH值呈现出稳步上升的现象。原因在于电石渣中富含超过60%的CaO成分,这是一种强碱性氧化物,能与水反应生成高碱性的Ca(OH)2,从而提升溶液的pH水平。因此,电石渣在去除酸性废水中高浓度铁锰金属离子的过程中,主要依赖于其内部的CaO成分,其作用机制与直接使用Ca(OH)2去除铁锰离子的过程相似。电石渣中还含有微量的Al2O3、MgO等金属氧化物杂质,这些杂质在溶解于水后,会进一步与溶液中的OH-离子结合,形成Al(OH)3和Mg(OH)2等絮凝体。因此,除了CaO的直接作用外,电石渣中少量的Al(OH)3和Mg(OH)2也通过其絮凝作用,使废水中铁锰离子去除得到提高。当电石渣投加量在1.2 g/L至1.5 g/L范围内时,对总铁的去除率较低影响,而投加量为1.4 g/L时,对总锰的去除效果达到了最佳。综合考虑去除效率与成本效益,我们选择1.4 g/L作为电石渣的最佳投加量,在此条件下,废水中铁锰离子的去除率都达到了98%以上。
2.3 Ca(OH)2和电石渣对铁锰离子去除效果的对比
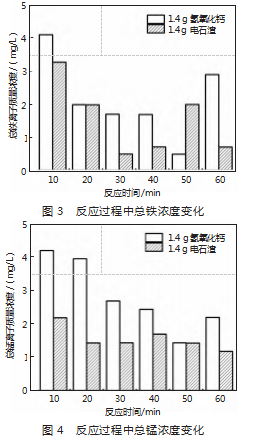
在确定了Ca(OH)2与电石渣在各自应用中的最佳投加量均为1.4 g/L的基础上,为了进一步比较两者的处理效能,设计一项对比分析。将分别投加了1.4 g/L Ca(OH)2和电石渣的两种酸性废水,在完全相同的反应条件下进行处理,并确保它们具有相同的反应时间,测量并记录这两种废水在反应结束后剩余的铁锰离子浓度。通过直接对比这两种废水中的剩余铁锰浓度,在最佳投加量条件下,Ca(OH)2与电石渣在去除酸性废水中铁锰离子方面的实际效果差异,如图3、图4所示。
由图3可知,当酸性废水中加入1.4 g/L的Ca(OH)2反应50 min后,总铁离子质量浓度达到最低点0.48 mg/L,同样浓度的电石渣在仅30 min内就实现了更低的总铁离子质量浓度,电石渣在铁去除上效果更好。Ca(OH)2处理后的废水在60 min时总铁浓度有明显回升,表明其处理效果随时间有退化趋势;电石渣处理后的废水总铁浓度没有回升,电石渣处理表现稳定。因此,从铁去除效果和出水稳定性两方面考量,电石渣优于Ca(OH)2。由图4可知,Ca(OH)2处理酸性废水在50 min时达到总锰浓度的最低点,前40min内总锰浓度下降缓慢,且在60 min时出现回升。而电石渣在20min内就使总锰离子质量浓度降至2 mg/L以下,并保持这一低浓度至反应结束,说明电石渣在锰去除上的效果比Ca(OH)2好。选择电石渣作为酸 性废水的前处理物质,不仅能有效提升废水的碱度,还能在短时间内高效且稳定地去除其中的铁锰金属离子。
3结论
1)探究处理酸性废水的实验中,对比了电石渣与氢氧化钙的效能。结果表明,两者在最佳投加量均为1.4 g/L时,均能有效提升废水pH值至理想范围,符合作为中和剂的标准。在处理效率上,电石渣处理的效率更高。
2)分析两者对废水中总铁和总锰离子残余质量浓度的影响,存在明显区别:电石渣在20min内就能将总锰离子质量浓度降低至2 mg/L以下,并持续保持稳定,这是氢氧化钙所没有的。氢氧化钙处理后的总锰浓度则表现出一定的波动性,处理效果相对较差。最终决定选用电石渣作为中和剂,不仅因为它能高效去除酸性废水中的铁锰元素,还因为实现了“废物利用,以废治污”的环保理念。
参考文献
[1]惠兆松.电厂化学废水处理中重金属离子的去除技术研究[J].纯碱工业,2024(4):26-29.
[2]肖雨洪.工业废水中重金属离子处理方法研究进展[J].浙江化工,2023,54(5):38-44.
[3]庞国强,张勃,刘杨.干熄焦烟气脱硫中高活性氢氧化钙脱硫剂的应用[J].化工设计通讯,2021,47(12):151-152.
[4]李彦鑫,张金山,曹永丹,薛泽民.电石渣的理化性质表征及其应用研究[J].无机盐工业,2018,50(4):49-52.
[5]郝怡臣,李明杰.电石渣的资源化利用技术工业化进展[J].中国氯碱,2023(6):44-48.
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/ligonglunwen/81540.html