摘要:本研究旨在比较液相色谱-三重四级杆串联质谱法(LC-MS/MS)以及紫外分光光度法(UV-Vis),在水样中丁基黄原酸测定中的适用性和性能差异。通过上述两种分析方法,对其方法原理、仪器与试剂、分析条件进行了详细描述,并进行了标准曲线的绘制、样品测定、检出限、精密度和加标回收率的比较分析。本研究结果表明,液相色谱-三重四级杆串联质谱法在水中丁基黄原酸的分析中具有显著优势,不仅提供了更高的分析灵敏度和准确性,还能有效应对复杂水样的分析需求,为环境监测以及水质评估等领域提供了重要的数据支撑。
关键词:丁基黄原酸,紫外分光光度法,液相色谱-三重四级杆串联质谱法
0引言
在环境监测及水质评估工作中,丁基黄原酸作为一种重要的指示性污染物,其准确测定对于评估水体污染程度以及生态环境质量十分关键。传统的分析方法如紫外分光光度法(UV-Vis)和现代的液相色谱-三重四级杆串联质谱法(LC-MS/MS)在这一过程中发挥着关键作用。紫外分光光度法因其操作简便、成本低廉而被广泛应用于水质分析,特别是对于单一成分的测定具有较好的适用性。其原理则是基于分析物吸收紫外光的特性,通过比较吸光度与浓度之间的关系来测定目标物质的含量。然而,UV-Vis法在复杂水样中常受到其他成分的干扰,导致测定精度和特异性方面存在一定的局限性。相比之下,液相色谱-三重四级杆串联质谱法具有高灵敏度、高选择性等优势。该方法通过将液相色谱与质谱联用,利用色谱分离和质谱检测的双重优势,能够有效地分离复杂矩阵中的目标化合物,并准确测定其浓度[1-2]。LC-MS/MS法具备广泛的线性范围、极低的检出限以及良好的精密度和准确度,尤其适用于需要高灵敏度、高选择性的分析场景。
1实验部分
1.1液相色谱-三重四级杆串联质谱法
1.1.1方法原理
样品过滤后直接进样,经液相色谱柱分离,用质谱仪在多反应监测(MRM)条件下检测丁基黄原酸,根据保留时间和特征离子定性,内标法定量。
1.1.2仪器及试剂高效液相色谱-三重四级杆串联质谱仪(4500 Qtrap):质谱仪配备电喷雾离子源;色谱柱:Kinetex 1.7μmEVO C18100A;采样瓶:40 mL棕色玻璃瓶;滤膜:孔径0.22μm。
乙腈,液相色谱纯;氨水,优级纯;甲酸,优级纯;丁基黄原酸标准储备液,直接购买有证标准溶液:100 mg/L;丁基黄原酸标准使用溶液,1.00μg/mL:从丁基黄原酸标准储备溶液中取样,进行稀释配置,于使用前现场制备;内标储备液(购自认证的2,4-二氯苯氧乙酸-13C6标准溶液100 mg/L),内标使用溶液(1.00μg/mL):将内标储备液以水为稀释介质,稀释至1.0 mg/L,使用时现场制备。
1.1.3仪器分析条件
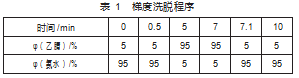
柱温:40℃;流动相A:氨水溶液(pH≈9.5),流动相B:乙腈;流速0.3 mL/min;进样体积10μL;洗脱程序见表1。
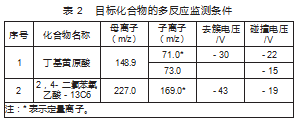
质谱条件,离子源:电喷雾(负离子);监测方式:多反应监测(MRM);离子化电压(IS):-4500 V;雾化气(GS1)压力:345 kPa;辅助气(GS2)压力:379 kPa;气帘气(CUR)压力:172 kPa;离子源温度(TEM):550℃。目标化合物的多反应监测条件见表2。
1.2紫外分光光度法
1.2.1方法原理
紫外分光光度法(UV-Vis)是一种常用的光谱分析技术,适用于测定吸收紫外或可见光的化合物。在测定丁基黄原酸(Butylparaben)时,UV-Vis法基于化合物在紫外区域(200~400 nm)的吸收特性进行分析。丁基黄原酸在紫外区域有较强的吸收特性,通常在约250~280 nm波长范围内具有显著的吸收峰,这种吸收特性是由其分子结构中的芳香环和酯基团引起的。在单波长测量中,选择丁基黄原酸吸收峰附近的一个波长作为工作波长。本次研究中,工作波长选择在260~270 nm之间,利用PDA检测器在整个紫外可见光范围内进行光谱扫描,以获取丁基黄原酸在不同波长下的吸收特性,进而确定最佳测量波长或建立吸收光谱。
1.2.2仪器与试剂
紫外可见分光光度计(SP-756P)配备25 nm石英比色皿、30 mL带塞比色管及0.47μm滤膜。丁基黄原酸标准储备溶液(110μg/mL)可直接购买具有证书的标准溶液。丁基黄原酸标准使用溶液(4.00μg/mL)的操作步骤为:取12.00 mL丁基黄原酸标准储备溶液置于270 mL棕色容量瓶内,加适量水定容至刻度,使用时现配制。饱和碳酸氢钠溶液的制备:称取超过9.8 g碳酸氢钠,溶于100 mL水中,瓶底会有结晶生成。
2测定过程与结果
2.1液相色谱-三重四级杆串联质谱法
2.1.1标准曲线的绘制
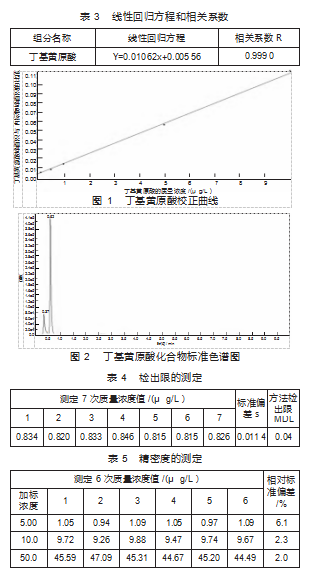
采取适当数量的丁基黄原酸标准使用液,将其置于氨水溶液中,制备质量浓度分别为1.00、5.00、10.0、50.0、100μg/L的标准系列。每毫升标准系列溶液中加入10.0μL内标使用液,以丁基黄原酸的质量浓度为横坐标,丁基黄原酸的峰面积与内标物的峰面积比值和内标物浓度的乘积为纵坐标,建立标准曲线。工作曲线见表3。丁基黄原酸校正曲线和标准色谱图见图1、图2。
2.1.2样品测定
取1.00 mL经0.22μm过滤后的水样于棕色样品瓶中,加入10.0μL内标使用液(1.0 mg/L),同时,取1.00 mL纯水于棕色样品瓶中,加入10.μL内标使用液(1.0 mg/L)进行空白试样的测定。
2.1.3检出限的测定
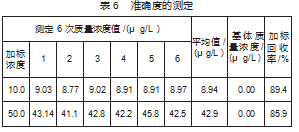
以1.00 mg/L的丁基磺酸标准溶液为原料,制备出0.8μg/L的空白加标水样。按照以下公式计算:MDL=t(n-1,0.99)×S,计算方法检出限为0.04μg/L,结果见表4[3]。
2.1.4精密度的测定
用质量浓度为1.00 mg/L的丁基磺酸标准溶液,配制成质量浓度为5.00、10.0、50.0μg/L样品溶液,进行6次平行测定的相对标准偏差为2.0%~6.1%,符合测定要求。结果见表5。
2.1.5加标回收率的测定
对地表水进行加标,加标质量浓度分别为10.0μg/L和50.0μg/L的样品,进行6次平行测定的回收率为85.9%~89.4%,符合测定要求。测定结果见表6:
2.2紫外分光光度法
2.2.1标准曲线的绘制
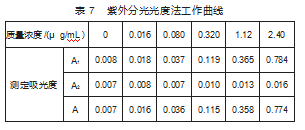
采用丁基黄原酸标准使用溶液,制备两组质量浓度分别为0、0.016、0.080、0.320、1.12、2.40 mg/L的标准系列溶液,分别置于25mL带塞比色管中,第一组加入0.50 mL水。第二组,加入盐酸(1+1)0.10 mL,静止5 min以上,再加饱和碳酸氢钠溶液0.40 mL,放置10 min。在波长301 nm处,以水为参照,测定吸光度(A2)。以吸光度A=[A1-(A2-A0)]为纵坐标,丁基黄原酸含量(μg)作为横坐标形成标准曲线。回归方程为:Y=0.322 7x,相关系数r达到0.999 8[4-5],满足测定要求。
工作曲线见表7。
2.2.2样品测定
取25.0 mL水样于25 mL具塞比色管中,加入0.50 mL水,摇匀。用30 nm石英比色皿,用水为参比,在波长301 nm处测定吸光度(A1)。用纯水代替试样,同步做空白实验,测定的吸光度为A0。
另取25.0 mL水样于25 mL具塞比色管中,进行丁基黄原酸酸化分解处理,加入盐酸(1+1)0.10 mL,静止5 min以上,再加入饱和碳酸氢钠溶液40 mL,放置10 min。待气泡完全赶尽后,以水为参比,在波长301 nm处测定吸光度(A2)。
2.2.3检出限的测定
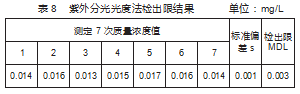
采用丁基黄原酸标准使用溶液,制备质量浓度为0.015 mg/L的样品,并进行7次平行测定。计算7次平行测定结果的偏差,依据公式MDL=t(n-1,0.99)×S2得出检出限为0.003 mg/L。结果见表8。
2.2.4精密度的测定
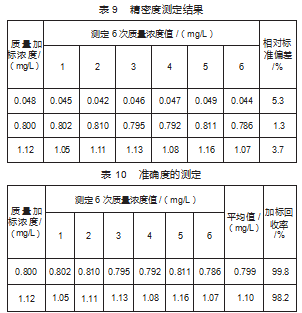
用质量浓度为4.00 mg/L的丁基磺酸标准溶液,配制成质量浓度为0.048、0.800、1.12 mg/L样品溶液,进行6次平行测定的相对标准偏差为1.3%~5.3%。精密度符合测定要求。结果见表9。
2.2.5加标回收率的测定
对地表水进行加标,加标质量浓度分别为0.800 mg/L和1.12 mg/L的样品,进行6次平行测定的加标回收率为98.2%~99.8%。加标回收率符合测定要求。测定结果见表10。
3结论
通过实验结果可以看到:两种方法的检出限均较低,均适用于地表水、地下水、生活污水和工业废水中丁基黄原酸的测定。两种方法比较结果:液相色谱-三重四级杆串联质谱法灵敏度高,检出限较低。但所用的仪器设备AB Sciex高效液相色谱-三重四级杆串联质谱仪价格昂贵、操作过程复杂,对分析人员的能力要求比较高,实验前仪器设备需抽真空时间比较长,实验过程中需要使用有机溶剂乙腈作为流动相,产生的有机废液乙腈具有较高的毒性,对人体的中枢神经系统和肝脏要损害作用,在大气中易挥发,进入水体和土壤会对生态环境造成污染。所使用的流动相有氨水,氨水易对色谱柱和液相系统造成污染,使用氨水流动相会损坏色谱柱填料造成液相色谱柱报废,影响液相色谱分析;而紫外分光光度法具备投资费用少、不需使用有机溶剂和氨水等有毒有害腐蚀性试剂。
参考文献
[1]环境保护部.水质丁基黄原酸的测定紫外分光光度法:HJ 756—2015[S].北京:中国环境科学出版社,2015.
[2]环境保护部.水质丁基黄原酸的测定液相色谱-三重四级杆串联质谱法:HJ 1002—2018[S].北京:中国环境科学出版社,2018.
[3]环境保护部.环境监测分析方法标准制订技术导则:HJ 168—2020[S].北京:中国环境科学出版社,2020.
[4]李廷才,邹本崇.污水中丁基黄原酸盐提取方法的探讨-pH对测定的影响[J].数理医药学杂志,2000,13(4):42.
[5]陈泓霖,邱国良.水中丁基黄原酸的测定方法比较[J].仪器仪表与分析监测,2017(2):40-43.
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/ligonglunwen/80947.html