摘要:本文研发了一种测定食品中二氧化硫(SO₂)的气相色谱-质谱法。首先,将样品放入200 g/L NaCl溶液中超声提取,然后离心,取上清液并加入顶空瓶中(含H₂SO₄溶液)。食品中的SO₂在80℃的酸性条件下反应并生成,同时在气相和液相中实现平衡。利用气相色谱柱GS-GASPRO对气相部分进行分离,然后利用离子扫描(SIM)模式采集数据,以进行定量和定性分析。大批量食品中的SO₂均可采用此方法进行定量和定性测定,相关系数在2.5~100μg范围内为0.999 9,6类典型食品经过加标实验后(3种不同浓度),当添加量为25.0~250 mg/kg时,RSD与回收率分别为0.38%~6.4%、90.1%~104.4%,此方法的检出限为3.0 mg/kg。
关键词:气相色谱-质谱法;二氧化硫;离子扫描;回收率;加标试验
二氧化硫广泛应用于食品加工中,具有防腐、漂白、抗氧化功能。需要注意的是,胡椒、八角与大蒜等香料产品在生长过程中易吸收富集S元素。据GB5009.34—2016标准,目前检测方法测得香料中SO₂的残留量是样品中硫化合物的总量,而非SO₂实际量。为解决此问题,本文的研究结合食品中SO₂实际检测,并使用顶空-气相色谱-质谱(HS-GC-MS)建立了一种更准确、方便的食品中SO₂检测方法。此外使用气相色谱法和热导检测器(TCD)检测草药或汤剂中的SO₂残留也被纳入2015年版的药典。
1实验部分
1.1仪器、试剂与材料
NaCl;H₂SO₄,1.84g/mL;NaOH,AR;Na₂SO₃基准试剂,纯度99.8%。
气相色谱-串联质谱仪,Agilent 7890/7000B;高速离心机,Allegra64RCentrifuge。
1.2标准溶液的配制
称量50 mg的硫酸钠置于容量瓶中,并向其中加入100 mL的水得到质量浓度为500 mg/L的标准溶液。在此基础上,分别量取0.05、0.1、0.2、0.5、1、2m标准溶液,分别向其中加入质量浓度为100 g/L的氢氧化钠溶液1 mL和20 mL质量浓度为200 g/L的氯化钠溶液。同时,再量取4 mL标准溶液,并向其中加入浓度为10 mol/L的硫酸溶液2 mL。将上述配置所得溶液精制备用。
1.3样品前处理
1)均匀试样(淀粉、红糖、果酒等):取精确至0.001 g的样品2.0 g放入离心管内(50 mL),在液体与固体样品中分别加入18 mL与20 mL的NaCl溶液200 g/L),进行漩涡混合10 s后,在超声波10 min的作用后完成对其的提取;在此基础上,将上述的样品在离心机的作用下进行处理,离心机设定的速度为12000 r/min,最后取样品的上清液4 mL备用。
2)均匀试样(白糖及相关制品):采用天平量取2g的样品对其进行破碎处理,并将破碎后的样品置于50 mL离心管中。在离心管中加入氢氧化钠和氯化钠溶液,其中氢氧化钠的质量浓度为100 g/L,体积为1 mL;氯化钠溶液质量浓度为200 g/L,体积为19 mL;加入上述两种溶液后充分混合10 s,同样在超声波和离心机的作用下对其进行提取4 mL上清液备用。
1.4分析条件
1)质谱条件:采用温度为230℃的EI离子源,其电离能量为70 eV,选择离子扫描(SIM)模式,且四极杆温度设定为150℃,其中使用64号离子作为定量限离子,使用48号、50号、66号离子作为定性离子。溶剂延迟时间为4 min。
2)顶空条件:采用容量为20 mL顶空瓶,进样针与加热温度分别设定为105℃与80℃,加热温度维持时间为10 min。进样量与速度分别为500μL与200μL/s,且于进样口停留1 s,进样后采取1 min的吹扫操作。
3)气相色谱条件:采用30 m×0.32 mm规格的气相色谱柱GS-GASPRO,5 min内匀速率将其整体温度从50℃(需保持4 min)升至125℃,色谱柱内流体采用恒流式高纯氦气(纯度≥99.999%),其速度为2.0 mL/min;传输线与进样口温度均为200℃;分流比为1∶20。
2结果与讨论
2.1检测条件的优化
1)色谱柱:本文通过对两种气固色谱柱进行对比分析(GS-GASPRO与PoraPLOT U)。通过改进升温程序,发现PoraPLOTU色谱柱在检测SO₂时存在持续的拖尾现象。但是,从图1中可以看出,基于GS-GASPRO毛细柱可以提高整体的检测精度。因此,针对二氧化硫的检测需求采用GS-GASPRO毛细柱法。
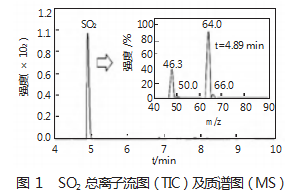
2)酸溶液的选择:通过实验可以看出,采用硫酸溶液相对采用盐酸溶液可获得更高精度的检测结果;而且,盐酸溶液相比较于硫酸溶液其腐蚀性更强。因此,最终确定采用硫酸溶液。
3)标准溶液稳定性:采用碱与非碱溶液对标准溶液进行反应稳定性考察。实验结果表明,无论在哪种溶液中,亚硫酸钠在8 h内拥有着不低于90%的稳定性,因此,其使用的有效时间为8 h。实验样品前处理中引入NaCl溶液(200 g/L)抑制吸水性食品的膨胀性。研究发现,NaCl与蒸馏水对SO₂的影响效果较小,因此,选择NaCl来稀释定容;碱性条件下H₂SO₃的响应强度是非碱性条件的10倍。
4)顶空条件:通过实验表明,随着顶空温度的增加,对应二氧化硫的响应能力越强,同时还会引入大量的水蒸气;而且保温时间对二氧化硫的影响较小。因此,最终确定保温时间为80℃,保温时间为10 min。
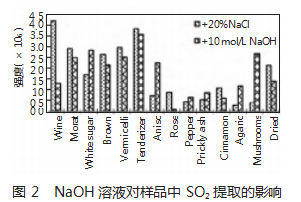
5)NaOH溶液对SO₂提取的影响(图2):是发生亲核加成反应的强亲核试剂。亚硫酸盐在食品中以三种形式存在:可逆、不可逆以及游离态,其中不可逆态盐不会与酸反应产生SO₂。NaOH可释放可逆结合态盐,因此样品中盐通过加入20 mL NaOH(100 g/L)与NaCl(200 g/L)的混合溶液进行提取。此外,前5样产品采用碱性条件提取,后3样产品采用NaCl溶液进行提取。对前边8种样品进行吸附实验可得其饱和吸附点。此外,还考察了碱浓度对SO₂提取效果的影响,实验结果表明,100 g/L NaOH溶液对样品中的亚硫酸盐释放效果最好。
2.2方法学考察
2.2.1标准曲线
基于前文研究成果进行溶液配制绘制SO₂标准曲线,当SO₂质量浓度低于100μg/L时,钠亚硫酸盐的质量浓度与其峰面积的线性相关系数为0.99。标准曲线的线性方程为y=40 964.5x-77 011。
2.2.2检测范围及检出限
根据该方法的信噪比计算,检出限为3.0 mg/kg,定量限为10.0 mg/kg。
2.2.3回收率和精密度
将Na₂SO₃标准溶液添加到6类食品中,经实验发现,添加SO₂量在25.0~250 mg/kg范围内,回收率的平均值为97.2%,相对标准偏差(RSD)范围为0.38%~6.4%。
2.2.4实际样品测定
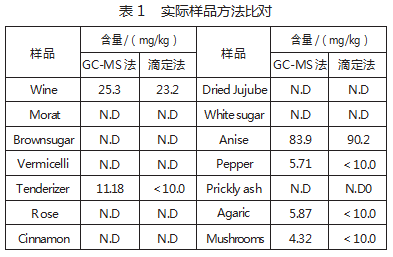
采用滴定方法对14种市售样品中SO₂含量进行比较实验与分析,结果如表1所示。两种方法检测结果相当一致。
3结论
本文研究开发了一种测定食品中二氧化硫(SO₂)含量的GC-MS方法,其简化了前处理且省去蒸馏环节,有效降低检测用时,适用于样品数量较多时的检测。此方法对于部分产品存在回收率低现象,但检测效果差别不大,至于不同产品亚硫酸钠吸收效果与回收率间的具体关系与原因还需深入分析研究。
参考文献
[1]邱宏,肖义夫,钟汉怀.葡萄酒中游离二氧化硫的比色法测定研究[J].中国卫生检验杂志,2018,28(24):2968.
[2]李艳霞,廖丽莎,林萍,等.甲醛吸收-盐酸副玫瑰苯胺-分光光度法测定生粉中亚硫酸盐[J].理化检验:化学分册,2015,51(8):1143.
[3]刘海燕,白冰,时文兴,等.枸杞中二氧化硫含量的测定[J].现代农业科技,2019(3):221.
[4]毛琏,王娣,张兰天,等.凯氏蒸馏-电子滴定器碘滴定法测定食品中的二氧化硫[J].中国食品卫生杂志,2016,28(5):605.
[5]王永姣,张鑫,程方园.电位滴定法测定白术饮片中二氧化硫残留量[J].中国现代中药,2018,20(7):816.
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
据媒体报道,三大运营商目前均已制定了2020年... 详细>>
如何设计有效的环境治理政策, 是学术界和政策... 详细>>
