SCI论文(www.lunwensci.com):
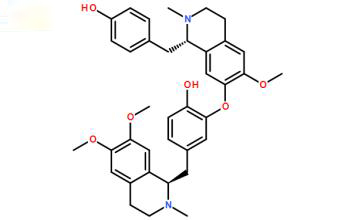
摘 要:目的 研究莲 Nelumbo nucifera Gaertn. 的成熟种子中间绿色胚根(莲子心)的化学成分。方法 利用ODS、Sephadex LH-20、聚酰胺柱色谱及半制备高效液相色谱等方法分离纯化;通过 NMR、MS 等波谱方法鉴定其结构。结果 从莲子心的乙醇提取物中分离得到 8 个化合物,分别鉴定为莲心碱(Liensinine,1)、异莲心碱(Isoliensinine,2)、甲基莲心碱(Neferine,3)、荷叶碱(Nuciferine、4)、去甲乌药碱(Higenamine,5)、3 个黄酮类:芦丁(Rutin,6)、金丝桃苷(Hyperoside,7)、木樨草素 -β-D- 葡萄糖苷(Luteolin-β-D-glycoside,8)。结论 化合物 8 为首次从莲属植物中分离得到。
关键词: 莲子心;生物碱;黄酮
本文引用格式:吕晶 , 韩栋年, 金磊 , 等. 莲子心化学成分研究[J]. 世界最新医学信息文摘 ,2018,18(73):100-101.
0引言
莲子心为睡莲科莲属 NelumboAdans 植物莲 Nelumbo nucifera Gaertn. 的成熟种子中间的绿色胚根,即莲子除去子叶的胚,略呈细棒状,绿色,长 1-1.4 cm,直径约 2 mm[1]。主要分布于湖南,湖北、广东等地,始载于《食性本草》“生取为末,以米饮调下三钱,疗血渴疾、产后渴疾”。莲子心性味苦寒,归心、肺、肾三经,具清心去热,固精止血之功效含有多种化学成分,包括生物碱类、黄酮类、多糖类及挥发油类等成分 [2]。现代药理研究证明其具有抗炎、降血脂、降血糖、抗心律失常及抗癌及等功效 [3]。本实验从莲子心乙醇提取物中分离得到 8 个化合物,分别鉴定为莲心碱(Liensinine,1)、异莲心碱(Isoliensinine,2)、甲基莲心碱(Neferine,3)、荷叶碱(Nuciferine,4)、去甲乌药碱(Higenamine,5)、3 个黄酮类:芦丁(Rutin,6)、金丝桃苷(Hyperoside,7)、木樨草素 -β-D- 葡萄糖苷(Luteolin-β-D-glycoside,8)。其中,化合物 8 为首次从莲属植物中分离得到。
1仪器和材料
电子天平 [ 梅特勒 - 托利多仪器(上海)有限公司 ];闪式提取器(北京金鼎科技发展有限公司);色谱柱(迪马科技有限公司);Agilent 1200 HPLC(美国安捷伦科学仪器有限公司);Bruker-AV-600 型核磁共振仪(瑞士布鲁克公司);柱色谱用硅胶、HSGF254 薄层板(山东青岛海洋化工厂);聚酰胺(沧州宝恩吸附材料科技有限公司);ODS(日本 YMC 公司);Sephedex LH-20(美国 AB 公司);氘代试剂(德国 Merck 公司;化学试剂(分析纯,山东禹王实业有限公司化工分司);莲子心于 2014 年 12 月采购自江西石城。
2提取分离
莲子心药材干燥后称重 10 kg,按照闪式提取技工艺进行提取:17.74 倍量 60% 乙醇溶液提取三次,每次提取时间为 2.76 min,高速离心去除残渣后合并滤液,浓缩共得浸膏2.57 kg。用适量蒸馏水将浸膏分散,分别依次用正己烷、氯仿、正丁醇溶剂进行多次萃取。三氯甲烷萃取物经硅胶柱色谱(200-300 目),氯仿 - 甲醇 - 水(50:3:1、30:3:1、15:3:1、7:3:1); 聚酰胺柱色谱,乙醇 - 水(1:9、3:7、2:3、1:1、7:3);ODS 柱色谱,甲醇 - 水(1:4、2:3、1:1、7:3)梯度洗脱,并结合Sephadex LH-20 柱色谱及半制备高效液相色谱,分离得化合物 1-8。
3结构鉴定
化合物 1:白色无定形粉末,碘化铋钾反应阳性,ESI- MS m/z:611[M+H]+ 。 13C-NMR(600MHz,DMSO-d6)δ: 64.5(C-1),42.4(C-2),44.5(C-3),22.0(C-4),111.4(C-5),55.3(C-6),148.2(C-7),118.0(C-8),130.8(C-11),116.5(C-14),65.1(C-1'),40.5(C-2'),47.60(C-3'),26.2(C-4'),111.3(C-5'),112.2(C-8'),39.7(C-9'),121.5(C-11'),115.5(C-14')。
以上波谱 数据与文献报道基本一致 [4],鉴定该化合物为莲心碱。
化合物 2:白色无定形粉末,碘化铋钾反应阳性,ESI- MS m/z:611[M+H]+ 。 13C-NMR(600MHz,DMSO-d6)δ: 63.9(C-1),42.1(C-2),46.1(C-3),24.8(C-4),110.6(C-5),54.7(C-6),145.1(C-7),113.8(C-8),30.1(C-11),113.2(C-14),64.1(C-1'),42.0(C-2'),46.84(C-3'),25.5(C-4'),112.4(C-5'),118.7(C-8'),38.8(C-9'),110.7(C-11'),115.1(C-14')。
以上波谱 数据与文献报道基本一致 [4],鉴定该化合物为异莲心碱。
化合物 3:白色无定形粉末,碘化铋钾反应阳性,ESI- MS m/z:625[M+H]+ 。 13C-NMR(600MHz,DMSO-d6)δ: 64.4(C-1),42.6(C-2),46.5(C-3),25.0(C-4),111.1(C-5),55.4(C-6),148.9(C-7),112.3(C-8),130.4(C-11),113.4(C-14),64.7(C-1'),42.3(C-2'),47.1(C-3'),26.0(C-4'),111.0(C-5'),119.3(C-8'),39.8(C-9'),120.0(C-11'),115.5(C-14'),125.3(C-15')。
以上波谱数据与文献报道基本一致 [4],鉴定该化合物为甲基莲心碱。
化合物 4:白色针状晶体,熔点 160-162℃,碘化铋钾反应阳性,13C-NMR(600MHz,DMSO-d6)δ:145.5(C-1), 125.6(C-1a),127.0(C-1b),152.2(C-2),110.3(C-3),276.0(C-4),127.6(C-4a),50.0(C-5),71.6(C-6a),34.4(C-7),136.8(C-7a),128.2(C-8),127.5(C-9),126.4(C-10),125.6(C-11),132.3(C-11a),43.6(C of N-CH3),56.1(C of O-CH3),60.6(C of O-CH3)。
以上波谱数据与文献报道基本一致 [5],鉴定该化合物为荷叶碱。
化合物 5:白色针状晶体,熔点 160~162℃,碘化铋钾反应 阳 性 ,ESI-MS m/z:272[M+H]+,13C-NMR(600MHz, DMSO-d6) δ:156.4(C-13),145.0(C-5),144.0(C-6), 130.6(C-10),126.0(C-8),122.4(C-11),122.8(C-15),115.4(C-7),115.2(C-4),55.3(C-9),38.6(C-2)。
以上波谱数据与文献报道基本一致[6],鉴定该化合物为去甲乌药碱。
化合物 6:黄色粉末,10% 的硫酸- 乙醇溶液显色呈黄色,1H-NMR(600MHz,DMSO-d6)δ:12.3(1H,s,5-OH),0.8(1H,s,7-OH),9.7(1H,s,4'-OH),9.2(1H,s,3-OH), 7.6(1H,d,J=2.2Hz,H-2'),7.5(1H,brs,H-6'),6.8(1H, d,J=8.4Hz,H-5'),6.2(1H,d,J=2.0Hz,H-6),6.4(1H,d, J=2.0Hz,H-8),5.3(1H,d,J=7.4Hz,H-1" of Glc),4.4(1H,s,H-1"'of Rha),1.0(3H,d,J=6.2Hz,5-CH3) 。
以上波谱数据与文献报道基本一致[7],鉴定该化合物为芦丁。
化合物 7:黄色结晶,Molish 应呈阳性,13C-NMR(600MHz,DMSO-d6)δ:156.3(C-2),133.5(C-3),177.5(C-4),161.2(C-5),98.6(C-6),164.2(C-7),93.5(C-8),156.3(C-9),103.9(C-10),121.1(C-1'),115.2(C-2'),144.8(C-3'),148.5(C-4'),115.9(C-5'),121.9(C-6'),101.8(C-1"),71.2(C-2"),73.2(C-3"),67.9(C-4"),75.8(C-5"),60.1(C-6")。
以上波谱数据与文献报道基本一致 [8],鉴定该化合物为金丝桃苷。
化合物 8:淡黄色粉末,10% 的硫酸 - 乙醇溶液显色呈黄色,13C-NMR(600MHz,DMSO-d6)δ:164.5(C-2),103.2(C-3),181.9(C-4),161.1(C-5),99.5(C-6),162.9(C-7),94.7(C-8),156.9(C-9),105.3(C-10),121.4(C-1'),113.6(C-2'),145.8(C-3'),149.9(C-4'),115.9(C-5'),119.2(C-6'),99.9(C-1"),73.1(C-2"),77.2(C-3"),69.5(C-4"),76.4(C-5"),60.6(C-6")。
以上波谱数据与文献报道基本一致 [9],鉴定该化合物为木樨草素 -β-D- 葡萄糖苷。
4结论
莲子心乙醇提取物经萃取后,活性追踪结果表明氯仿层抗炎活性最强,故选择氯仿层进行分离纯化,并得到 8 种有效成分。本研究为进一步的莲子心药理学研究奠定了物质基础。
参考文献:
[1]国家药典委员会. 中华人民共和国药典 3 部[M]. 中国医药科技出版社 ,2010.
[2]曾建伟, 吴锦忠 , 张书娟. 莲子心药学研究进展[J]. 福建中医药大学学报 ,2005(S1):40-42.
[3]谢纲, 曾建国. 莲子心的主要成分和药理作用研究进展 [C]. 中华中医药学会中药鉴定学术研讨会、2007 年中国中西医结合学会中药专业委员会全国中药学术研讨会,2007.
[4]WuS,Sun C,Cao X ,et al.Preparative counter-current chromatography isolation of liensinine and its analogues from embryo of the seed of Nelumbo nucifera GAERTN. using upright coil planet centrifuge with four multilayer coils connected in series[J]. Journal of Chromatography A,2004,1041(1–2):153-162.
[5]李萍, 杨光明 , 张玉玲, 等. 莲子心脂溶性生物碱的分离、鉴定 [J]. 食品与生物技术学报 ,2016,35(01):19-27.
关东, 陈新民. 手性去甲乌药碱及其盐的制备方法 [J]. 医药前沿,2015,30(5):360-362.
[6]孙建瑞, 王大红 , 邱智军, 等. 连翘叶中连翘酯苷 A、芦丁和连翘苷提取纯化工艺优化 [J]. 食品科学,2017,38(14):200-205.
[7]李柰, 龙立梅, 樊琛 , 等. 蜀葵花中金丝桃苷及其异构体的分离纯化 [J]. 食品科学,2015,36(4):131-135.
[8]凌云, 何板作, 鲍燕燕 , 等. 浮萍的化学成分研究 [J]. 中草药 ,1999(02):88-90.
《莲子心化学成分研究论文》附论文PDF版下载:
http://www.lunwensci.com/uploadfile/2018/1113/20181113023854708.pdf
关注SCI论文创作发表,寻求SCI论文修改润色、SCI论文代发表等服务支撑,请锁定SCI论文网!
文章出自SCI论文网转载请注明出处:https://www.lunwensci.com/yixuelunwen/1594.html